Содержание
- 2. Превращения белков и азотистых экстрактивных веществ Ослизнение. Сплошной рост аэробных бактерий. Аэробы, развивающиеся в кислой среде,
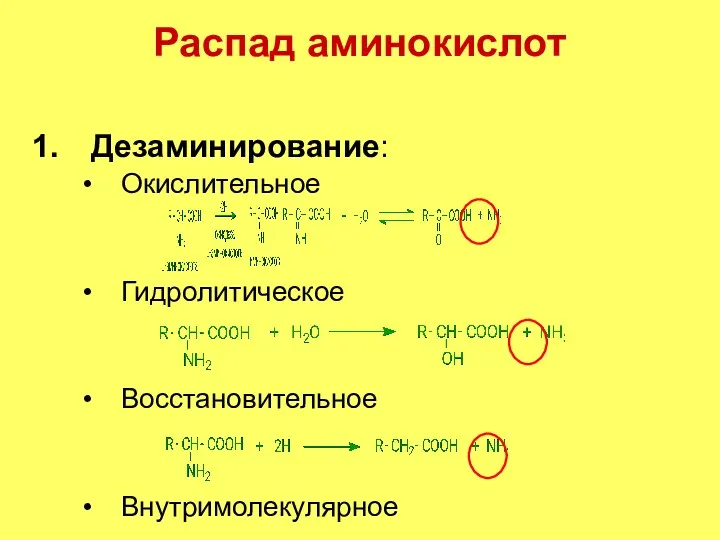
- 3. Распад аминокислот Дезаминирование: Окислительное Гидролитическое Восстановительное Внутримолекулярное
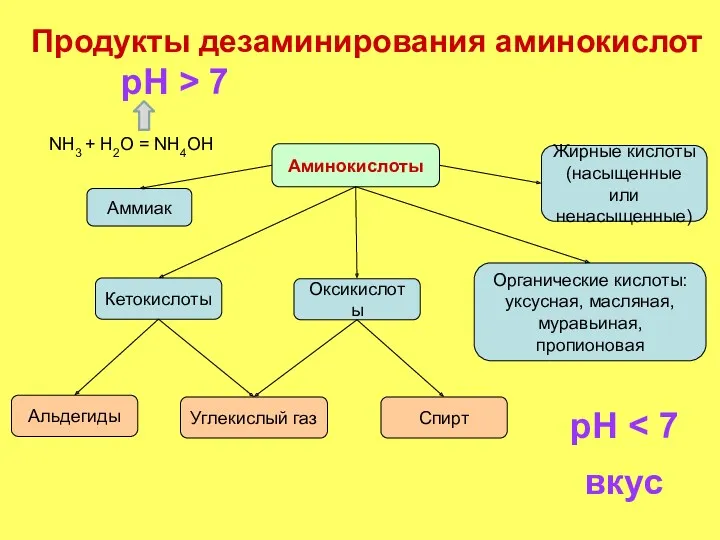
- 4. Продукты дезаминирования аминокислот Аминокислоты Аммиак Кетокислоты Оксикислоты Жирные кислоты (насыщенные или ненасыщенные) Органические кислоты: уксусная, масляная,
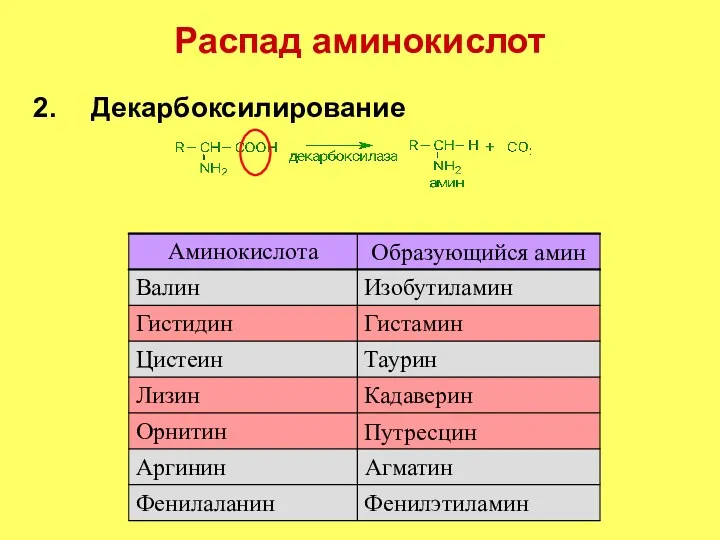
- 5. Распад аминокислот Декарбоксилирование Фенилэтиламин Фенилаланин Путресцин Орнитин Агматин Аргинин Кадаверин Лизин Таурин Цистеин Гистамин Гистидин Изобутиламин
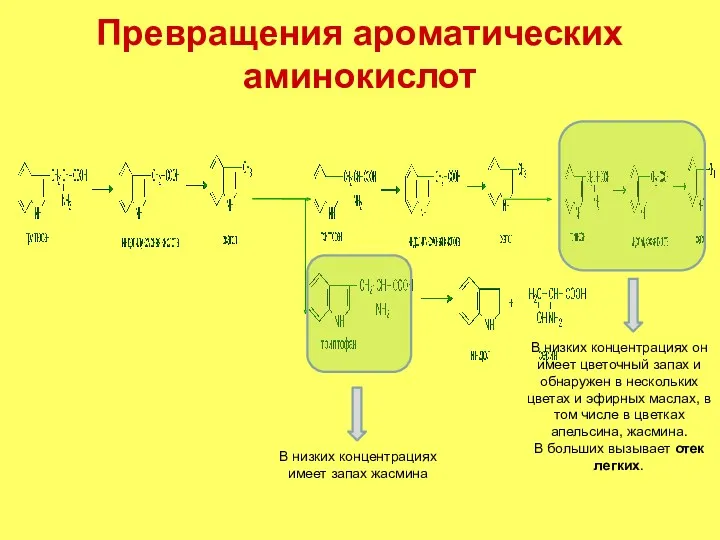
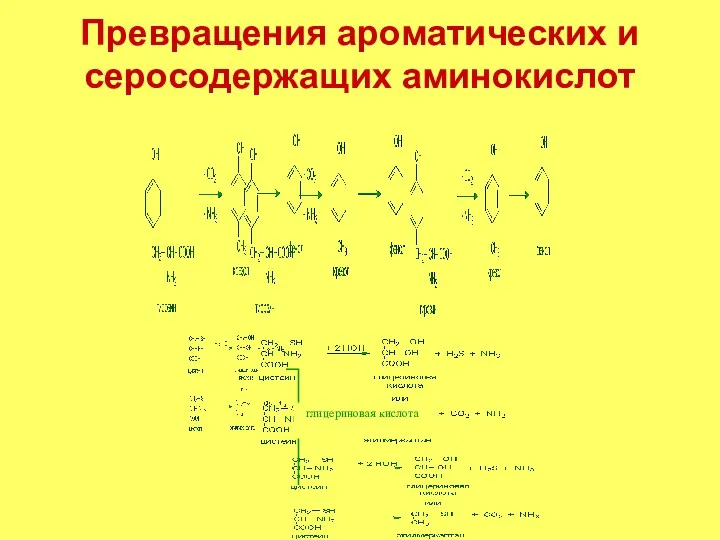
- 6. Превращения ароматических аминокислот В низких концентрациях он имеет цветочный запах и обнаружен в нескольких цветах и
- 7. Превращения ароматических и серосодержащих аминокислот глицериновая кислота
- 8. Превращения белков и азотистых экстрактивных веществ Карбоновые жирные (уксусная, масляная, муравьиная); Оксикислоты Амины Альдегиды Неорганические вещества
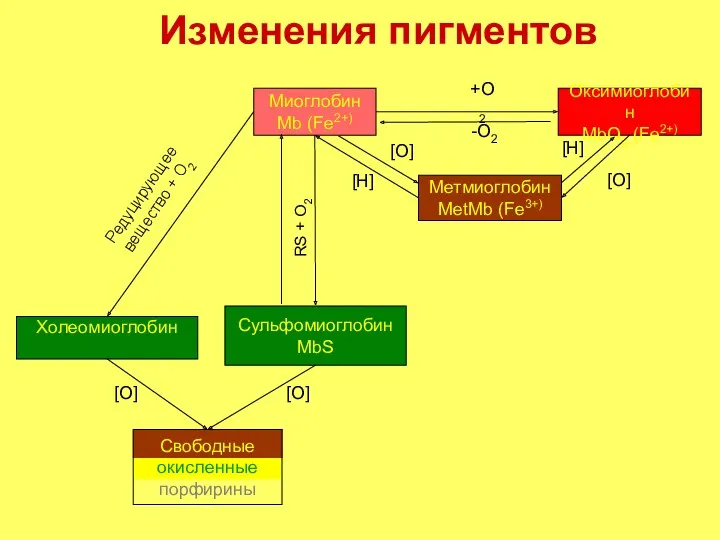
- 9. Изменения пигментов Оксимиоглобин MbO2 (Fe2+) Метмиоглобин MetMb (Fe3+) Миоглобин Mb (Fe2+) +О2 -О2 [О] [Н] [Н]
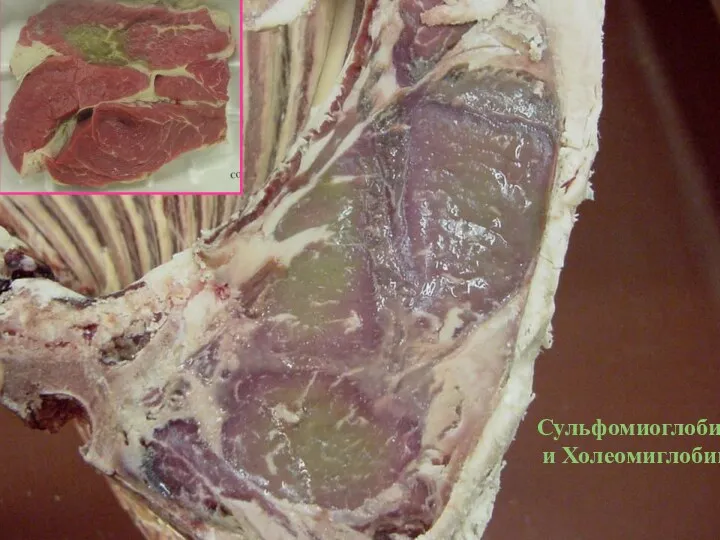
- 10. Сульфомиоглобин и Холеомиглобин
- 11. Биохимические и физико-химические изменения жиров Гидролитические Окислительные
- 12. Гидролитические изменения тканевых жиров В свежей жировой ткани кислотное число обычно не выше 0,05-0,2 ТГ ДГ
- 13. Факторы, влияющие на гидролиз жира: Температура. Высокая влажность. Обсеменение микрофлорой. Неполная денатурация белков при вытопке жира.
- 14. Окислительные изменения жиров Образование перекисей: Образование активированной реакционноспособной молекулы: RH + hv ↔ R*H Распад на
- 15. Автоокисления жиров Поглощение квантов света: R1-CH2-CH=CHR2 + hv → R1-CH∙-CH=CHR2 + H∙ Образование перекисного радикала: R1-CH∙-CH=CHR2
- 16. Перекисное число Индукционный период: очень мало молекул с повышенной кинетической энергией (возбужденных или свободных радикалов) наличие
- 17. Каталитическое действие металлов легкоокисляющиеся металлы (окислы или соли железа, меди, свинца, олова) органические соединения, содержащие железо:
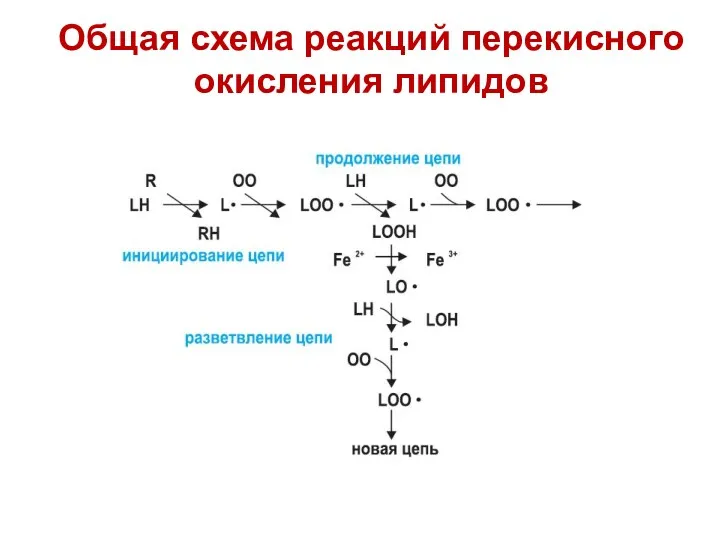
- 18. Общая схема реакций перекисного окисления липидов
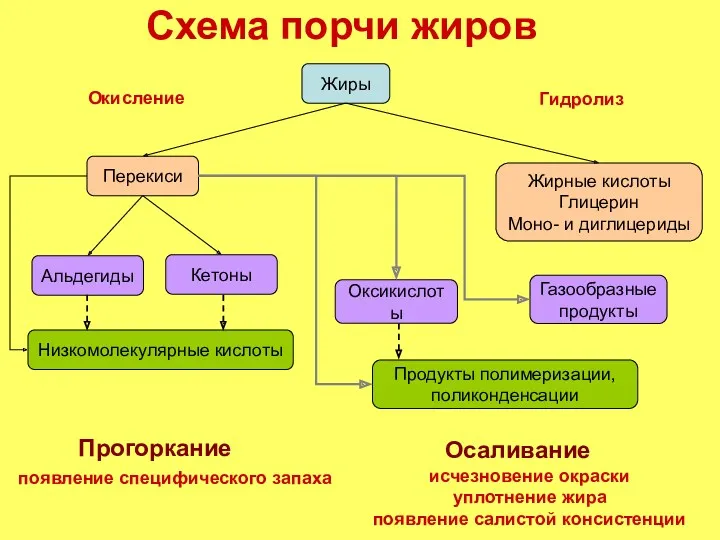
- 19. Схема порчи жиров Жиры Перекиси Жирные кислоты Глицерин Моно- и диглицериды Окисление Гидролиз Альдегиды Кетоны Низкомолекулярные
- 20. Изменение биологической ценности жиров Окисление жизненно необходимых, ненасыщенных жирные кислот. Образование ядовитых веществ (мускарин, триметиламин и
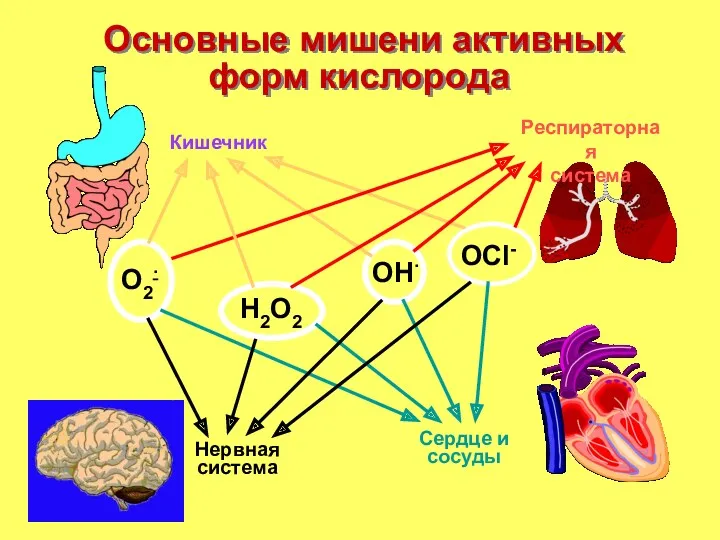
- 21. Основные мишени активных форм кислорода O2∙ H2O2 OСl- OH∙ Кишечник Сердце и сосуды Респираторная система Нервная
- 22. Последствия окислительного стресса Повреждение мембран на молекулярном уровне: Активация перекисного окисления липидов Нарушение жидкокристаллической структуры Увеличение
- 23. Химические принципы предохранения жиров от порчи Уменьшить (исключить) контакт жира с кислородом воздуха и с источниками
- 24. Антиокислители (антиоксиданты) не должны обладать вредными для организма свойствами при введении в жир они не должны
- 25. Механизм действия антиокислителей L + hv → L∙ L∙ + O2 → LOO∙ LOO∙ + AH
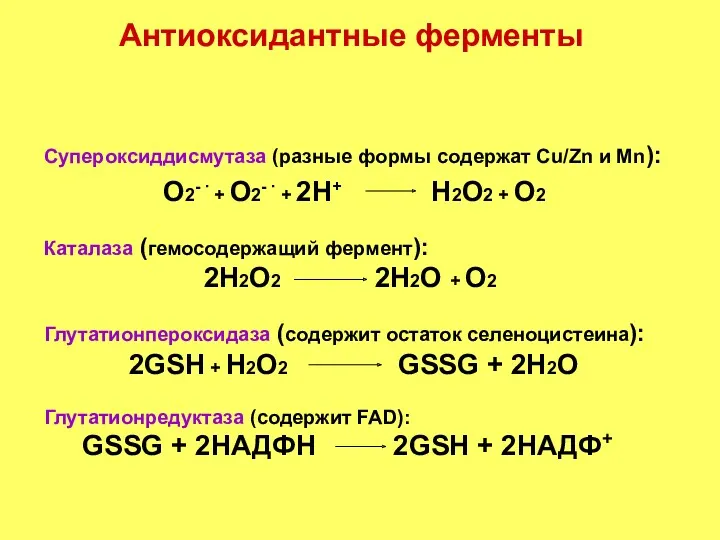
- 26. Супероксиддисмутаза (разные формы содержат Cu/Zn и Mn): О2- ∙ + О2- ∙ + 2Н+ Н2О2 +
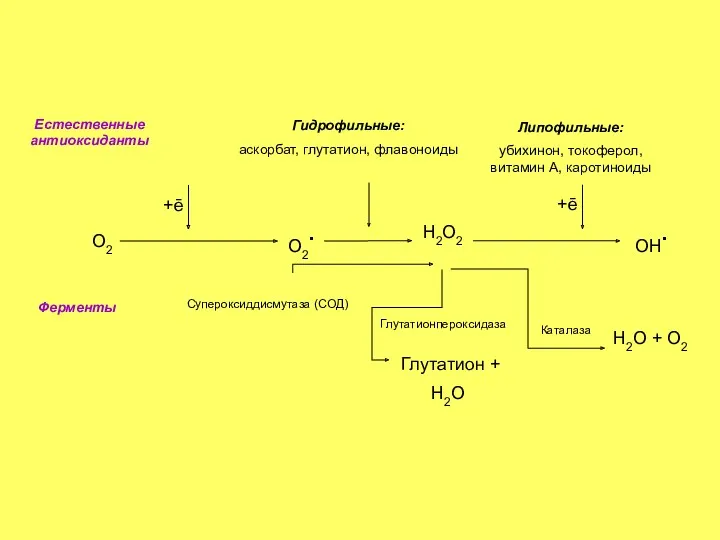
- 27. О2 О2. Н2О2 ОН. Естественные антиоксиданты Ферменты Гидрофильные: аскорбат, глутатион, флавоноиды +ē Липофильные: убихинон, токоферол, витамин
- 29. Скачать презентацию













 Обратимость химических реакций. Химическое равновесие
Обратимость химических реакций. Химическое равновесие Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Выращивание кристаллов в домашних условиях
Выращивание кристаллов в домашних условиях Легированные стали
Легированные стали Фенолы
Фенолы Теплота сгорания топлива
Теплота сгорания топлива Физико-химические свойства сырья, продукции, реагентов и материалов (часть 2)
Физико-химические свойства сырья, продукции, реагентов и материалов (часть 2) Химическая связь
Химическая связь Генетическая связь между классами неорганических веществ. Химический тренажёр
Генетическая связь между классами неорганических веществ. Химический тренажёр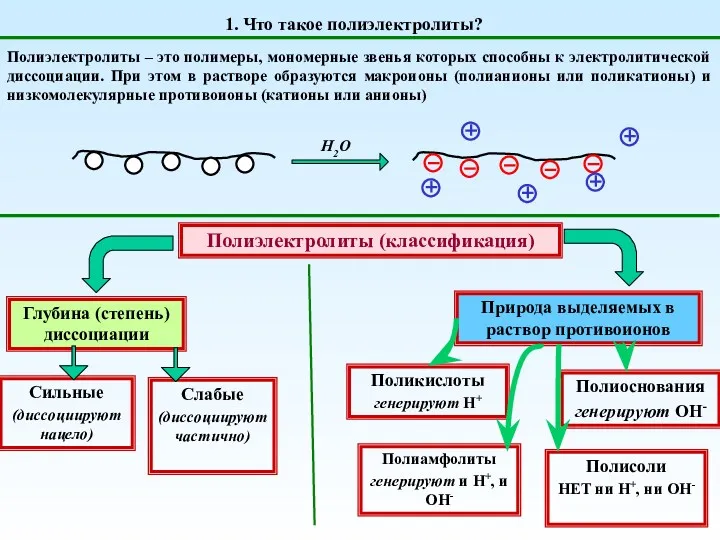 Полиэлектролиты. (Тема 3)
Полиэлектролиты. (Тема 3) Источники углеводородов
Источники углеводородов Химия 20 века
Химия 20 века Амины. Анилин
Амины. Анилин Аквамарин
Аквамарин Непредельные углеводороды этиленового ряда (олефины, алкены)
Непредельные углеводороды этиленового ряда (олефины, алкены) Ультраосновные породы (гипербазиты)
Ультраосновные породы (гипербазиты) Природные (натуральные) полимеры. Композиционные материалы
Природные (натуральные) полимеры. Композиционные материалы Химические свойства основных неорганических соединений в свете ЭД и ОВР. 9 класс
Химические свойства основных неорганических соединений в свете ЭД и ОВР. 9 класс Нуклеиновые кислоты. Нуклеотиды
Нуклеиновые кислоты. Нуклеотиды Методы исследования гидрохимического режима водоемов
Методы исследования гидрохимического режима водоемов Сложные эфиры
Сложные эфиры Металлы в нашей жизни
Металлы в нашей жизни Химические реакции. Условия необходимые для протекания химических реакций?
Химические реакции. Условия необходимые для протекания химических реакций? Коррозия металлов. Способы защиты металлов от коррозии
Коррозия металлов. Способы защиты металлов от коррозии Штучні і синтетичні волокна
Штучні і синтетичні волокна Методы окислительно-восстановительного и комплексонометри-ческого титрования
Методы окислительно-восстановительного и комплексонометри-ческого титрования Теоретические основы органической химии
Теоретические основы органической химии Что такое химия. Техника безопасности. Интересные факты (урок 1)
Что такое химия. Техника безопасности. Интересные факты (урок 1)