Слайд 2

Слайд 3

КОРРОЗИЯ – самопроизвольное разрушение металлов и сплавов в результате химического или
электрохимического взаимодействия их с окружающей средой.
Это окислительно-восстановительная реакция, при которой атомы металла превращаются в ионы. Чем активнее металл, тем он больше подвержен коррозии.
В роли окислителя выступают атмосферный кислород и катионы водорода.
Слайд 4

ЗНАЧЕНИЕ КОРРОЗИИ
Вызывает серьезные экологические последствия: утечка нефти, газа, других химических продуктов.
Недопустима
во многих отраслях промышленности: авиационной, химического, нефтяного и атомного машиностроения.
Отрицательно влияет на жизнь и здоровье людей.
Слайд 5

ФАКТОРЫ,
ВЫЗЫВАЮЩИЕ КОРРОЗИЮ
Кислород и влага атмосферы
Углекислый и сернистый газы, содержащиеся в
атмосфере
Морская вода
Грунтовые воды
Слайд 6
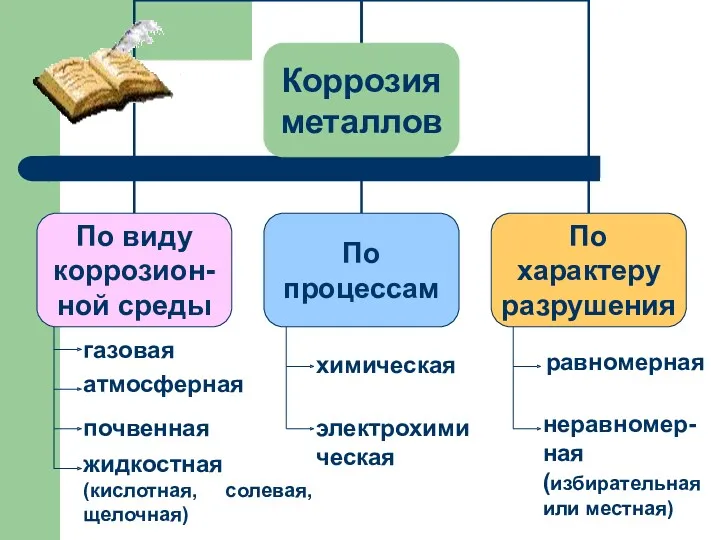
газовая
атмосферная
почвенная
жидкостная (кислотная, солевая, щелочная)
химическая
электрохимическая
равномерная
неравномер- ная (избирательная или местная)
Слайд 7

ВИДЫ КОРРОЗИИ
ХИМИЧЕСКАЯ – это разрушение металлов и сплавов в результате их
химического взаимодействия с веществами окружающей среды.
Защитная оксидная пленка на поверхности алюминия
Рыхлая пленка на поверхности железа, приводящая к разрушению металла
Слайд 8

Слайд 9

ВИДЫ КОРРОЗИИ
ЭЛЕКТРОХИМИЧЕСКАЯ – это разрушение металлов, которое сопровождается возникновением электрического тока
в воде или среде другого электролита.
Химические процессы – это окисление корродируемого металла, отдача электронов.
Электрические процессы – перенос электронов с одного участка изделия к другому.
Слайд 10

УСЛОВИЯ,
СПОСОБСТВУЮЩИЕ ЭЛЕКТРОХИМИЧЕСКОЙ КОРРОЗИИ
Положение металла в ряду активности металлов: чем они
дальше расположены друг от друга, тем быстрее происходит коррозия.
Чистота металла: примеси ускоряют коррозию.
Неровности поверхности металла, трещины.
Грунтовые воды, морская вода, среда электролита.
Повышение температуры.
Действие микроорганизмов (грибы, бактерии и лишайники воздействуют на металл с высокой коррозионной стойкостью).









 Количество вещества. Моль
Количество вещества. Моль Основы органической химии
Основы органической химии Методические рекомендации по изучению курса Коррозия и защита металлов
Методические рекомендации по изучению курса Коррозия и защита металлов Рекомендации по оформлению развёрнутых ответов на задания ЕГЭ
Рекомендации по оформлению развёрнутых ответов на задания ЕГЭ Кремний. Применение кремния
Кремний. Применение кремния Титанның химиялық элементі
Титанның химиялық элементі Твердое состояние вещества. Плавление
Твердое состояние вещества. Плавление Химиядан сұрақтар
Химиядан сұрақтар Кислород. Атом кислорода
Кислород. Атом кислорода Природные источники углеводородов
Природные источники углеводородов Қатты күйдегі препараттар
Қатты күйдегі препараттар Радиусы атомов и ионов
Радиусы атомов и ионов Теорія горіння та вибуху
Теорія горіння та вибуху Химия. Изучение жиров
Химия. Изучение жиров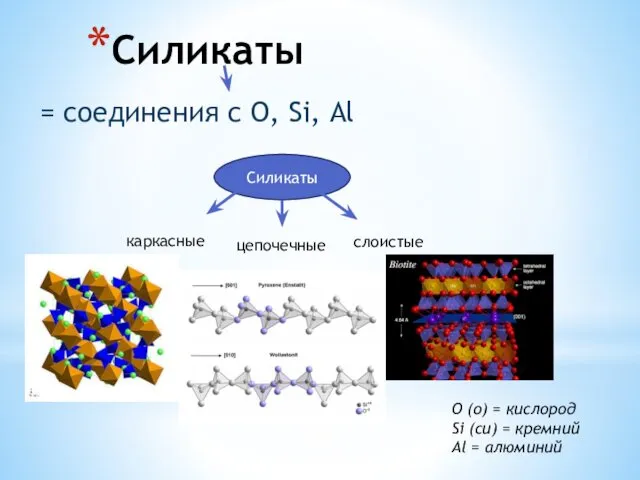 Силикаты. Слюды. Тальк. Фосфаты. Апатит. Крокоит
Силикаты. Слюды. Тальк. Фосфаты. Апатит. Крокоит Индикаторы кислотно-основного титрования
Индикаторы кислотно-основного титрования Solutions and solubilities
Solutions and solubilities Хімічні сполуки у побуті
Хімічні сполуки у побуті Физические, химические свойства предельных и непредельных карбоновых кислот, получение
Физические, химические свойства предельных и непредельных карбоновых кислот, получение Кислородсодержащие органические соединения. Спирты. 10 класс
Кислородсодержащие органические соединения. Спирты. 10 класс Химическая связь
Химическая связь Как и где используется соляная кислота
Как и где используется соляная кислота Виды химической связи
Виды химической связи Вода. Растворимость, растворы
Вода. Растворимость, растворы Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Электролитическая диссоциация кислот, солей и оснований Степень электролитической диссоциации. Сильные и слабые электролиты
Электролитическая диссоциация кислот, солей и оснований Степень электролитической диссоциации. Сильные и слабые электролиты Обмоточные провода
Обмоточные провода Классификация химических реакций
Классификация химических реакций