Содержание
- 2. Обобщение и закрепление знаний по теме: «Химическая связь. Строение веществ» Цель:
- 4. Ионная химическая связь Ковалентная неполярная химическая связь Ковалентная полярная химическая связь Металлическая химическая связь
- 5. Повторение основных понятий
- 6. 1.Что такое химическая связь? 2. Электроны, за счет которых атомы вступают в химические связи называются ………
- 7. 4. Что указывает на число этих электронов? 5. Сколько валентных электронов в атоме Са и N?
- 8. 7. Ионная связь - это … … … 8. Что такое электроотрицательность? 9. Электроотрицательность в периоде
- 9. Ионная- это связь, которая образуется между ионами металла и неметалла за счет принятия и отдачи электронов
- 10. Образование ионов и их взаимодействие. Na Cl NaCl +
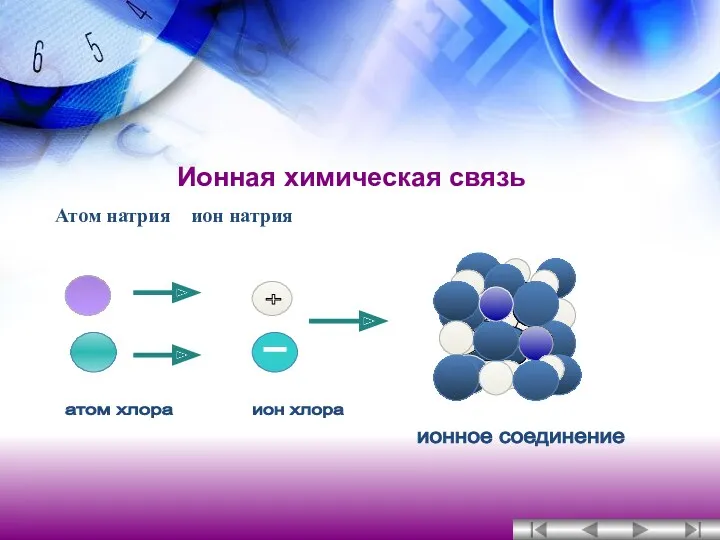
- 11. Ионная химическая связь Атом натрия ион натрия атом хлора ион хлора + ионное соединение
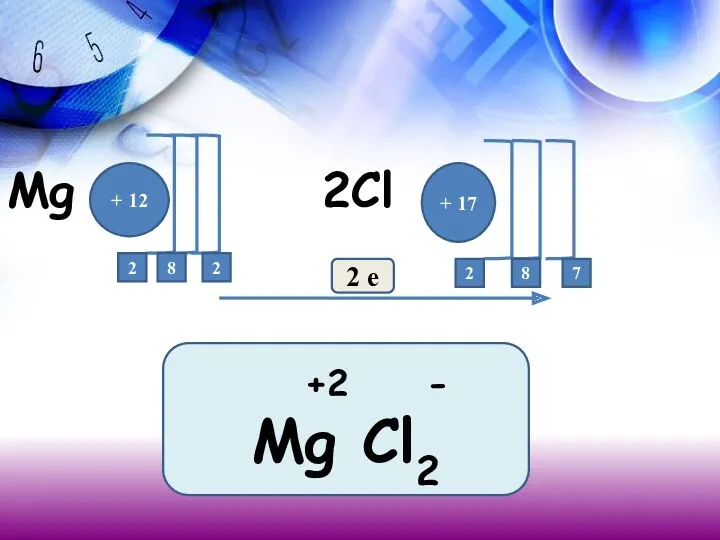
- 12. + 12 2 + 17 7 2 е 2 2 8 8 +2 - Mg Cl2
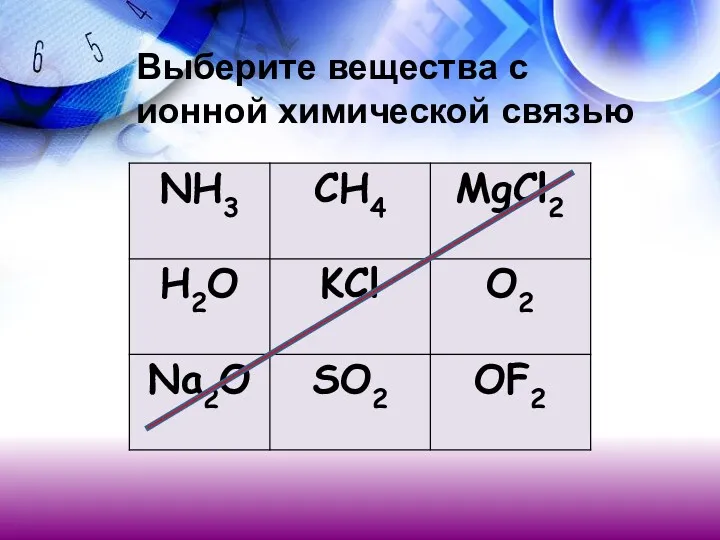
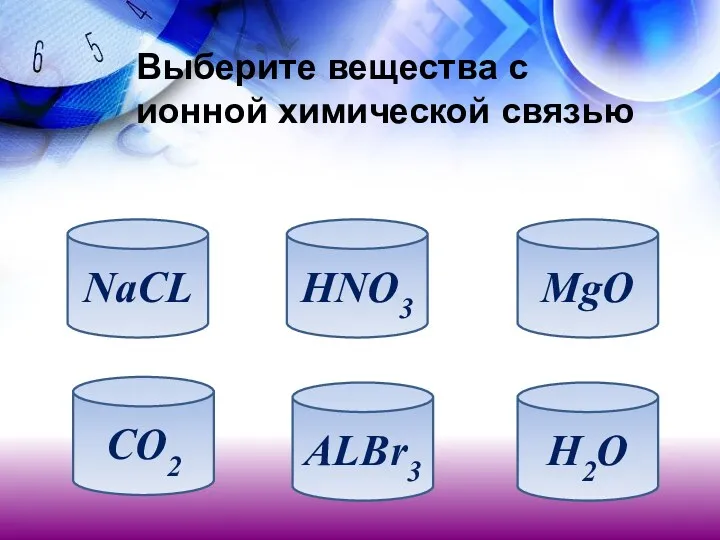
- 13. Выберите вещества с ионной химической связью
- 14. Выберите вещества с ионной химической связью NaCL CO2 ALBr3 H2O MgO HNO3
- 15. Ковалентная полярная связь
- 16. Химическая связь, возникающая в результате образования общих электронных пар, называется ковалентной. Связь возникающая между разными неметаллами
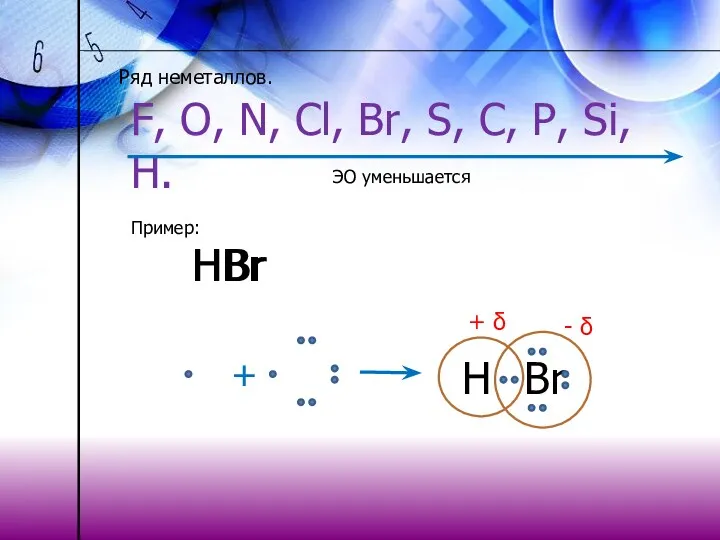
- 17. Ряд неметаллов. F, O, N, Cl, Br, S, C, P, Si, H. ЭО уменьшается Пример: НBr
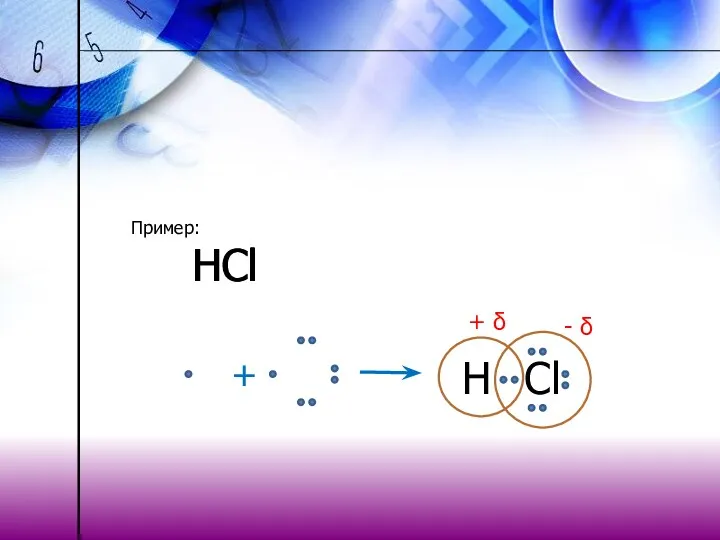
- 18. Пример: НCl Н Cl + Н Cl - δ + δ
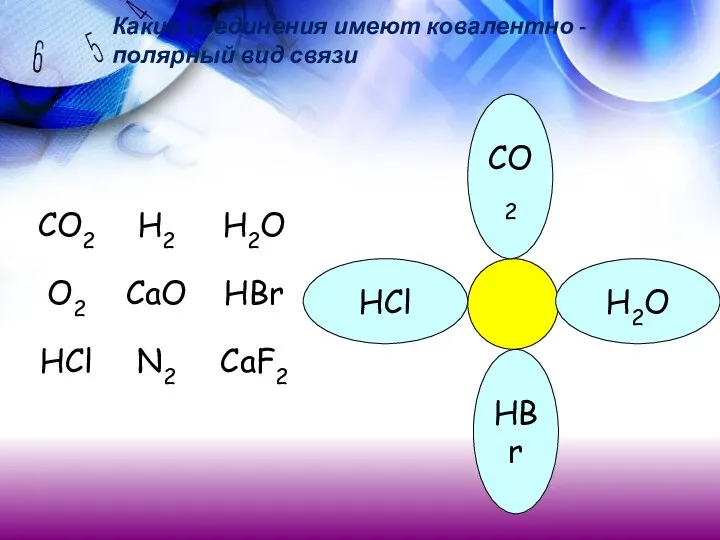
- 19. CО2 H2O HBr НCl Какие соединения имеют ковалентно -полярный вид связи
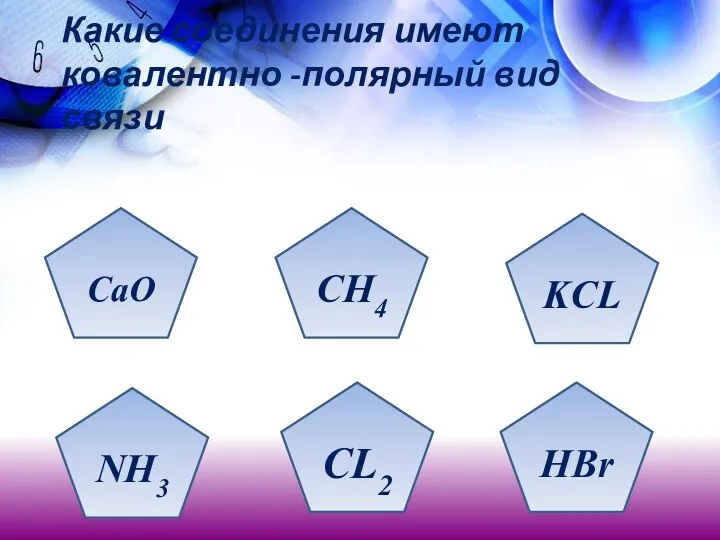
- 20. Какие соединения имеют ковалентно -полярный вид связи CaO NH3 CL2 HBr KCL CH4
- 21. Ковалентная неполярная связь
- 22. Химическую связь ,возникающую в результате образования общих электронных пар ,называют ковалентной. Ковалентная неполярная связь образованна между
- 23. а) Cl2 N2 Cu __________________ б) Н2О PH3 O2 __________________ «Третий лишний»
- 24. Из перечня веществ выберите формулы с ковалентной неполярной связью Cl2 CO2 Mg H2O O3 N2
- 25. Металлическая химическая связь
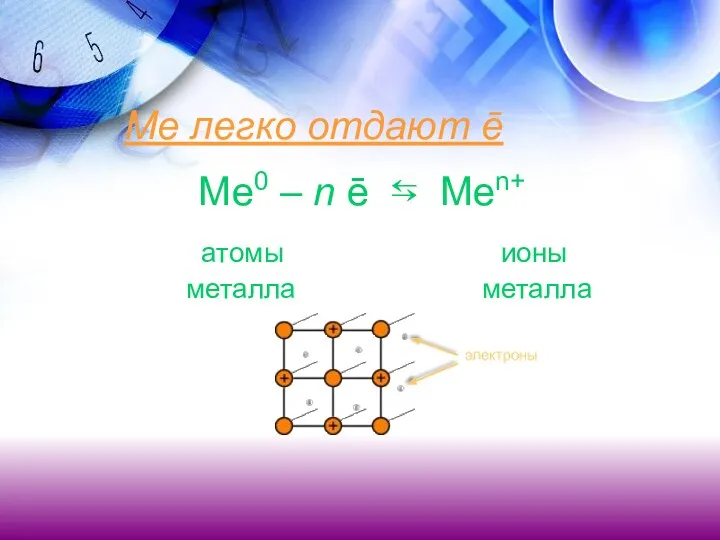
- 26. Ме легко отдают ē Ме0 – n ē ⇆ Men+ атомы ионы металла металла электроны
- 27. Связь в металлах атом-ионами посредством обобществленных электронов называют металлической Атомы большинства металлов на внешнем уровне содержат
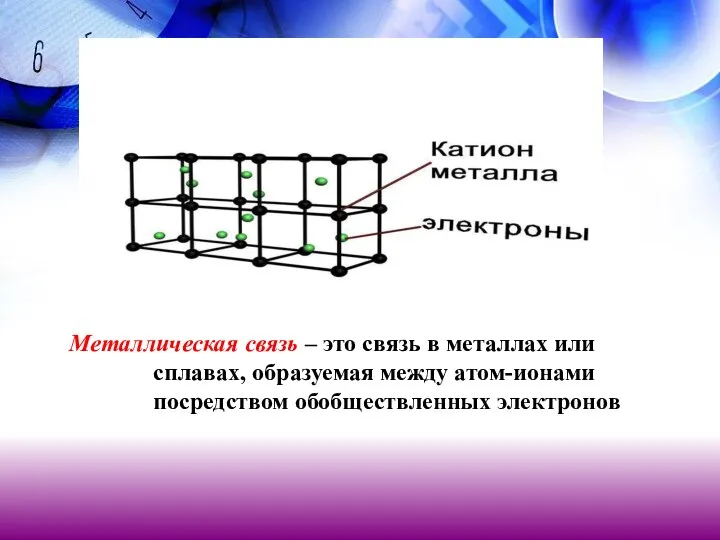
- 28. Металлическая связь Металлическая связь – это связь в металлах или сплавах, образуемая между атом-ионами посредством обобществленных
- 30. Химическая гимнастика Физическое тело – вращение плечами назад; Вещество– вращение плечами вперед Кислород Карандаш Углерод Гвоздь
- 31. Химическая гимнастика Формула простого вещества – поворот головы к правому плечу; Формула сложного вещества – поворот
- 32. Сравнение различных видов связи Сходство: любой вид связи образуется за счет перехода электронов Различие: способ образования
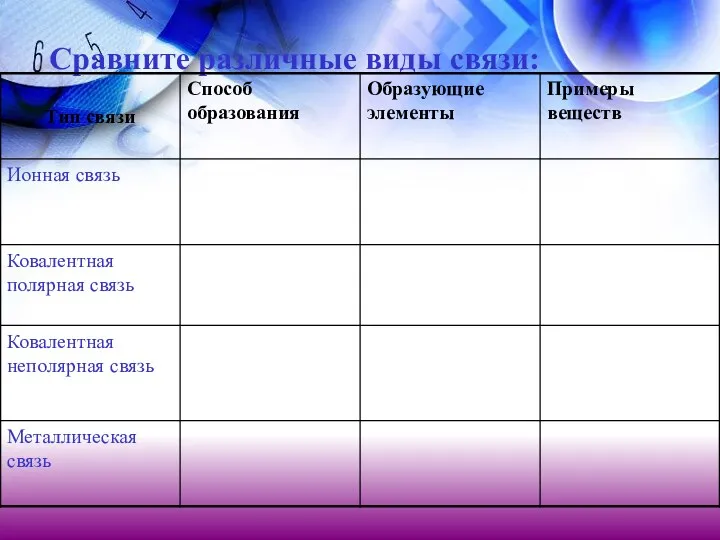
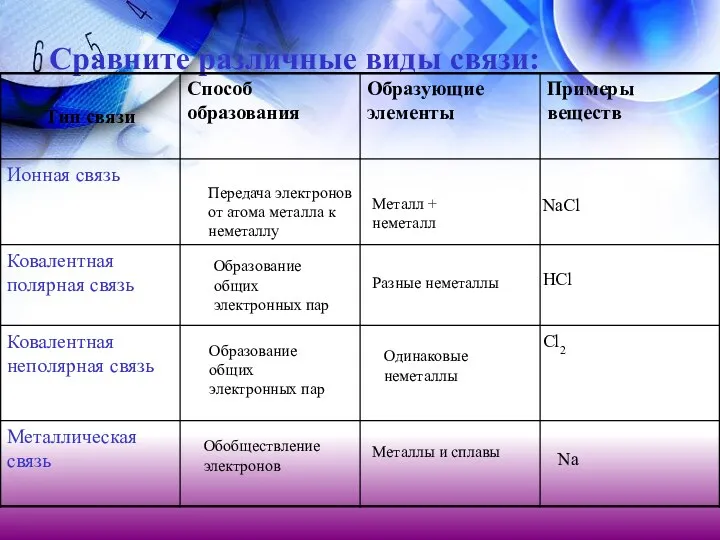
- 33. Сравните различные виды связи:
- 34. Сравните различные виды связи: Передача электронов от атома металла к неметаллу Образование общих электронных пар Образование
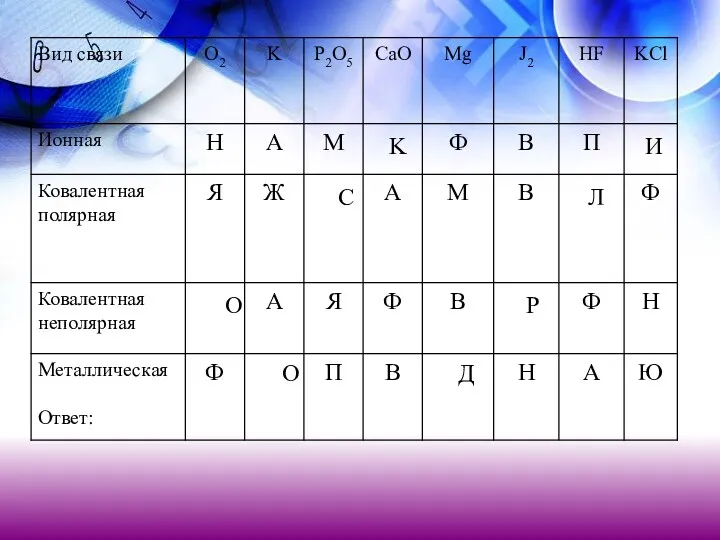
- 35. Задание: Составьте формулы веществ с различными видами связи, выбрав элементы из списка: Na N S Al
- 36. K И С Л О Р О Д
- 38. Скачать презентацию





















 Взаимодействия кислорода с металлом
Взаимодействия кислорода с металлом Соли (12 класс)
Соли (12 класс) Хімічний зв’язок
Хімічний зв’язок Токсичні характеристики найбільш розповсюджених небезпечних хімічних речовин і симптоми ураження
Токсичні характеристики найбільш розповсюджених небезпечних хімічних речовин і симптоми ураження Пластмаси. Пластичні маси
Пластмаси. Пластичні маси Титриметрический метод анализа
Титриметрический метод анализа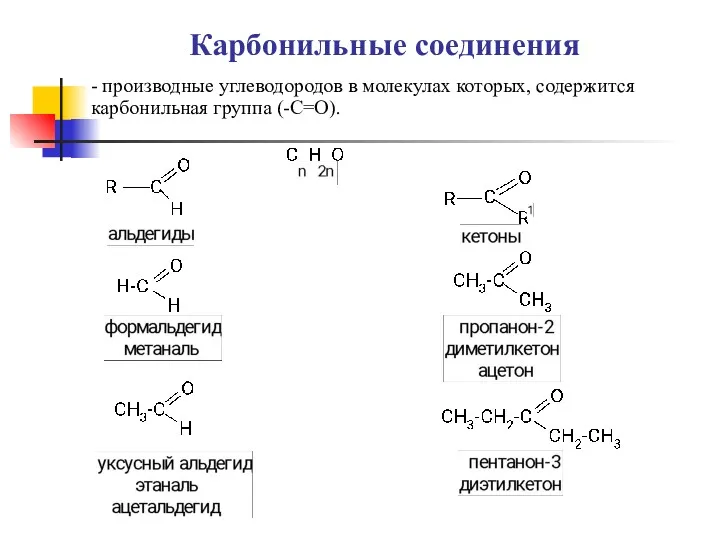 Карбоновые кислоты, альдегиды
Карбоновые кислоты, альдегиды Химическое равновесие в гомогенных системах. Ионное произведение воды. 12 класс
Химическое равновесие в гомогенных системах. Ионное произведение воды. 12 класс Положение тугоплавких металлов в Периодической системе элементов
Положение тугоплавких металлов в Периодической системе элементов Основания. Неорганические соединения
Основания. Неорганические соединения Жиры. История открытия, строение, классификация, свойства
Жиры. История открытия, строение, классификация, свойства Перманганат калия
Перманганат калия Массовая доля элемента в веществе
Массовая доля элемента в веществе Введение в химическую технологию топлив и углеродных материалов
Введение в химическую технологию топлив и углеродных материалов Высокомолекулярные соединения и супрамолекулярные структуры. (Лекция 3)
Высокомолекулярные соединения и супрамолекулярные структуры. (Лекция 3) Расчеты по химическим уравнениям. 8 класс
Расчеты по химическим уравнениям. 8 класс Акцепторы катионов и анионов. Краун-эфиры и близкие структурные аналоги: поданды, лариатэфиры. Супрамолекулярная фотоника
Акцепторы катионов и анионов. Краун-эфиры и близкие структурные аналоги: поданды, лариатэфиры. Супрамолекулярная фотоника Поверхностно-активные вещества (ПАВ). Классификация ПАВ по степени влияния на окружающую среду
Поверхностно-активные вещества (ПАВ). Классификация ПАВ по степени влияния на окружающую среду Кремний и его соединения. Нахождение в природе
Кремний и его соединения. Нахождение в природе Лекция №11 ДИСПЕРСНЫЕ СИСТЕМЫ И РАСТВОРЫ
Лекция №11 ДИСПЕРСНЫЕ СИСТЕМЫ И РАСТВОРЫ Кислоты
Кислоты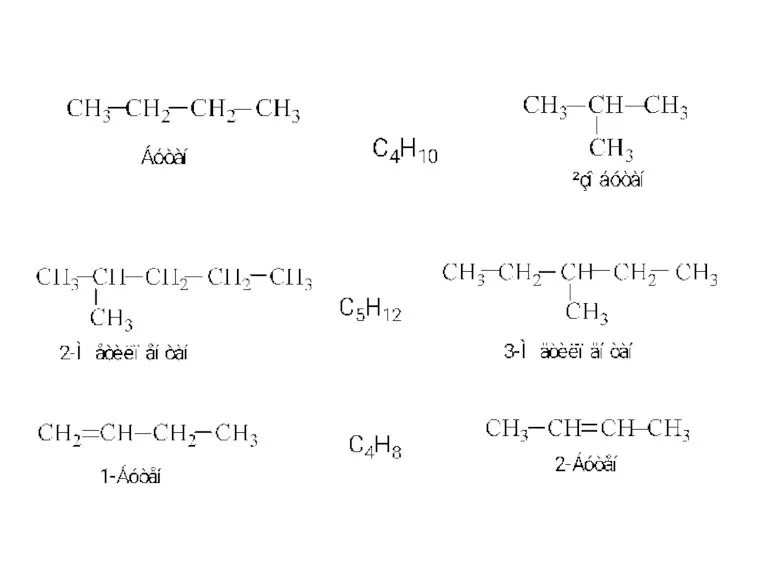 Структурна ізомерія
Структурна ізомерія Введение. Предмет и содержание фармацевтической химии, её связи с другими науками
Введение. Предмет и содержание фармацевтической химии, её связи с другими науками Менделеевские уроки. День науки
Менделеевские уроки. День науки Залежність властивостей полімерів від їхньої будови. Термопластичні й термореактивні полімери
Залежність властивостей полімерів від їхньої будови. Термопластичні й термореактивні полімери Сероводород и его свойства
Сероводород и его свойства Класифікація, будова та номенклатура органічних сполук
Класифікація, будова та номенклатура органічних сполук Непредельные углеводороды. Алкены. Номенклатура алкенов
Непредельные углеводороды. Алкены. Номенклатура алкенов