Содержание
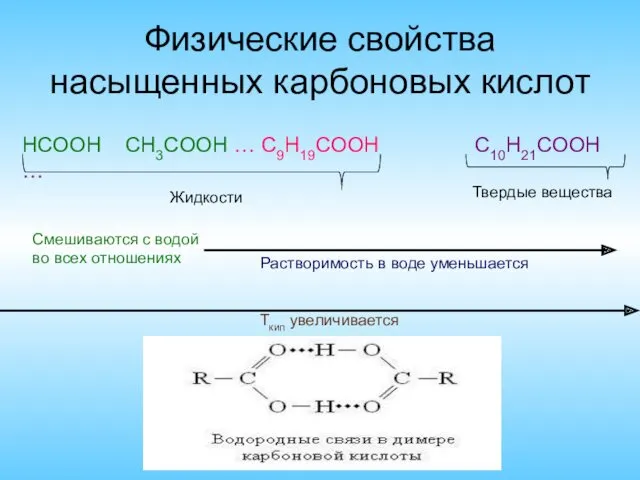
- 2. Физические свойства насыщенных карбоновых кислот HCOOH CH3COOH … C9H19COOH C10H21COOH … Жидкости Твердые вещества Смешиваются с
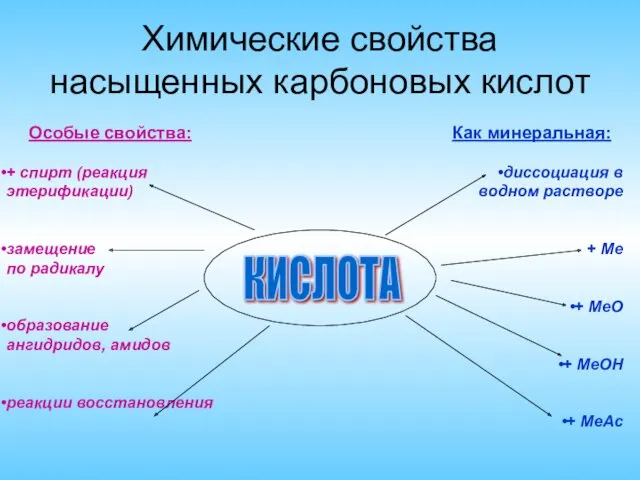
- 3. Химические свойства насыщенных карбоновых кислот КИСЛОТА Особые свойства: Как минеральная: + спирт (реакция этерификации) замещение по
- 4. Химические свойства карбоновых кислот как минеральных кислот Диссоциация в водном растворе (Слабые электролиты. Окрашивают индикатор) R-COOH
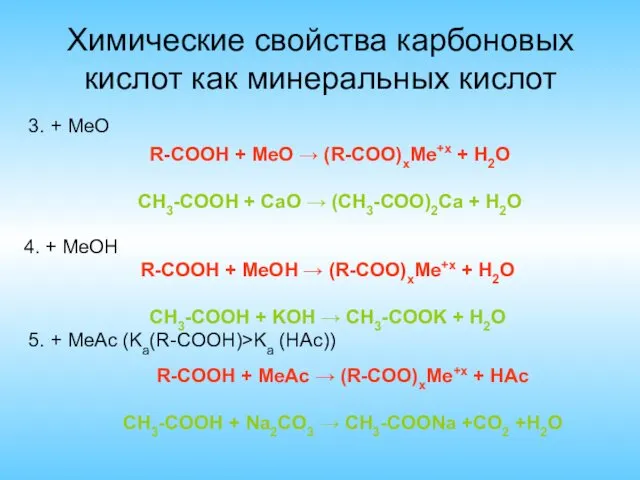
- 5. Химические свойства карбоновых кислот как минеральных кислот 3. + MeO R-COOH + MeO → (R-COO)xMe+x +
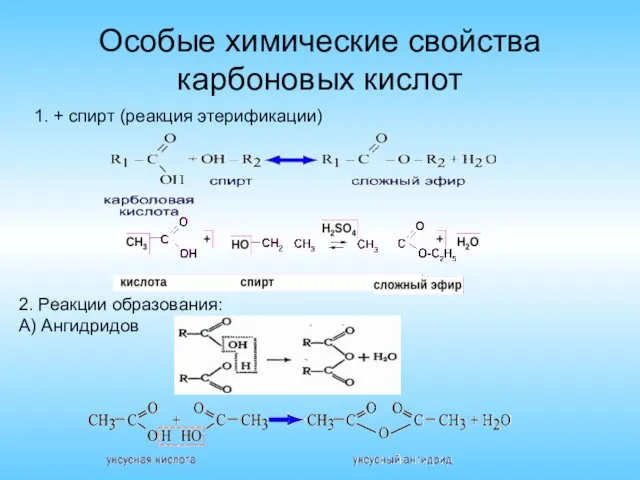
- 6. Особые химические свойства карбоновых кислот 1. + спирт (реакция этерификации) 2. Реакции образования: А) Ангидридов
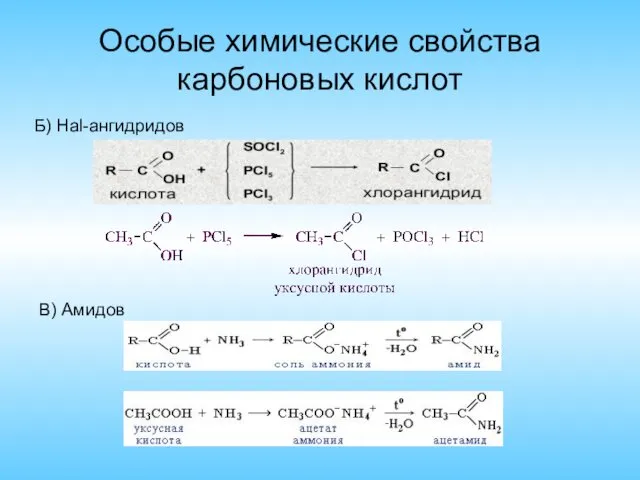
- 7. Особые химические свойства карбоновых кислот В) Амидов Б) Hal-ангидридов
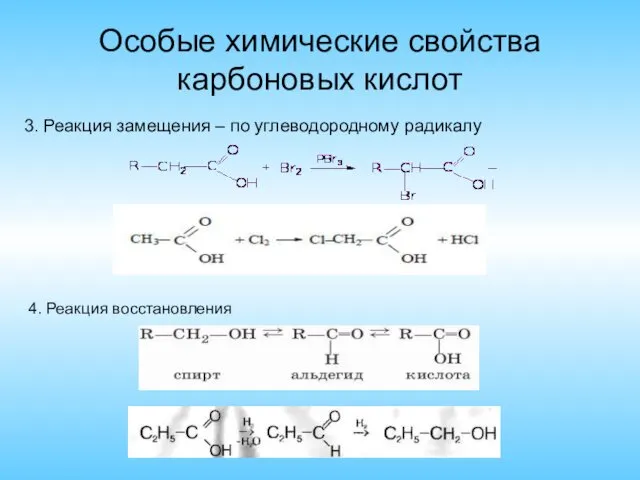
- 8. Особые химические свойства карбоновых кислот 3. Реакция замещения – по углеводородному радикалу 4. Реакция восстановления
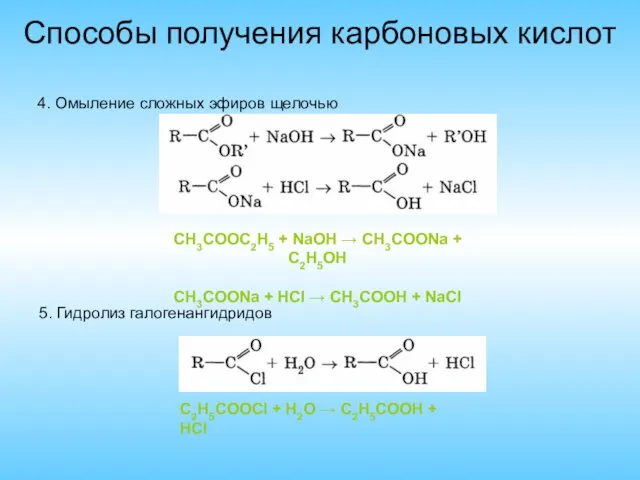
- 9. Способы получения карбоновых кислот 4. Омыление сложных эфиров щелочью CH3COOC2H5 + NaOH → CH3COONa + C2H5OH
- 10. Способы получения карбоновых кислот 1. Окисление первичных спиртов и альдегидов 2. Окисление алканов 2 R-R/ +
- 11. Непредельные карбоновые кислоты
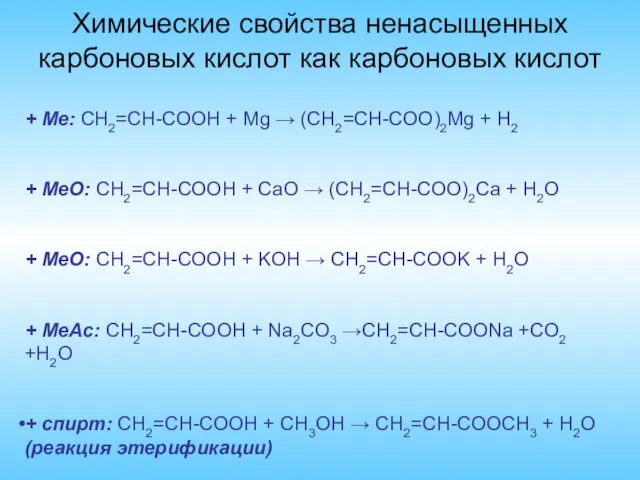
- 12. Химические свойства ненасыщенных карбоновых кислот как карбоновых кислот + Me: CH2=CH-COOH + Mg → (CH2=CH-COO)2Mg +
- 13. Химические свойства ненасыщенных карбоновых кислот как непредельных соединений Реакции присоединения: +H2: CH2=CH-COOH + H2→ CH3-CH2-COOH +
- 15. Скачать презентацию




 Техники ювелирного дела. Введение в предмет. Общие сведения
Техники ювелирного дела. Введение в предмет. Общие сведения Современные проблемы молекулярной биологии
Современные проблемы молекулярной биологии Цикл трикарбоновых кислот (Ц.Кребса). Подсчёт суммарного энергетического эффекта аэробного окисления глюкозы
Цикл трикарбоновых кислот (Ц.Кребса). Подсчёт суммарного энергетического эффекта аэробного окисления глюкозы Речовини. Молекули. Атоми
Речовини. Молекули. Атоми Процесс в химическом реакторе
Процесс в химическом реакторе 20231104_prezentatsiya_teoriya_elektroliticheskoy_dissotsiatsii
20231104_prezentatsiya_teoriya_elektroliticheskoy_dissotsiatsii Каталитический риформинг
Каталитический риформинг Купрум. Знаходження в періодичній системі
Купрум. Знаходження в періодичній системі Непредельные углеводороды. Алкены
Непредельные углеводороды. Алкены Массовая доля вещества в растворе
Массовая доля вещества в растворе Анионы. Группы анионов
Анионы. Группы анионов Углерод и его свойства. 9 класс
Углерод и его свойства. 9 класс Физико-химия полимеров и их растворов
Физико-химия полимеров и их растворов Химический состав клетки
Химический состав клетки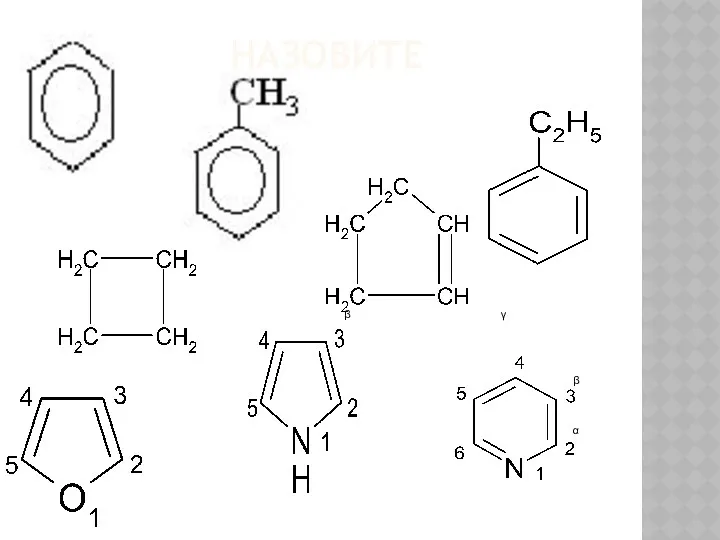 Общие сведения о гетероциклах
Общие сведения о гетероциклах Побочная подгруппа. 8 группы
Побочная подгруппа. 8 группы Проект узла регенерации растворителя уксусной кислоты производства терефталевой кислоты
Проект узла регенерации растворителя уксусной кислоты производства терефталевой кислоты Лекция 5. Нуклеофильное замещение при насыщенном атоме углерода
Лекция 5. Нуклеофильное замещение при насыщенном атоме углерода Пниктогены - элеметны VA группы
Пниктогены - элеметны VA группы Неметаллы: общая характеристика. 9 класс
Неметаллы: общая характеристика. 9 класс Полиэтилен
Полиэтилен Химическая посуда и лабораторное оборудование
Химическая посуда и лабораторное оборудование Кислоты. Состав кислот
Кислоты. Состав кислот Спектрофометрия
Спектрофометрия Углерод и его свойства
Углерод и его свойства d997-13229e5e
d997-13229e5e Теория электролитической диссоциации
Теория электролитической диссоциации Реакции ионного обмена
Реакции ионного обмена