Слайд 2

СОДЕРЖАНИЕ
1.Определение
2.Номенклатура алкенов
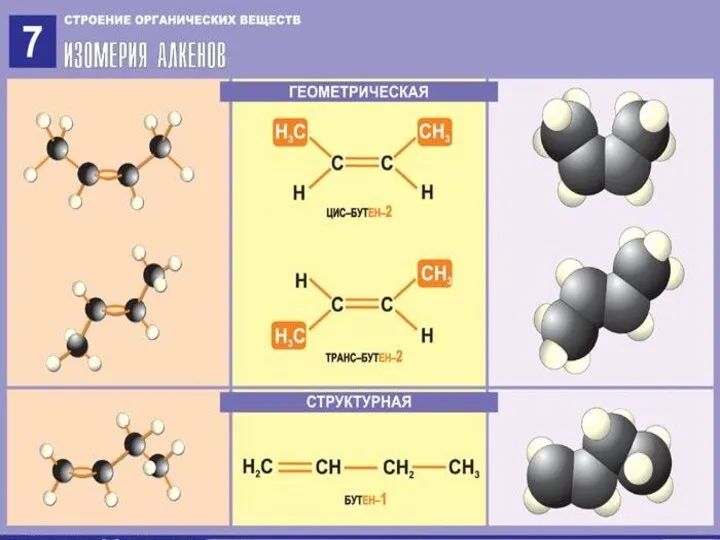
3.Изомерия алкенов
4.Строение алкенов
5.Получение алкенов
6.Физические свойства
7.Химические свойства
8.Применение алкенов
Слайд 3

ОПРЕДЕЛЕНИЕ
Алкены – непредельные углеводороды, в молекулах которых между атомами углерода
имеется одна двойная связь.
Общая формула: СnH2n , где n ≥2
Слайд 4
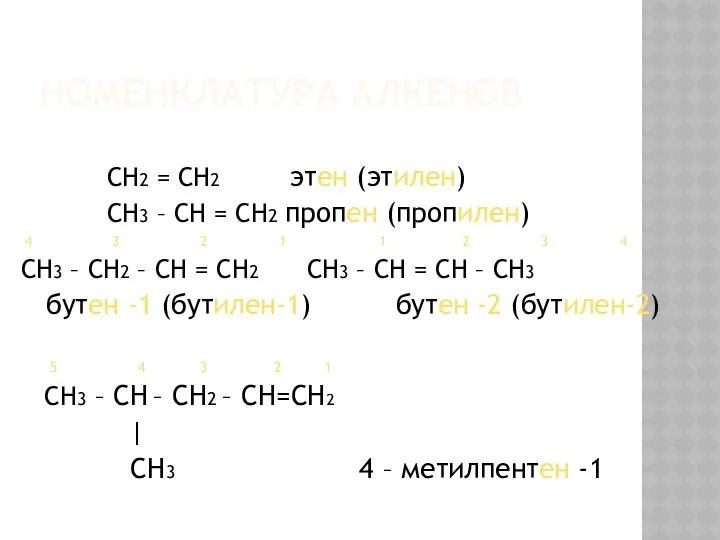
НОМЕНКЛАТУРА АЛКЕНОВ
СН2 = СН2 этен (этилен)
СН3 – СН =
СН2 пропен (пропилен)
4 3 2 1 1 2 3 4
СН3 – СН2 – СН = СН2 СН3 – СН = СН – СН3
бутен -1 (бутилен-1) бутен -2 (бутилен-2)
5 4 3 2 1
СН3 – СН – CH2 – CH=CH2
|
CH3 4 – метилпентен -1
Слайд 5
Слайд 6
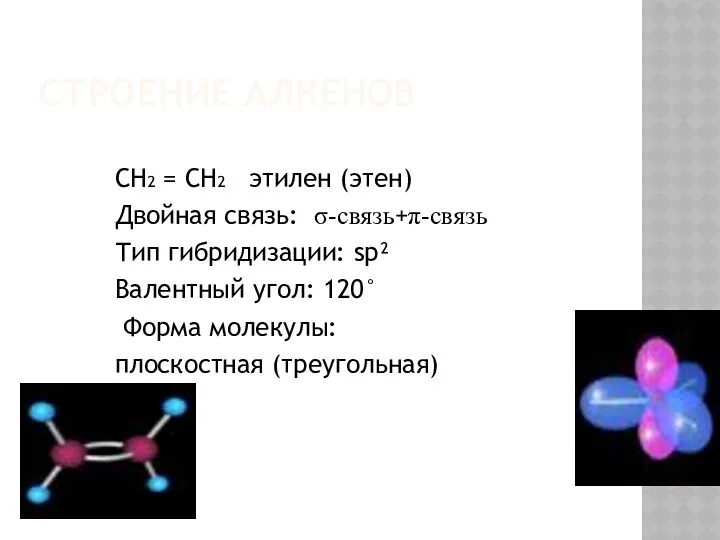
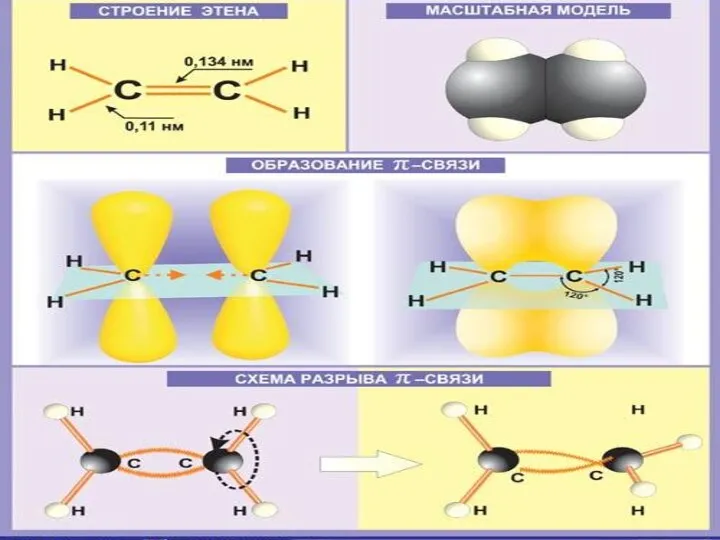
СТРОЕНИЕ АЛКЕНОВ
СН2 = СН2 этилен (этен)
Двойная связь: σ-связь+π-связь
Тип гибридизации: sp²
Валентный
угол: 120°
Форма молекулы:
плоскостная (треугольная)
Слайд 7
Слайд 8
ПОЛУЧЕНИЕ АЛКЕНОВ
1.Крекинг нефтепродуктов:
СН3 –СН2 –СН2 –СН3 → СН2 = СН2 +
СН3 – СН3
2.Дегидрирование алканов:
Pt
СН3 – СН3 → СН2 = СН2 + Н2
Слайд 9
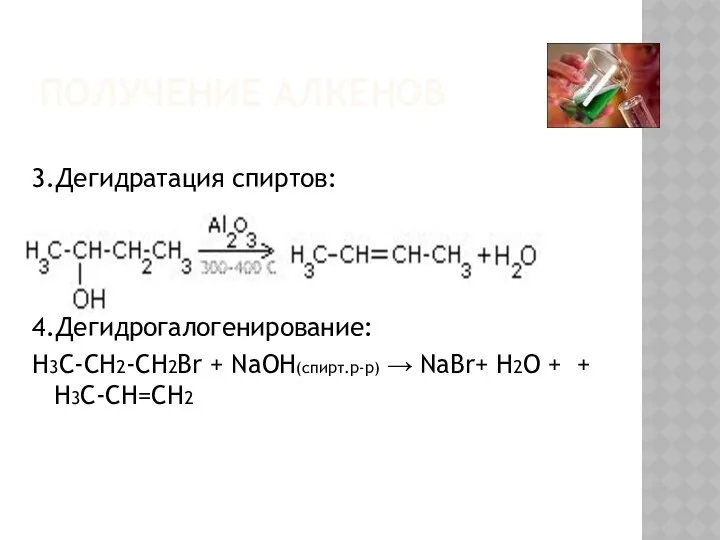
ПОЛУЧЕНИЕ АЛКЕНОВ
3.Дегидратация спиртов:
4.Дегидрогалогенирование:
H3C-CH2-CH2Br + NaOH(спирт.р-р) → NaBr+ H2O + + H3C-CH=CH2
Слайд 10
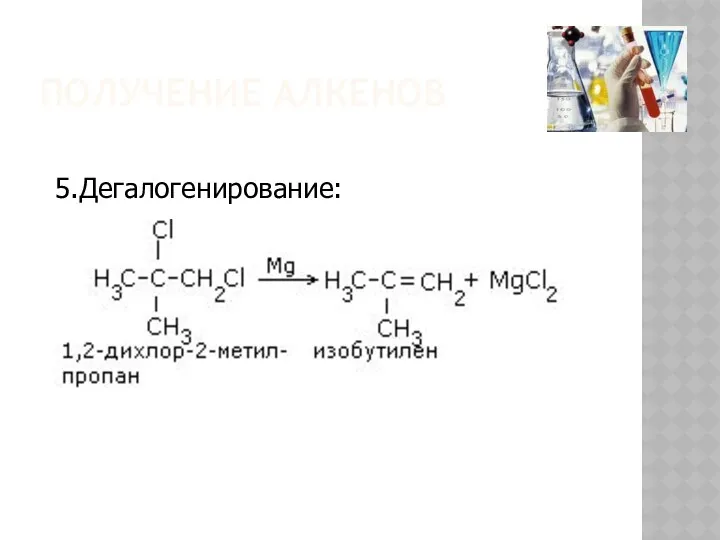
ПОЛУЧЕНИЕ АЛКЕНОВ
5.Дегалогенирование:
Слайд 11
ФИЗИЧЕСКИЕ СВОЙСТВА
Этен,пропен, бутен – газы
С5Н10 – С16Н32 - жидкости
Высшие
алкены – тв.вещества
Слайд 12

ХИМИЧЕСКИЕ СВОЙСТВА
I.Реакции присоединения:
1.Гидрирование :
CH2=CH-CH3+Н2 → CH3-CH2-CH3
2.Галогенирование:
CH2=CH-CH3+Cl2 → CH2Cl-CHCl-CH3
3.Гидрогалогенирование:
CH2=CH-CH3+НCl
→ CH3-CHCl-CH3
Слайд 13
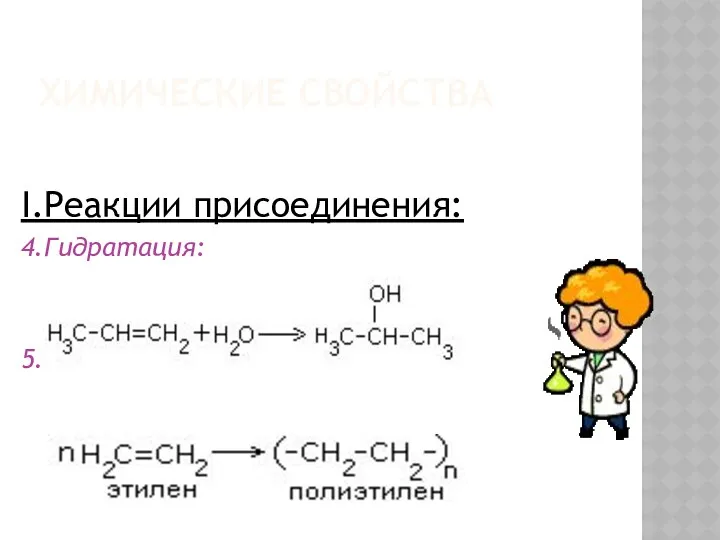
ХИМИЧЕСКИЕ СВОЙСТВА
I.Реакции присоединения:
4.Гидратация:
5.Полимеризация:
Слайд 14

ХИМИЧЕСКИЕ СВОЙСТВА
II.Реакции окисления:
1.Полное окисление (горение):
С2Н4 + 3О2 → 2СО2 +
2Н2О
2.Неполное окисление:
3С2Н4 + 2KMnO4 +4Н2О →3HOCH2-CH2OH +
+2MnO2 + 2KOH













 Reactors for catalytic alkylation
Reactors for catalytic alkylation Химическая коррозия
Химическая коррозия Лекции по курсу конструкционные и биоматериалы
Лекции по курсу конструкционные и биоматериалы Окисление перманганатом и бихроматом калияорганических соединений. Уровень ЕГЭ
Окисление перманганатом и бихроматом калияорганических соединений. Уровень ЕГЭ Соли аммония
Соли аммония ВКР: Изучение золей на основе железа и марганца, полученных методом химической конденсации
ВКР: Изучение золей на основе железа и марганца, полученных методом химической конденсации Теория химического строения органических соединений
Теория химического строения органических соединений Процессы и технологическая схема производства сегодня. АО Газпромнефть-ОНПЗ
Процессы и технологическая схема производства сегодня. АО Газпромнефть-ОНПЗ Теория электрической диссоциации
Теория электрической диссоциации Строение алканов. Физические и химические свойства алканов. Получение алканов
Строение алканов. Физические и химические свойства алканов. Получение алканов Общая характеристика неметаллов
Общая характеристика неметаллов Химическая посуда и лабораторное оборудование
Химическая посуда и лабораторное оборудование Задачи на вывод формулы органических веществ
Задачи на вывод формулы органических веществ Классификация моторных масел
Классификация моторных масел Отчет о прохождении производственно-технологической практики
Отчет о прохождении производственно-технологической практики Основы химической термодинамики
Основы химической термодинамики General characteristics of halogens. Halogen compounds
General characteristics of halogens. Halogen compounds Цинк. Месторождения. Применение
Цинк. Месторождения. Применение Хлороводород и соляная кислота
Хлороводород и соляная кислота Пластмассы. Связующие вещества
Пластмассы. Связующие вещества Алмазы. Бриллианты
Алмазы. Бриллианты Химиялық реакциялар. Амфотерлі негіздер
Химиялық реакциялар. Амфотерлі негіздер Жиры
Жиры Топливо и топливосжигающие устройства
Топливо и топливосжигающие устройства Генетическая связь между классами неорганических соединений
Генетическая связь между классами неорганических соединений IV группа главная подгруппа
IV группа главная подгруппа Сероводород. Сульфиды
Сероводород. Сульфиды Почему мыло пенится
Почему мыло пенится