Слайд 2

Требования, предъявляемые к кислотно-основным индикаторам
1. Индикатор должен быть чувствительным, чтобы расход
индикатора был как можно меньше
2. Равновесие между двумя формами должно устанавливаться быстро
3. Обе формы или одна из форм должны быть интенсивно окрашены
4. Интервал перехода окраски индикатора не должен быть большим
Слайд 3

Теории кислотно-основных индикаторов
Ионная теория
Хромофорная теория
Ионно-хромофорная теория
Слайд 4

Ионная теория: кислотно-основные индикаторы меняют свой цвет при изменении концентра-ции ионов
водорода в растворе, т.е. при изменении рН среды.
HInd → H+ + Ind–
кислая основная
красная желтая
Слайд 5

Недостатки:
1. Не объясняет природы наличия и изменения окраски индикаторов
2. Не связывает
окраску индикаторов с их строением
3. На переход окраски требуется какое время, в то время как ионные реакции протекают быстро
Слайд 6

Хромофорная теория: изменение окраски индикатора обусловлено обратимой перегруппировкой атомов в молекуле,
в результате которой появляются или исчезают группы, обуславливающие цвет раствора
Хромофорные группы: –N=N–, =C=S, –N=O и др
Ауксохромные группы: –NH2, –OH, –OCH3 и др.
Слайд 7
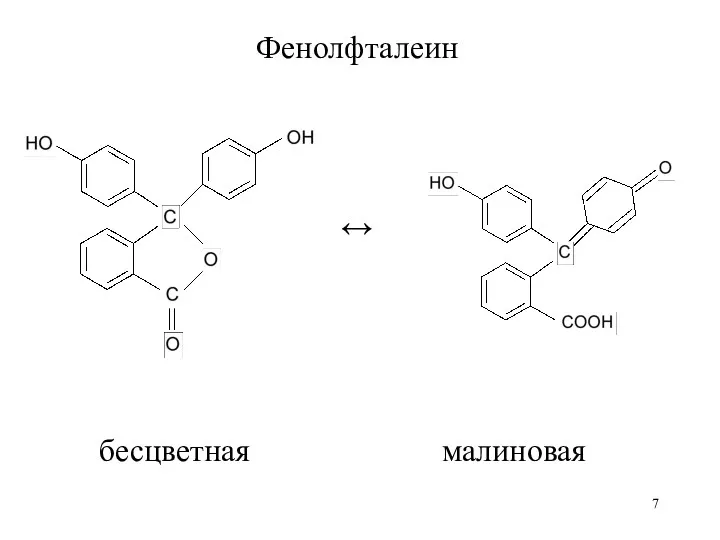
Фенолфталеин
↔
бесцветная малиновая
Слайд 8
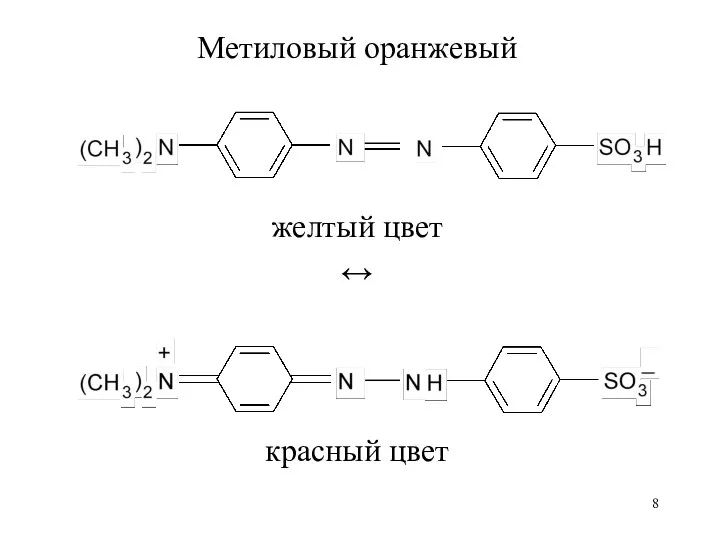
Метиловый оранжевый
желтый цвет
↔
красный цвет
Слайд 9

На таутомерные превращения требуется некоторое время, поэтому окраска индикатора изменяется не
мгновенно, очевидна взаимосвязь между окраской и строением молекул
Не объясняет, почему изменение происходит при изменении рН раствора
Слайд 10

Ионно-хромофорная теория индикаторов: отщепление протона или гидроксид-иона привод к перегруппировке атомов
в молекуле, что приводит к изменению цвета индикатора
Объясняет:
Изменение цвета раствора при изменении рН
Изменение окраски во времени
Связывает изменение окраски с его структурой
Слайд 11
![HInd → H+ + Ind– кислая основная красная желтая [H+] · [Ind–] KInd = —————— [HInd]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/345039/slide-10.jpg)
HInd → H+ + Ind–
кислая основная
красная желтая
[H+]
· [Ind–]
KInd = ——————
[HInd]
Слайд 12
![[HInd] [H+] = KInd · ——— [Ind–] [Ind–] pH =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/345039/slide-11.jpg)
[HInd]
[H+] = KInd · ———
[Ind–]
[Ind–]
pH = pKInd + lg
———
[HInd]
Соотношение [Ind–]/[HInd] зависит от рН р-ра
Человеческий глаз замечает изменение окраски при 10-кратном избытке одной из форм
Слайд 13
![[Ind–]/[HInd] ≥ 10 – наблюдается окраска основной формы [Ind–] (желтая)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/345039/slide-12.jpg)
[Ind–]/[HInd] ≥ 10 – наблюдается окраска
основной формы [Ind–] (желтая)
pH
= pKInd + 1
[Ind–]/[HInd] ≤ 10 – наблюдается окраска
кислой формы [HInd] (красная)
pH = pKInd – 1
Слайд 14

Интервал перехода окраски индикатора:
ΔpH = pKInd ± 1
ΔpH не всегда охватывает
две единицы рН, т.к. соотношение концентраций двух форм, необ-ходимое для наблюдения изменения окраски индикатора, [Ind–]/[HInd] не всегда равно 10 и зависит от природы индикатора
м/о ΔpH = 3,2 – 4,4 красная – желтая
м/к ΔpH = 4,2 – 6,2 красная – желтая
ф/ф ΔpH = 8,2 – 10,0 бесцветная – малиновая
Слайд 15

Индикаторы часто характеризуют не интервалом перехода окраски индикатора, а показателем титрования
рТ
рТ – это значение рН, при котором наиболее резко происходит изменение окраски индикатора.
м/о ΔpH = 3,2 – 4,4 рТ = 4,0
м/к ΔpH = 4,2 – 6,2 рТ = 5,5
ф/ф ΔpH = 8,2 – 10,0 рТ = 9,0
Слайд 16

Классификация кислотно-основных индикаторов:
1. По строению:
- трифенилметановые индикаторы (ф/ф, ф/к)
- нитроиндикаторы (о-,
м-, п-нитрофенолы)
- других структурных типов (лакмус, индофенол, нейтральный красный и др.)
2. По способу применения:
- внутренние (ф/ф, ф/к, м/о, т/ф и др.)
- внешние ( лакмусовая бумага /красная, нейтральная, синяя/, куркумовая бумага, ф/ф бумага)
Слайд 17

3. По составу:
- индивидуальные:
(фенолфталеин, метиловый оранжевый и др.)
смешанные (более резкое
изменение окраски):
* смесь двух индикаторов
(фенолфталеин + тимолфталеин)
* смесь индикатора с красителем
(фенолфталеин + метиленовый синий)
4. По цветности: одноцветные (ф/ф), двухцвет-ные (м/о)
Слайд 18

Кривые кислотно-основного титрования
Отображают графическую зависимость рН титруемого раствора от объема прибавленного
титранта или от степени оттитрованности
Анализ кривой титрования позволяет подобрать оптимальные условия титрования (концентрация реагентов, индикатор)
Слайд 19

Расчет, построение и анализ кривой титрования сильной кислоты сильным основанием
HCl +
NaOH → NaCl + H2O
C(HCl) = C(NaOH) = 0,1 M
Изменением объема пренебрегаем
до ТЭ : рН = –lgCк-ты
ТЭ: рН = 7
после ТЭ: рН = 14 + lgСосн
Слайд 20

Доб Отт. Ост-к Конц рН рН
щ. к. % к. % к-ты
р-ра С=0,1М
0 0 100 С –lgC –lg10–1=1
90 90 10 10–1С –lg10–1С –lg10–2=2
99 99 1 10–2С –lg10–2С –lg10–3=3
99,9 99,9 0,1 10–3С –lg10–3С –lg10–4=4
100 100 — — — 7
изб-к конц.
щ.% щ.
100,1 — 0,1 10–3С 14+lg10–3С 14+lg10–4=10
101 — 1 10–2С 14+lg10–2С 14+lg10–3=11
110 — 10 10–1С 14+lg10–1С 14+lg10–2=12
Слайд 21
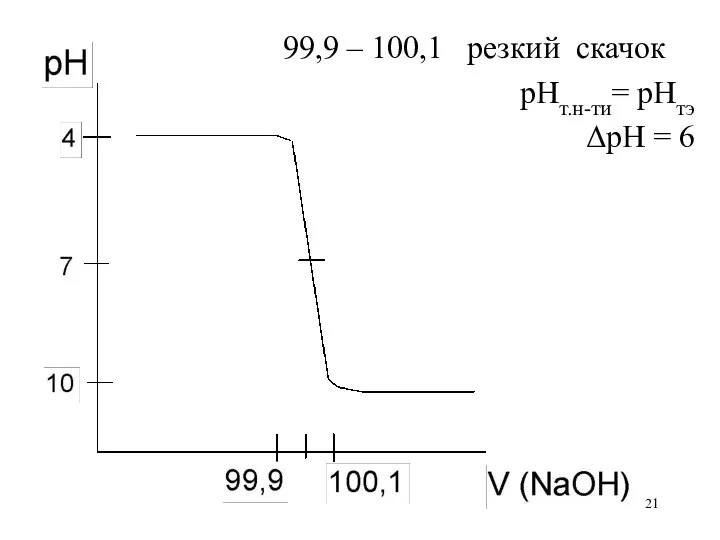
99,9 – 100,1 резкий скачок
рНт.н-ти= рНтэ
ΔрН = 6
Слайд 22

От чего зависит скачок титрования?
ΔpH = рН100,1 – рН99,9 = 14+lg10–3С
– (–lg10–3С) =
= 14 – 3 + lgC – 3 + lgC = 8 + 2lgC
Скачок зависит от:
- Температуры (с увеличением tо рКводы
уменьшается, скачок уменьшается)
- Концентрации (с уменьшением концентрации
скачок уменьшается)
Слайд 23

Как зависит скачок титрования от концентрации?
ΔpH = 8 + 2lgC
С
моль/л ΔpH
1 8
0,1 8 – 2 = 6
0,01 8 – 4 = 4
0,001 8 – 6 = 2
0,0001 8 – 8 = 0
Слайд 24
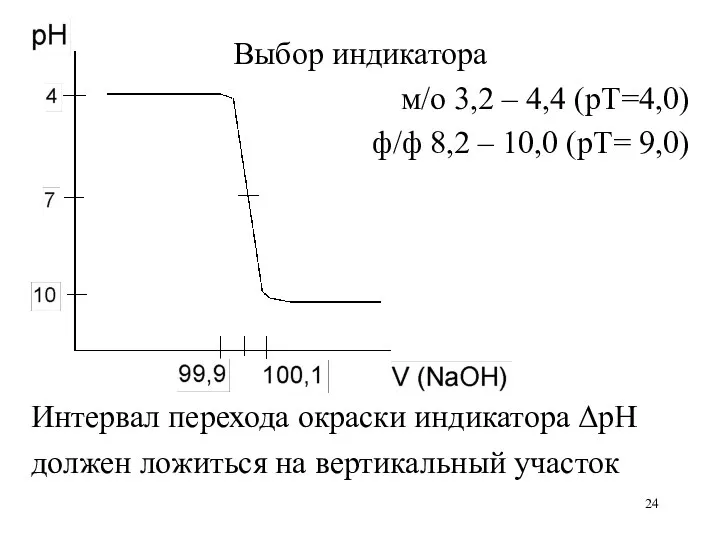
Выбор индикатора
м/о 3,2 – 4,4 (рТ=4,0)
ф/ф 8,2 – 10,0 (рТ=
9,0)
Интервал перехода окраски индикатора ΔpH
должен ложиться на вертикальный участок
Слайд 25

Расчет, построение и анализ кривой титрования слабой кислоты сильным основанием
CH3COOH +
NaOH → CH3COONa + H2O
C(HA) = C(BOH) = 0,1 M
pK(CH3COOH) = 4,76
Изменением объема пренебрегаем
В начальный момент: слабая кислота
рН = ½ pKк-ты – ½ lgCк-ты
Слайд 26

До ТЭ: слабая кислота и ее соль
Ссоли
рН = pKк-ты +
lg———
Ск-ты
ТЭ: соль сильного основания и слабой кислоты
рН = 7 + ½ pKк-ты + ½ lgCсоли
За ТЭ: избыток щелочи и соль (гидролиз
подавляется)
рН = 14 + lgСосн
Слайд 27

Доб. Отт-но Конц. Конц. Ссоли рН рН
——
щел. к-ты,% к-ты соли
Ск-ты р-ра С=0,1
0 — С — — ½pKк– ½lgCк 2,88
90 90 10–1С 9·10–1С 9≈10 рКк+lg10 5,75
99 99 10–2С 99·10–2С 99≈102 рКк+lg102 6,75
99,9 99,9 10–3С 999·10–3С 999≈103 рКк+lg103 7,75
100 100 — С — 7+½pKк+ ½lgCс 8,88
изб-к конц.
щ.% щ.
100,1 — 0,1 10–3С — 14+lg10–3С 10
101 — 1 10–2С — 14+lg10–2С 11
110 — 10 10–1С — 14+lg10–1С 12
Слайд 28
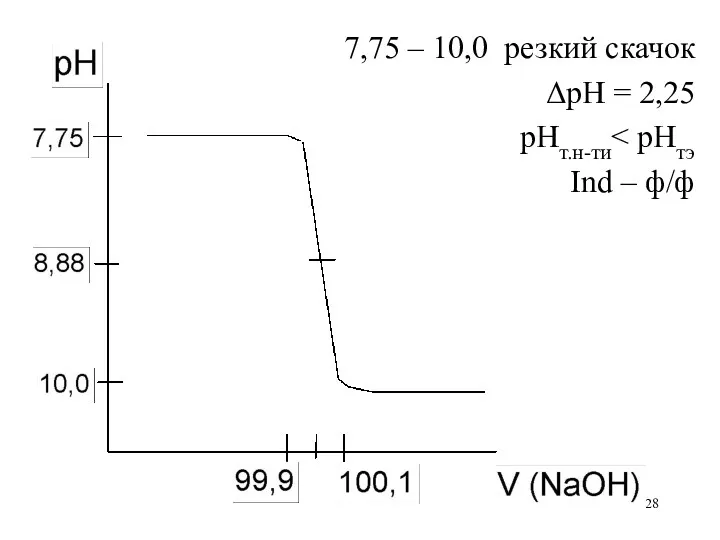
7,75 – 10,0 резкий скачок
ΔрН = 2,25
рНт.н-ти< рНтэ
Ind – ф/ф
Слайд 29

От чего зависит скачок титрования?
ΔpH=рН100,1– рН99,9=14+lg10–3С – (рКк + lg103) =
= 14 – 3 + lgC – рКк– 3 = 8 + lgC – рКк
Скачок зависит от:
- Температуры (с увеличением tо рКводы
уменьшается, скачок уменьшается)
- Концентрации (с уменьшением концентрации
скачок уменьшается)
- Природы кислоты (чем слабее кислота, тем
меньше скачок)
Слайд 30

Как зависит скачок титрования
от силы кислоты?
ΔpH = 8 + lgC
– рКк
С = 0,1 моль/л ΔpH = 7 – рКк
Если рКк ≥ 7 ΔpH = 0 скачка не будет, и
нельзя подобрать индикатор
Слайд 31

Расчет, построение и анализ кривой титрования сильного основания сильной кислотой
NaOH +
HCl → NaCl + H2O
C(NaOH) = C(HCl) = 0,1 M
Изменением объема пренебрегаем
до ТЭ : рН = 14 + lgСосн
ТЭ: рН = 7
после ТЭ: рН = –lgCк-ты
Слайд 32

Доб Отт. Ост-к Конц рН рН
к. щ. % щ. %
щ-чи р-ра С=0,1М
0 0 100 С 14+lgC 13
90 90 10 10–1С 14+lg10–1С 12
99 99 1 10–2С 14+lg10–2С 11
99,9 99,9 0,1 10–3С 14+lg10–3С 10
100 100 — — — 7
изб-к конц.
к.% к.
100,1 — 0,1 10–3С –lg10–3С 4
101 — 1 10–2С –lg10–2С 3
110 — 10 10–1С –lg10–1С 2
Слайд 33
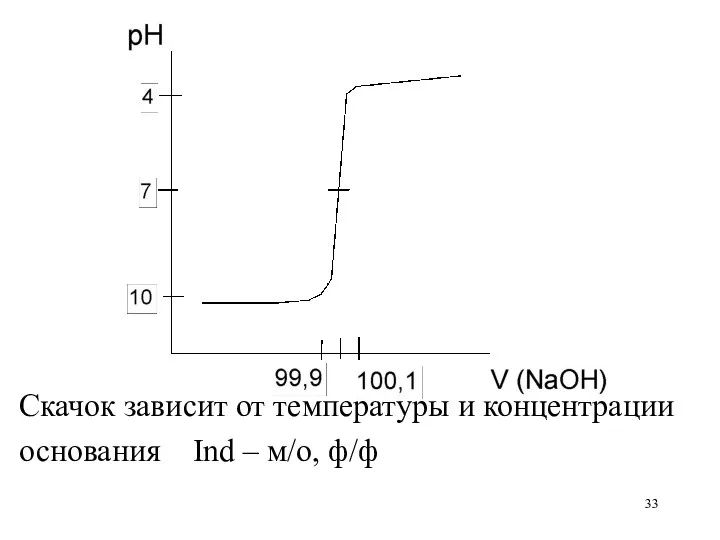
Скачок зависит от температуры и концентрации
основания Ind – м/о, ф/ф
Слайд 34

Расчет, построение и анализ кривой титрования слабого основания сильной кислотой
NH4OH + HCl → NH4Cl + H2O
C(NH4OH) = C(HCl) = 0,1 M рК(NH4OH)=4,75
Изменением объема пренебрегаем
В начальный момент: слабое основание
рН =14 – ½ pKосн + ½ lgCосн
Слайд 35

До ТЭ: слабое основание и его соль
Ссоли
рН =14 – pKосн
– lg———
Сосн
ТЭ: соль сильной кислоты и слабого основания
рН = 7 – ½ pKосн – ½ lgCсоли
За ТЭ: избыток кислоты и соль (гидролиз
подавляется)
рН = – lgСк-ты
Слайд 36

Доб. Отт-но Конц. Конц. Ссоли рН рН
——
К-ты. осн,% осн соли
Сосн р-ра С=0,1
0 — С — — 14–½pKо+½lgCо 12,13
90 90 10–1С 9·10–1С 9≈10 14–рКо–lg10 8,25
99 99 10–2С 99·10–2С 99≈102 14–рКо–lg102 7,25
99,9 99,9 10–3С 999·10–3С 999≈103 14–рКо– lg103 6,25
100 100 — С — 7–½pKо–½lgCс 5,13
изб-к конц.
к.% к.
100,1 — 0,1 10–3С — –lg10–3С 4
101 — 1 10–2С — –lg10–2С 3
110 — 10 10–1С — –lg10–1С 2
Слайд 37
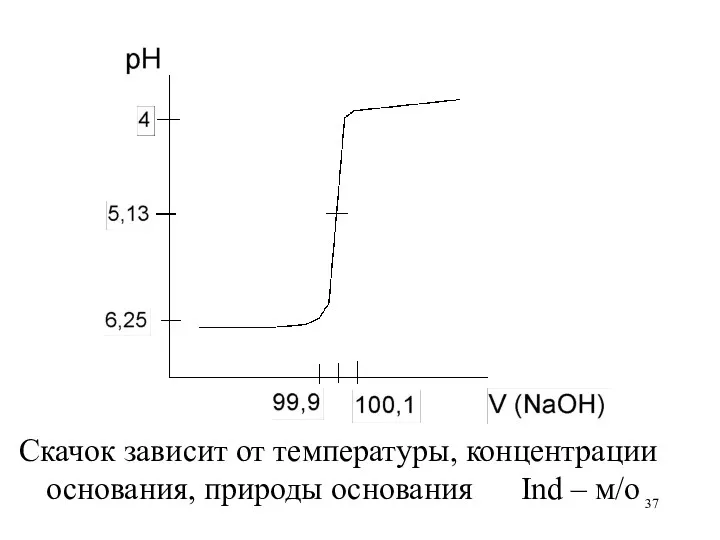
Скачок зависит от температуры, концентрации основания, природы основания Ind – м/о
Слайд 38

Расчетные формулы рН при титровании
слабой двухосновной к-ты сильным основанием
H2SO3 +
2NaOH → Na2SO3 + H2O
Нач: H2SO3 рН = ½ pK1к-ты – ½ lgCк-ты
До 1 ТЭ: H2SO3 + NaHSO3
Ссоли
рН = pK1к-ты + lg———
Ск-ты
1 ТЭ: NaHSO3
pK1к-ты + pK2к-ты
рН = ———————
2
Слайд 39
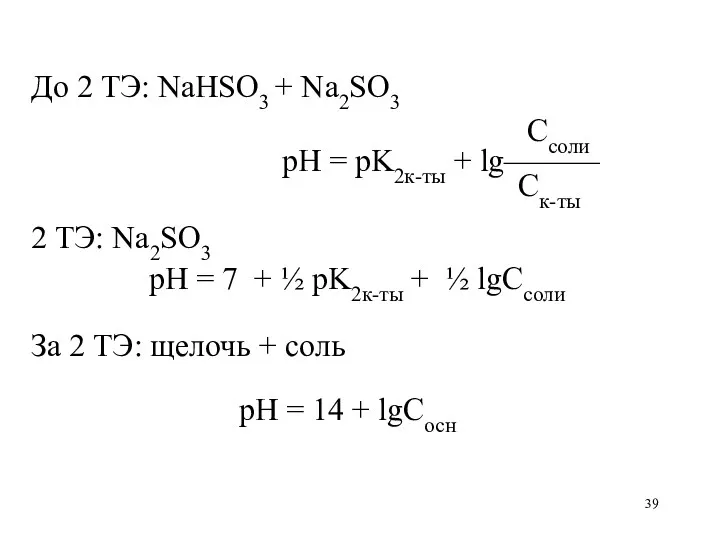
До 2 ТЭ: NaHSO3 + Na2SO3
Ссоли
рН = pK2к-ты +
lg———
Ск-ты
2 ТЭ: Na2SO3
рН = 7 + ½ pK2к-ты + ½ lgCсоли
За 2 ТЭ: щелочь + соль
рН = 14 + lgСосн
Слайд 40

Расчетные формулы рН при титровании соли
слабой двухосновной к-ты сильной кислотой
Na2SO3 +
2HCl → H2SO3 + 2NaCl
Нач: Na2SO3 рН = ½ pK2к-ты – ½ lgCк-ты
До 1 ТЭ: Na2SO3 + NaHSO3
Ссоли
рН = pK2к-ты + lg———
Ск-ты
1 ТЭ: NaHSO3
pK1к-ты + pK2к-ты
рН = ———————
2
Слайд 41
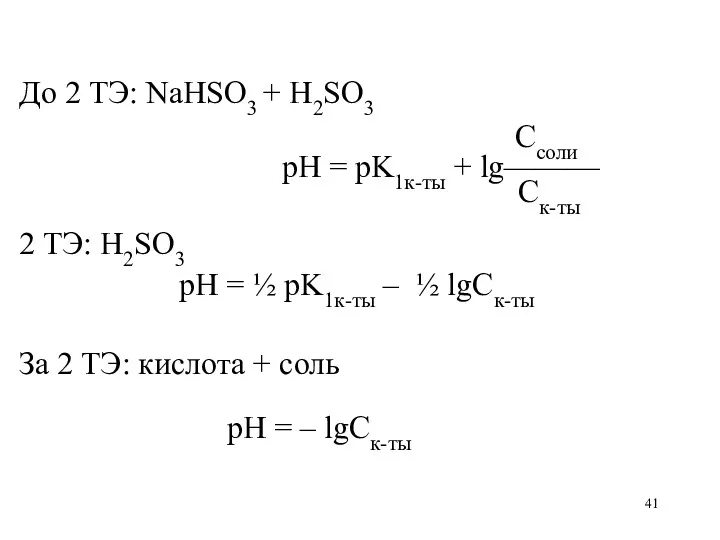
До 2 ТЭ: NaHSO3 + H2SO3
Ссоли
рН = pK1к-ты +
lg———
Ск-ты
2 ТЭ: H2SO3
рН = ½ pK1к-ты – ½ lgCк-ты
За 2 ТЭ: кислота + соль
рН = – lgСк-ты
Слайд 42

Индикаторные ошибки
кислотно-основного титрования
Индикаторные ошибки обусловлены несовпадением рН конца титрования (рТInd) и
рН точки эквивалентности
Слайд 43
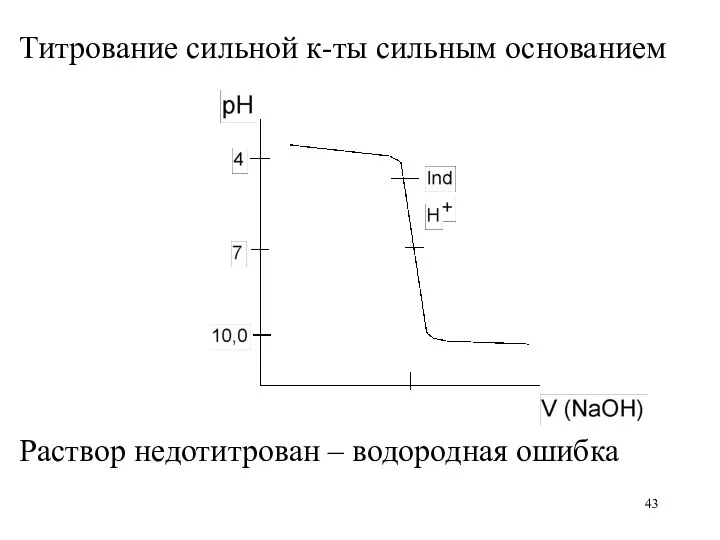
Титрование сильной к-ты сильным основанием
Раствор недотитрован – водородная ошибка
Слайд 44
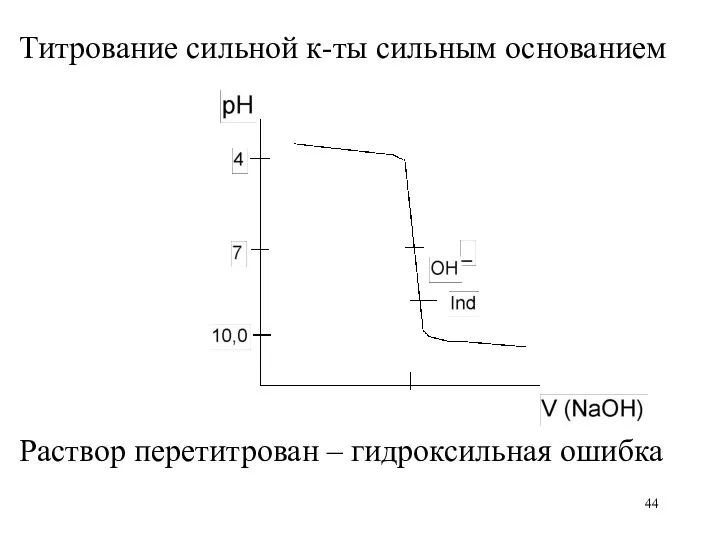
Титрование сильной к-ты сильным основанием
Раствор перетитрован – гидроксильная ошибка
Слайд 45
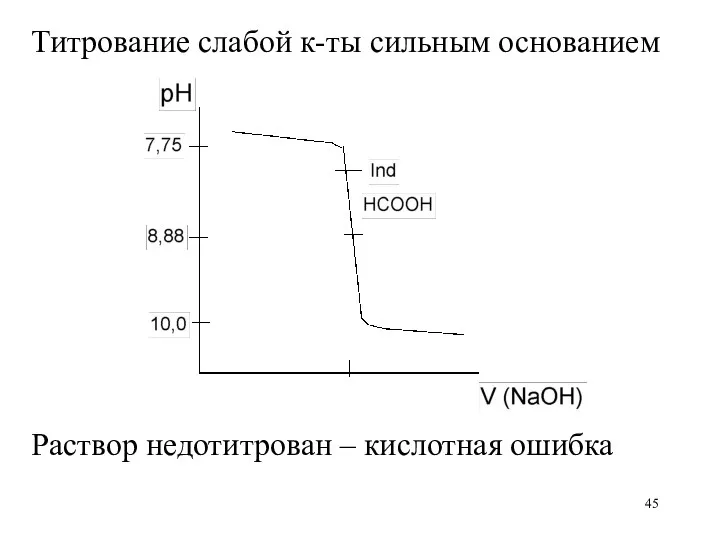
Титрование слабой к-ты сильным основанием
Раствор недотитрован – кислотная ошибка
Слайд 46
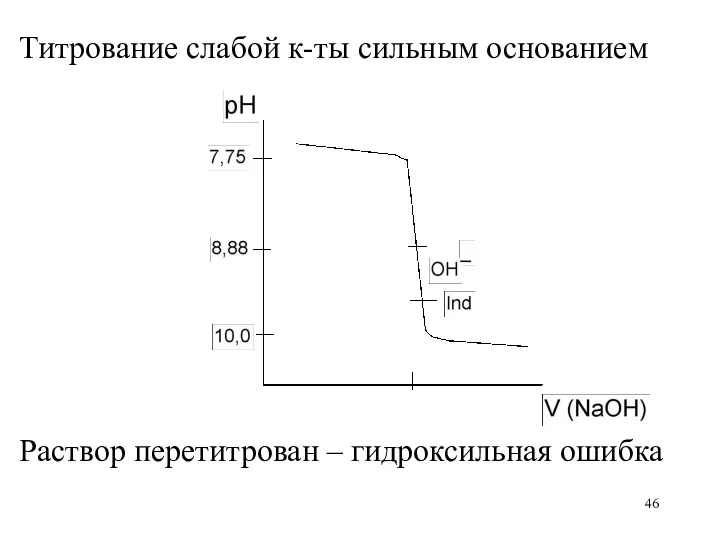
Титрование слабой к-ты сильным основанием
Раствор перетитрован – гидроксильная ошибка
Слайд 47
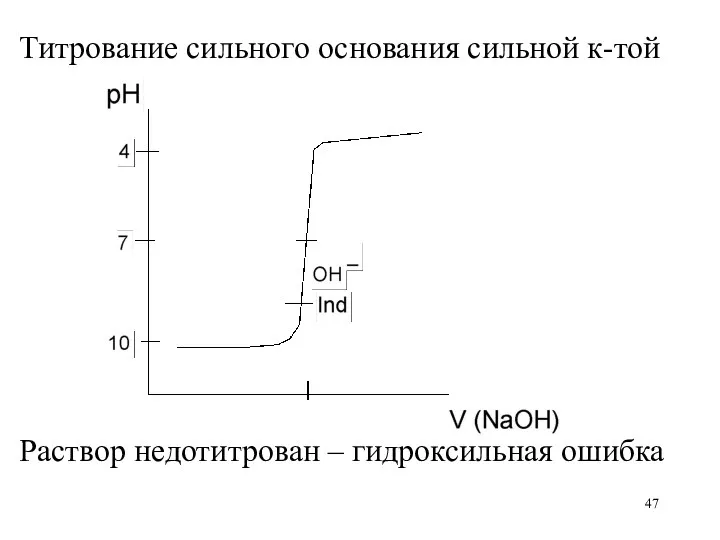
Титрование сильного основания сильной к-той
Раствор недотитрован – гидроксильная ошибка
Слайд 48
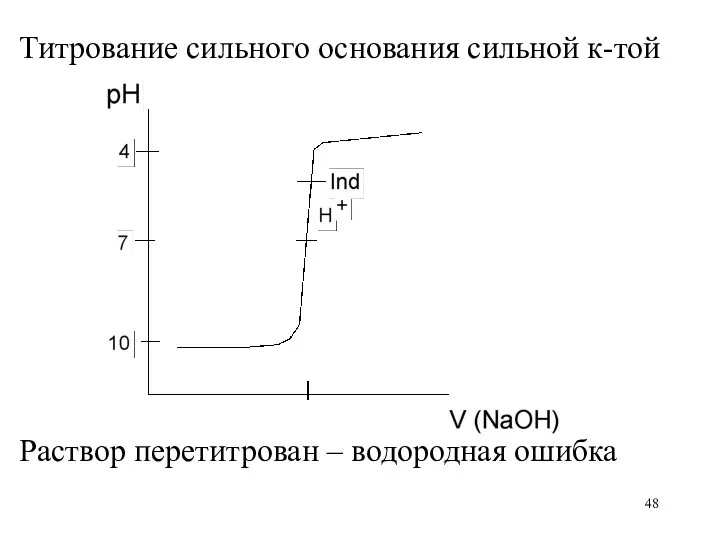
Титрование сильного основания сильной к-той
Раствор перетитрован – водородная ошибка
Слайд 49
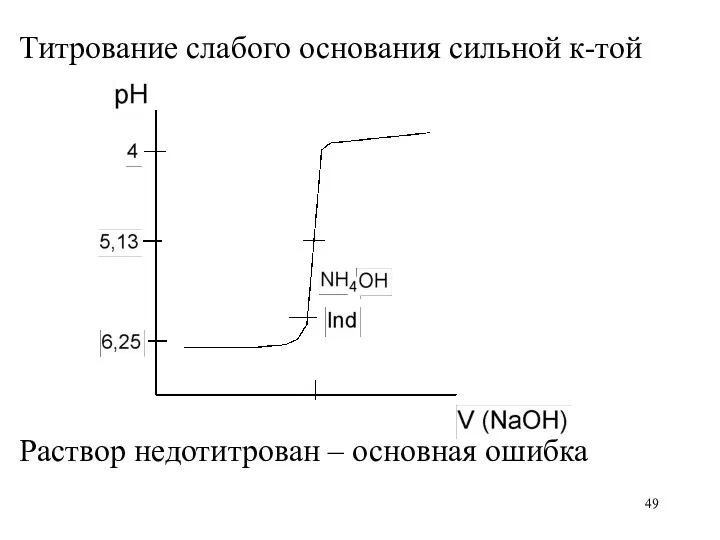
Титрование слабого основания сильной к-той
Раствор недотитрован – основная ошибка
Слайд 50
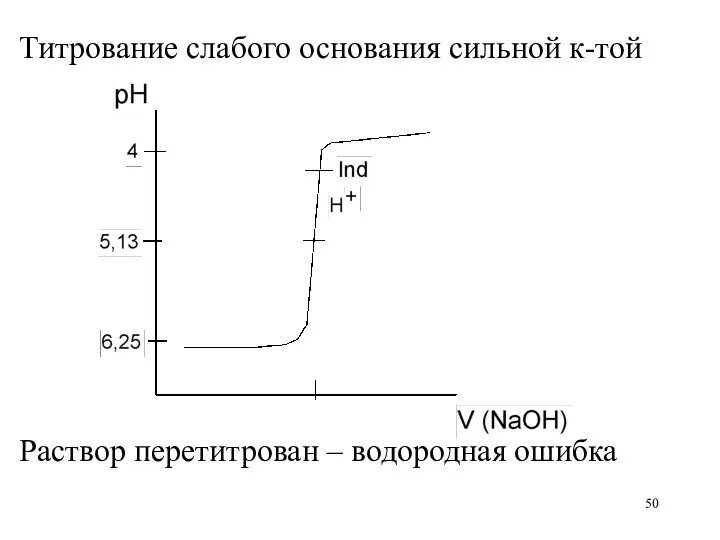
Титрование слабого основания сильной к-той
Раствор перетитрован – водородная ошибка









![HInd → H+ + Ind– кислая основная красная желтая [H+] · [Ind–] KInd = —————— [HInd]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/345039/slide-10.jpg)
![[HInd] [H+] = KInd · ——— [Ind–] [Ind–] pH =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/345039/slide-11.jpg)
![[Ind–]/[HInd] ≥ 10 – наблюдается окраска основной формы [Ind–] (желтая)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/345039/slide-12.jpg)





































 Минерал турмалин
Минерал турмалин Пластмассы: свойства, требования, перспективы развития. Виды конструкций из пластмасс
Пластмассы: свойства, требования, перспективы развития. Виды конструкций из пластмасс Лекарственные средства, относящиеся к производным пиридина : производные никотиновой и изоникотиновой кислоты
Лекарственные средства, относящиеся к производным пиридина : производные никотиновой и изоникотиновой кислоты Искусственные полимеры. 10 класс
Искусственные полимеры. 10 класс Теория химического строения органических соединений
Теория химического строения органических соединений Роль побутової хімії у житті
Роль побутової хімії у житті Методы чтения последовательностей нуклеиновых кислот. Секвенирование геномов древних людей
Методы чтения последовательностей нуклеиновых кислот. Секвенирование геномов древних людей альдегиды, свойства, получение
альдегиды, свойства, получение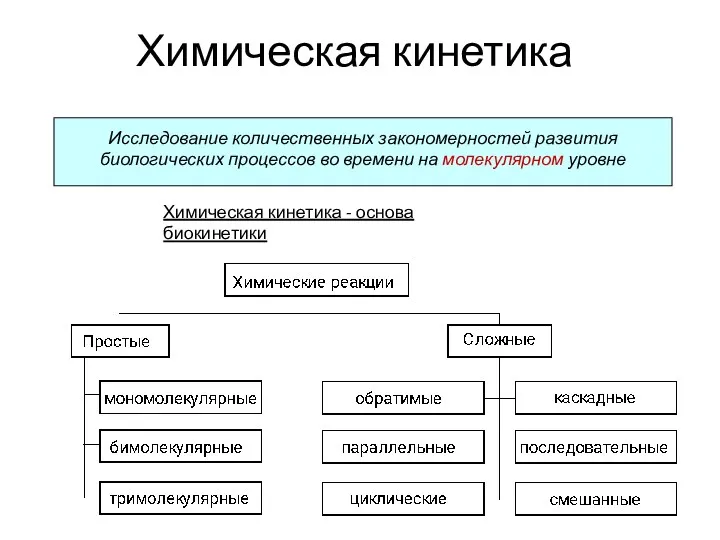 Химическая кинетика
Химическая кинетика Техника безопасности для учащихся в кабинете химии
Техника безопасности для учащихся в кабинете химии Theories of acids and bases. Ionic equilibria in electrolyte solutions. Buffer solutions (topic 3.4)
Theories of acids and bases. Ionic equilibria in electrolyte solutions. Buffer solutions (topic 3.4) Химические и физические свойства воды
Химические и физические свойства воды Окислительно-восстановительные реакции. Готовимся к ЕГЭ
Окислительно-восстановительные реакции. Готовимся к ЕГЭ Ферменты в биотехнологии
Ферменты в биотехнологии Губна помада та ії призначення
Губна помада та ії призначення Анализ двойных диаграмм. Лабораторная работа
Анализ двойных диаграмм. Лабораторная работа Общая характеристика металлов
Общая характеристика металлов Азот и его соединения
Азот и его соединения Обобщение по типам химических реакций
Обобщение по типам химических реакций The production of stable isotopes
The production of stable isotopes Хімічні властивості насичених одноатомних спиртів. Одержання етанолу
Хімічні властивості насичених одноатомних спиртів. Одержання етанолу Protein Chemistry
Protein Chemistry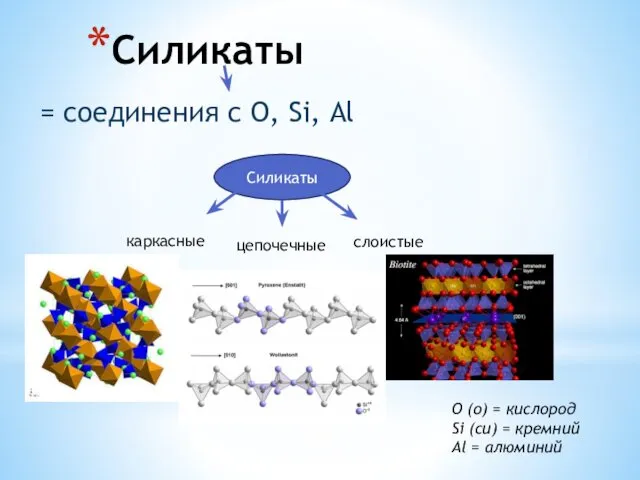 Силикаты. Слюды. Тальк. Фосфаты. Апатит. Крокоит
Силикаты. Слюды. Тальк. Фосфаты. Апатит. Крокоит Хинолин және хинуклидин, 4- жағдайда алмасқан хинолин туындыларының дәрілік заттарын талдау
Хинолин және хинуклидин, 4- жағдайда алмасқан хинолин туындыларының дәрілік заттарын талдау Выращивание кристаллов в домашних условиях
Выращивание кристаллов в домашних условиях Лекция 1 эквивалент 2
Лекция 1 эквивалент 2 Теплові прояви механічної, електричної та хімічної енергії
Теплові прояви механічної, електричної та хімічної енергії Элементы V группы главной подгруппы. Азот. Фосфор. (Лекция 13)
Элементы V группы главной подгруппы. Азот. Фосфор. (Лекция 13)