Лекарственные средства, относящиеся к производным пиридина : производные никотиновой и изоникотиновой кислоты презентация
Содержание
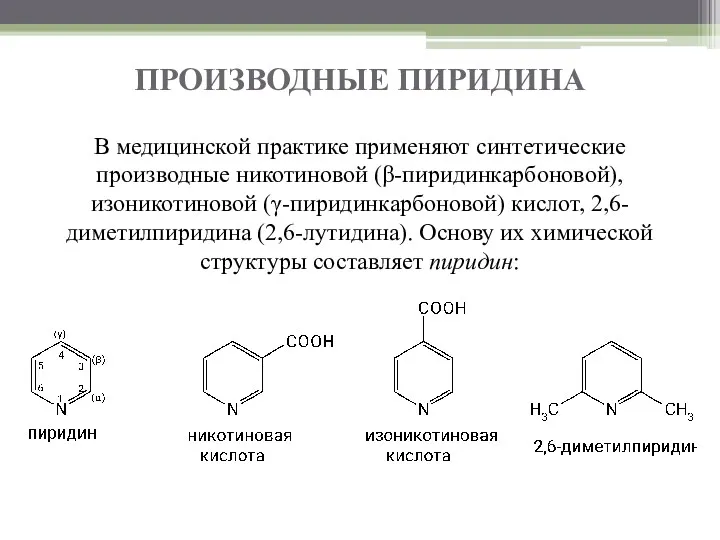
- 2. ПРОИЗВОДНЫЕ ПИРИДИНА В медицинской практике применяют синтетические производные никотиновой (β-пиридинкарбоновой), изоникотиновой (γ-пиридинкарбоновой) кислот, 2,6-диметилпиридина (2,6-лутидина). Основу
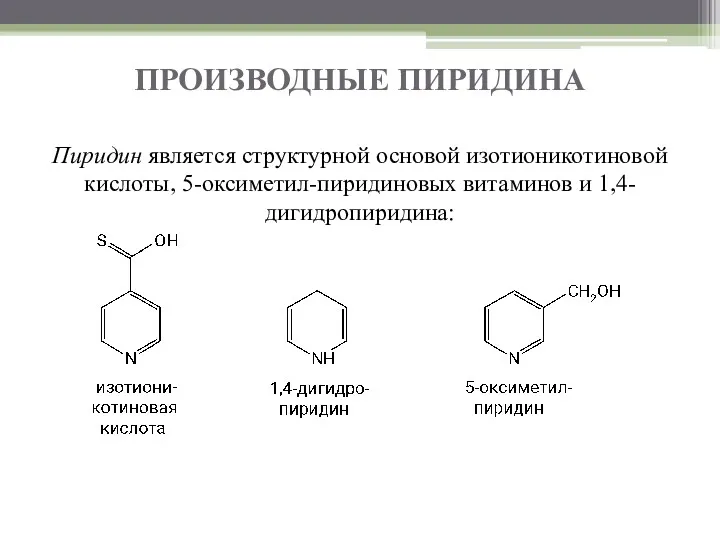
- 3. ПРОИЗВОДНЫЕ ПИРИДИНА Пиридин является структурной основой изотионикотиновой кислоты, 5-оксиметил-пиридиновых витаминов и 1,4-дигидропиридина:
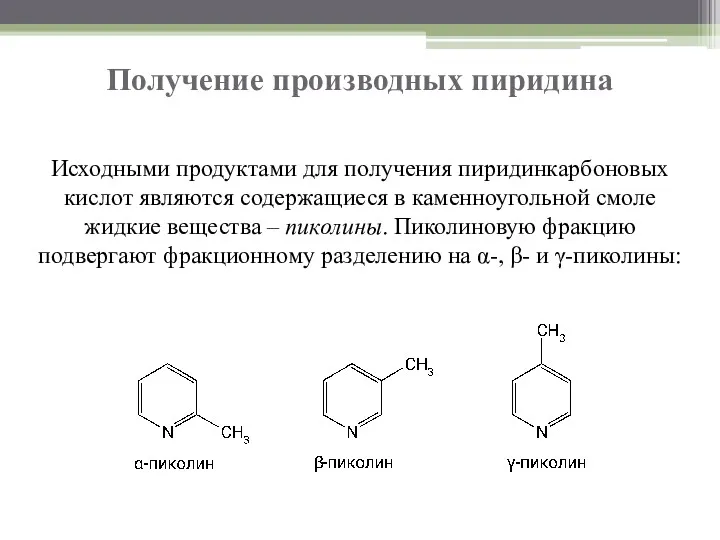
- 4. Получение производных пиридина Исходными продуктами для получения пиридинкарбоновых кислот являются содержащиеся в каменноугольной смоле жидкие вещества
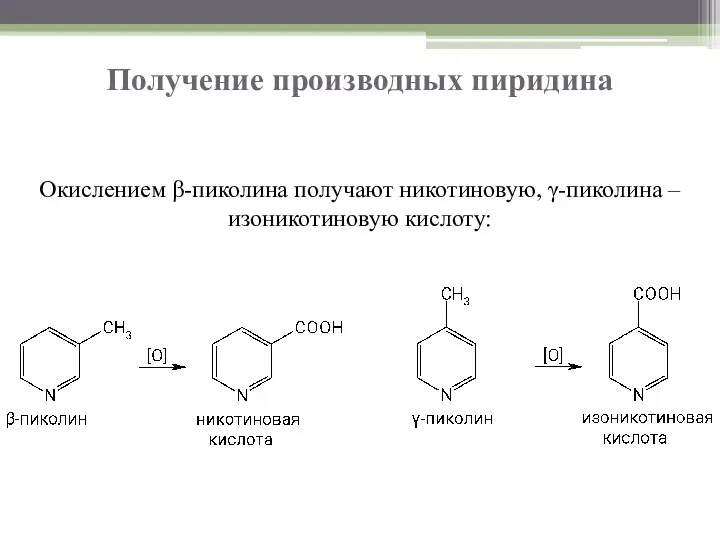
- 5. Получение производных пиридина Окислением β-пиколина получают никотиновую, γ-пиколина – изоникотиновую кислоту:
- 6. Производные никотиновой кислоты В медицинской практике применяют никотиновую кислоту (витамин РР) и ее производные: никотинамид, никетамид
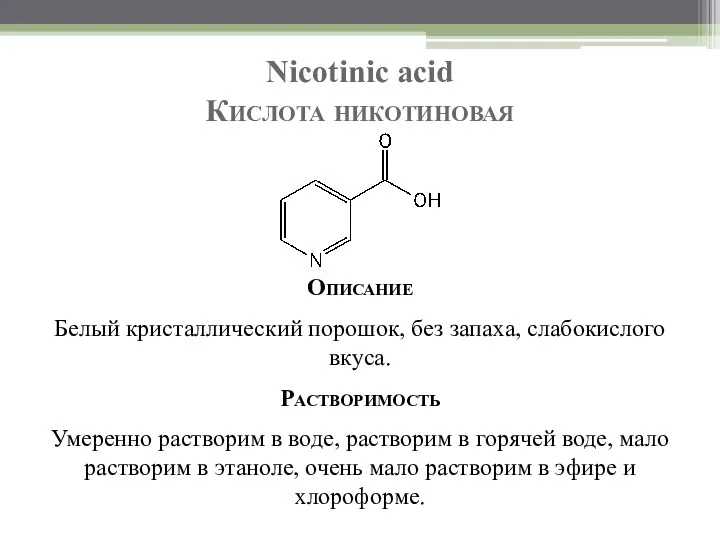
- 7. Nicotinic acid Кислота никотиновая Описание Белый кристаллический порошок, без запаха, слабокислого вкуса. Растворимость Умеренно растворим в
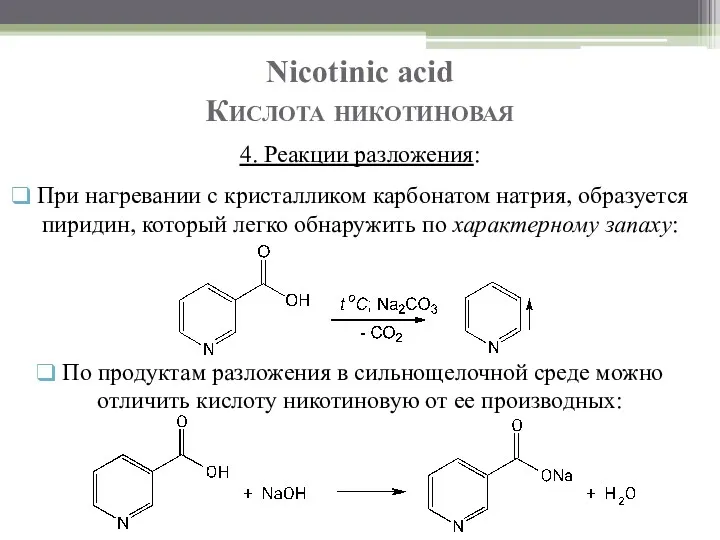
- 8. Nicotinic acid Кислота никотиновая Подлинность 1. Т.пл. 234 – 238°C. 2. ИК- и УФ-спектрофотометрия. 3. Реакция
- 9. Nicotinic acid Кислота никотиновая По продуктам разложения в сильнощелочной среде можно отличить кислоту никотиновую от ее
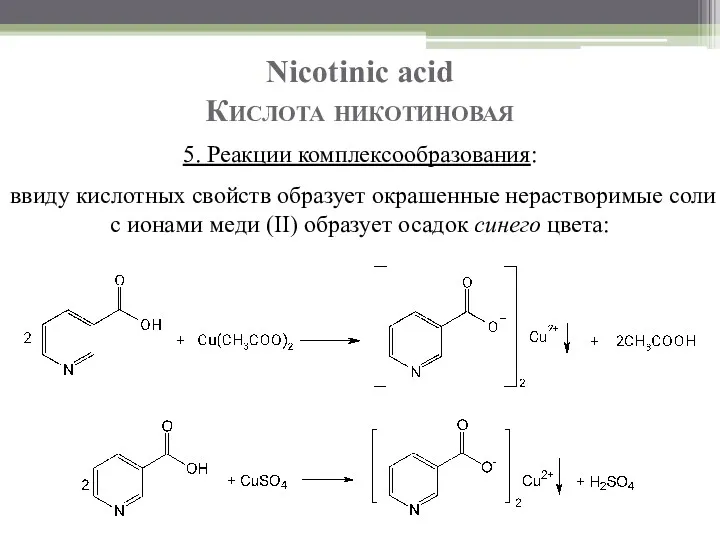
- 10. Nicotinic acid Кислота никотиновая 5. Реакции комплексообразования: ввиду кислотных свойств образует окрашенные нерастворимые соли с ионами
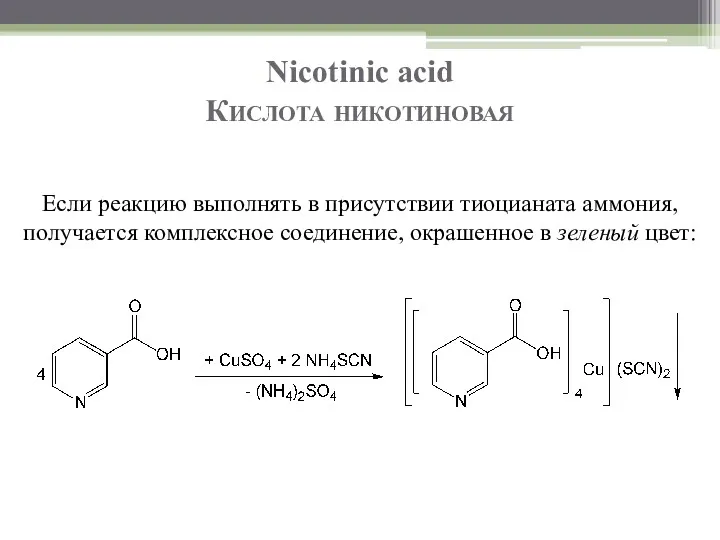
- 11. Nicotinic acid Кислота никотиновая Если реакцию выполнять в присутствии тиоцианата аммония, получается комплексное соединение, окрашенное в
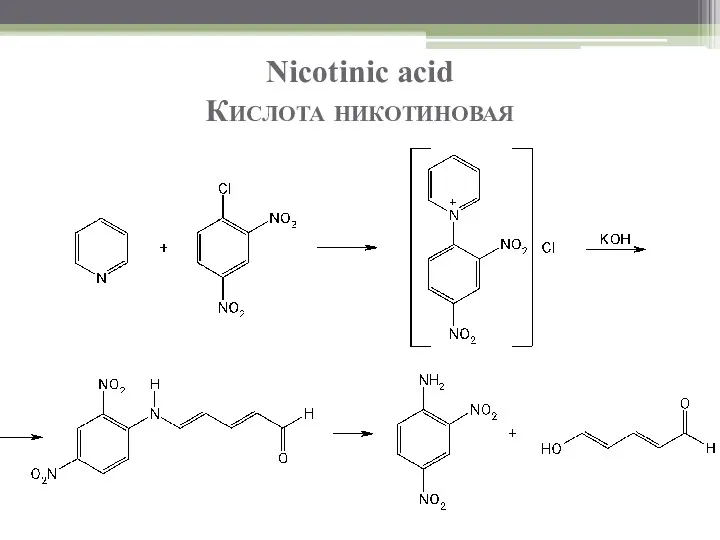
- 12. Nicotinic acid Кислота никотиновая 6. Реакции на пиридиновый цикл: При нагревании смеси раствора препарата, лимонной кислоты
- 13. Nicotinic acid Кислота никотиновая
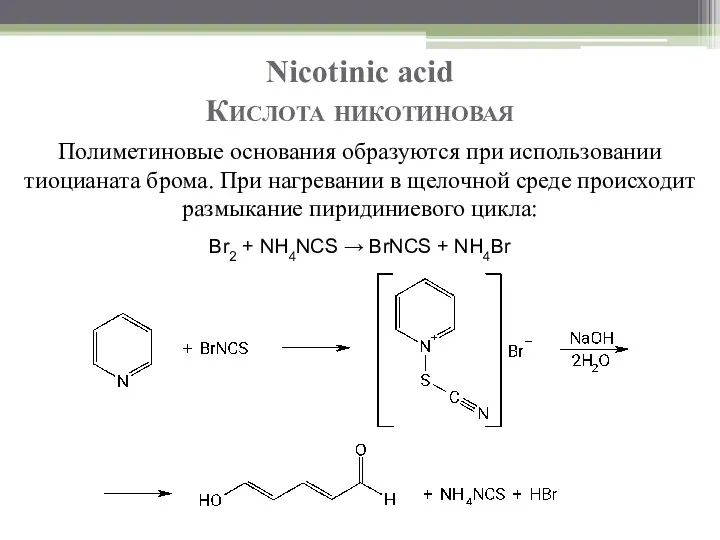
- 14. Nicotinic acid Кислота никотиновая Полиметиновые основания образуются при использовании тиоцианата брома. При нагревании в щелочной среде
- 15. Nicotinic acid Кислота никотиновая При последующем добавлении первичных ароматических аминов происходит их конденсация с глутаконовым альдегидом
- 16. Nicotinic acid Кислота никотиновая Испытания на чистоту Устанавливают прозрачность, цветность. Содержание примесей (хлоридов, сульфатов, нитратов, 2,6-
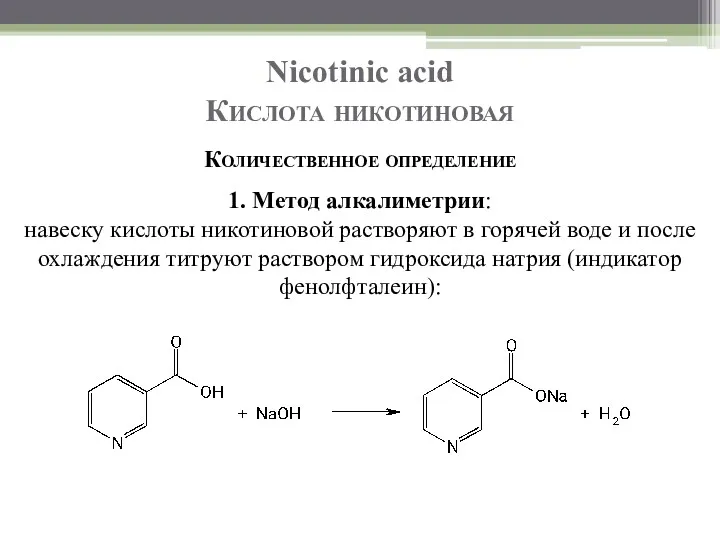
- 17. Nicotinic acid Кислота никотиновая Количественное определение 1. Метод алкалиметрии: навеску кислоты никотиновой растворяют в горячей воде
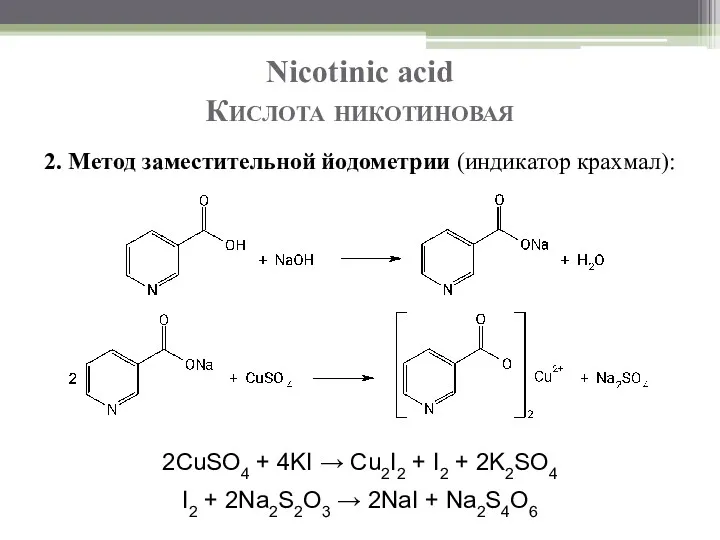
- 18. Nicotinic acid Кислота никотиновая 2. Метод заместительной йодометрии (индикатор крахмал): 2CuSO4 + 4KI → Cu2I2 +
- 19. Nicotinic acid Кислота никотиновая Хранение Список Б, в хорошо укупоренной таре, предохраняющей от действия света. Применение
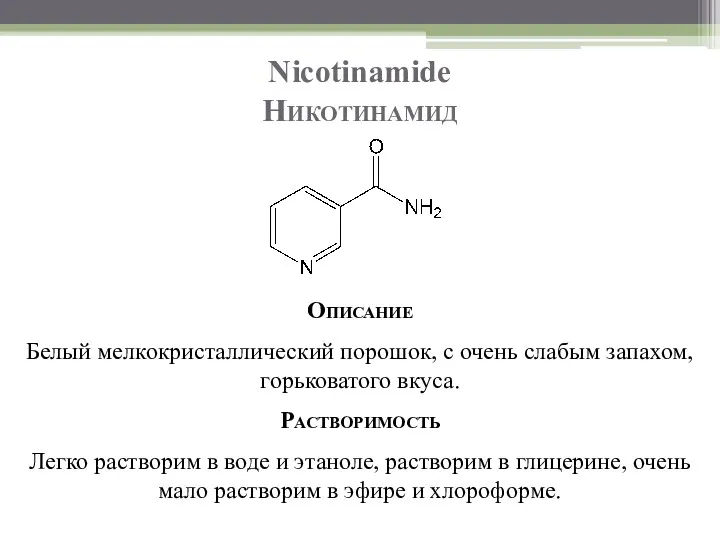
- 20. Nicotinamide Никотинамид Описание Белый мелкокристаллический порошок, с очень слабым запахом, горьковатого вкуса. Растворимость Легко растворим в
- 21. Nicotinamide Никотинамид Подлинность 1. Т.пл. 128–131°C. 2. ИК- и УФ-спектрофотометрия. 3. Реакция на третичные амины: 4.
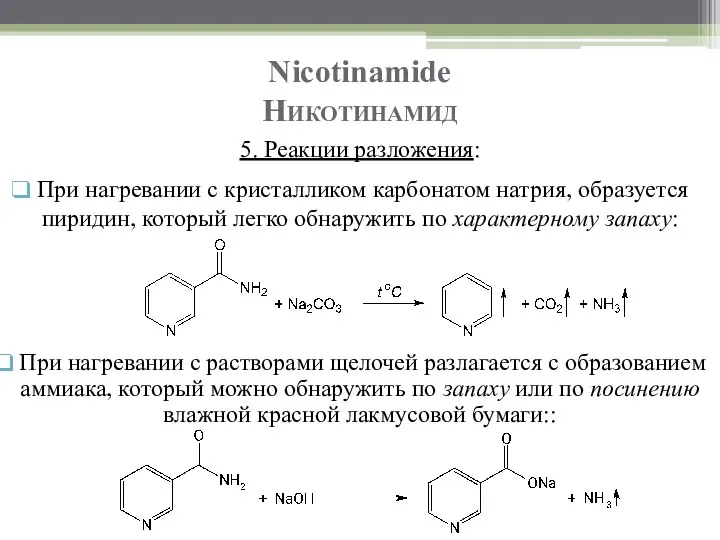
- 22. При нагревании с растворами щелочей разлагается с образованием аммиака, который можно обнаружить по запаху или по
- 23. Nicotinamide Никотинамид Испытания на чистоту Устанавливают прозрачность, цветность, рН раствора. Органические примеси. Потеря в весе при
- 24. Nicotinamide Никотинамид Количественное определение 1. Определение азота в органических соединениях: Определение по методу Кьельдаля. После разложения
- 25. Nicotinamide Никотинамид В приемнике образуется тетрагидроксиборат аммония, который оттитровывают 0,1 М раствором хлороводородной кислоты: H3BO3 +
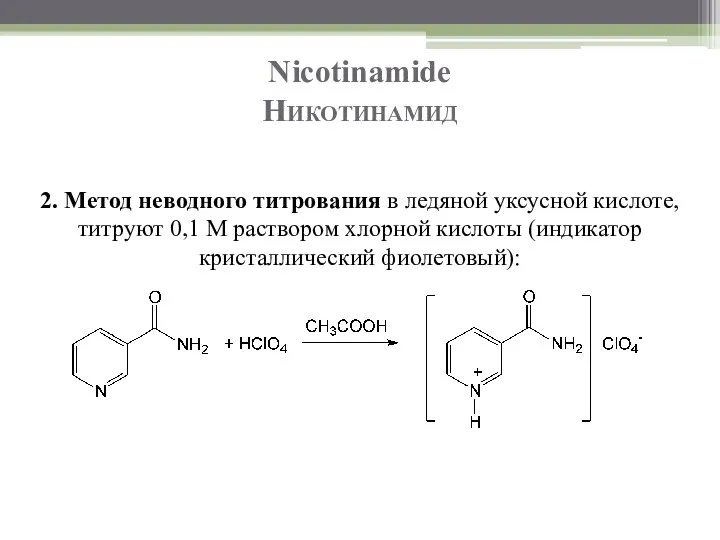
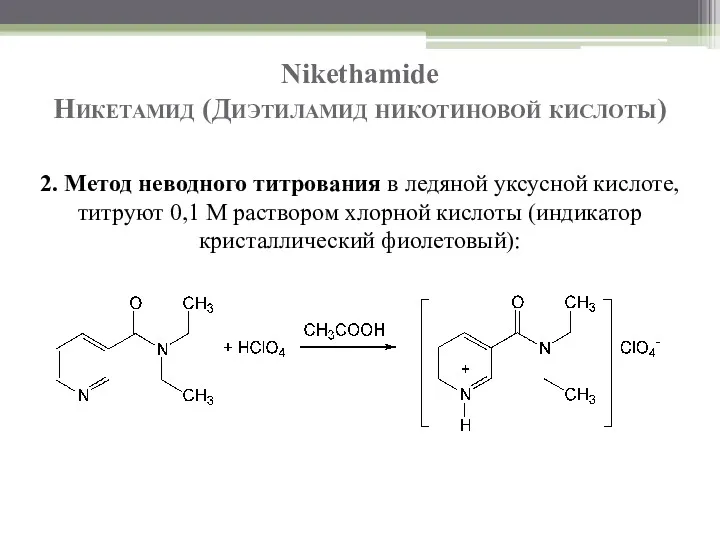
- 26. Nicotinamide Никотинамид 2. Метод неводного титрования в ледяной уксусной кислоте, титруют 0,1 М раствором хлорной кислоты
- 27. Nicotinamide Никотинамид Хранение В плотно укупоренной таре, предохраняющей от действия света. Применение Витаминный препарат. Является специфическим
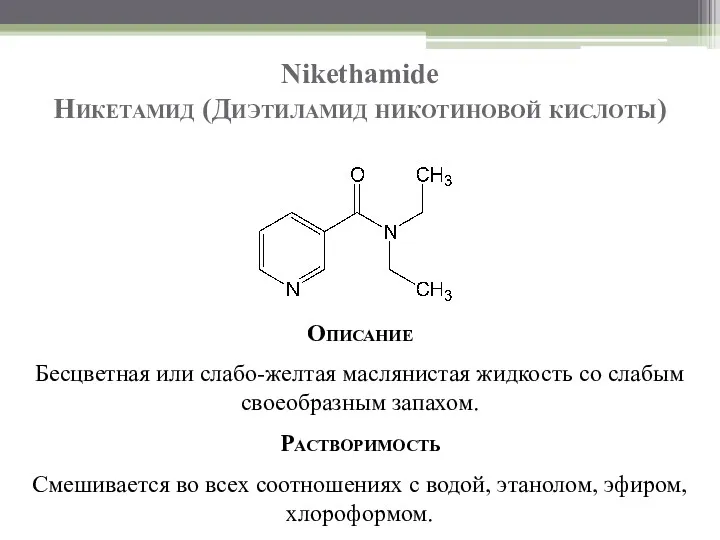
- 28. Nikethamide Никетамид (Диэтиламид никотиновой кислоты) Описание Бесцветная или слабо-желтая маслянистая жидкость со слабым своеобразным запахом. Растворимость
- 29. Nikethamide Никетамид (Диэтиламид никотиновой кислоты) Подлинность 1. Т. затвердевания 20 – 25°C. 2. Плотность 1,058 –
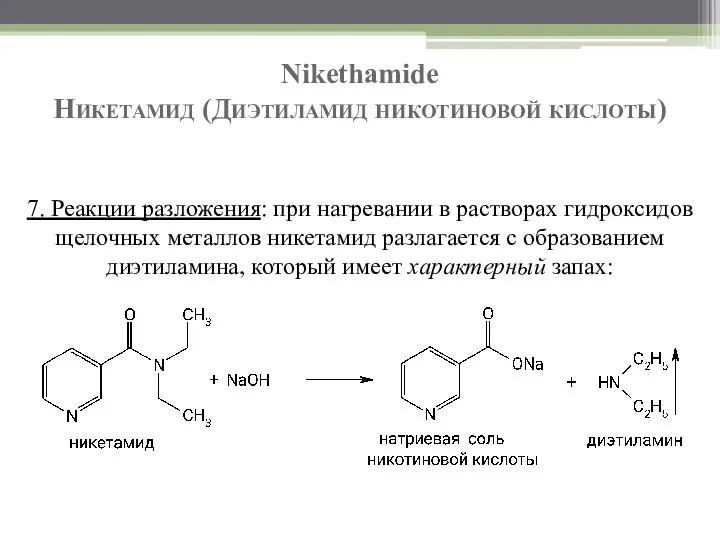
- 30. Nikethamide Никетамид (Диэтиламид никотиновой кислоты) 7. Реакции разложения: при нагревании в растворах гидроксидов щелочных металлов никетамид
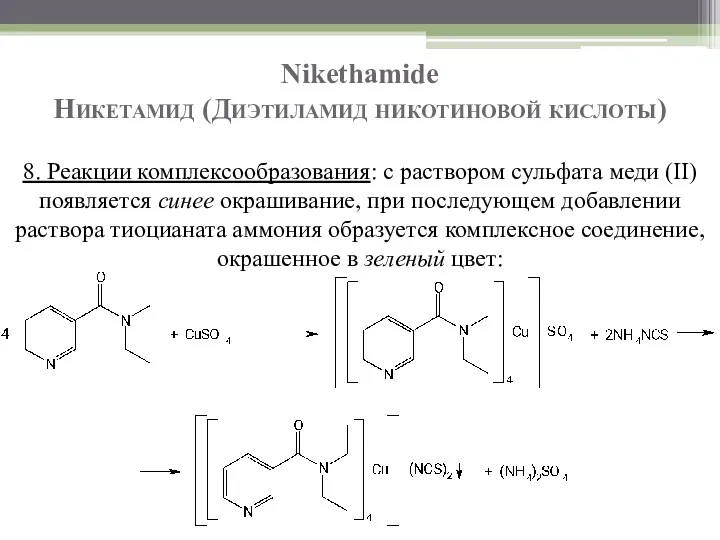
- 31. Nikethamide Никетамид (Диэтиламид никотиновой кислоты) 8. Реакции комплексообразования: с раствором сульфата меди (II) появляется синее окрашивание,
- 32. Nikethamide Никетамид (Диэтиламид никотиновой кислоты) Испытания на чистоту Устанавливают прозрачность, цветность, кислотность или щелочность раствора. Содержание
- 33. Nikethamide Никетамид (Диэтиламид никотиновой кислоты) Количественное определение 1. Определение азота в органических соединениях: Определение по методу
- 34. Nikethamide Никетамид (Диэтиламид никотиновой кислоты) В приемнике образуется тетрагидроксиборат диэтиламина, который оттитровывают 0,1 М раствором хлороводородной
- 35. Nikethamide Никетамид (Диэтиламид никотиновой кислоты) 2. Метод неводного титрования в ледяной уксусной кислоте, титруют 0,1 М
- 36. Nikethamide Никетамид (Диэтиламид никотиновой кислоты) Хранение В плотно укупоренной таре, предохраняющей от действия света. Применение Никетамид
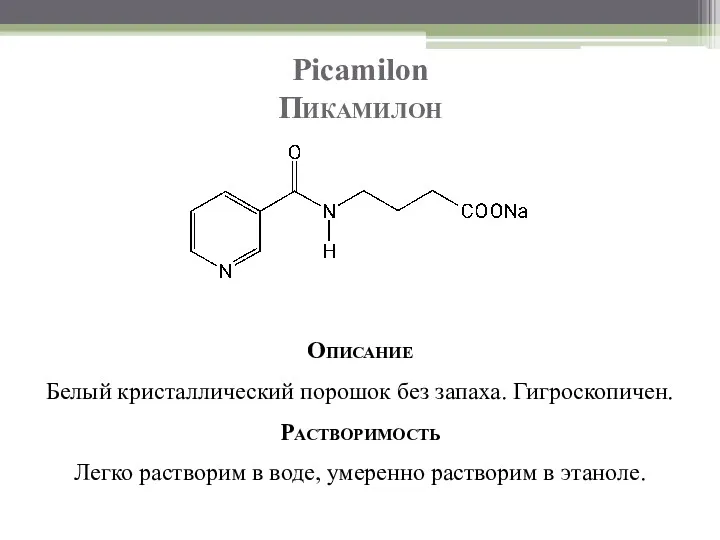
- 37. Picamilon Пикамилон Описание Белый кристаллический порошок без запаха. Гигроскопичен. Растворимость Легко растворим в воде, умеренно растворим
- 38. Picamilon Пикамилон Подлинность 1. ИК- и УФ-спектрофотометрия. 2. Реакции на пиридиновый цикл. 3. Реакции на третичные
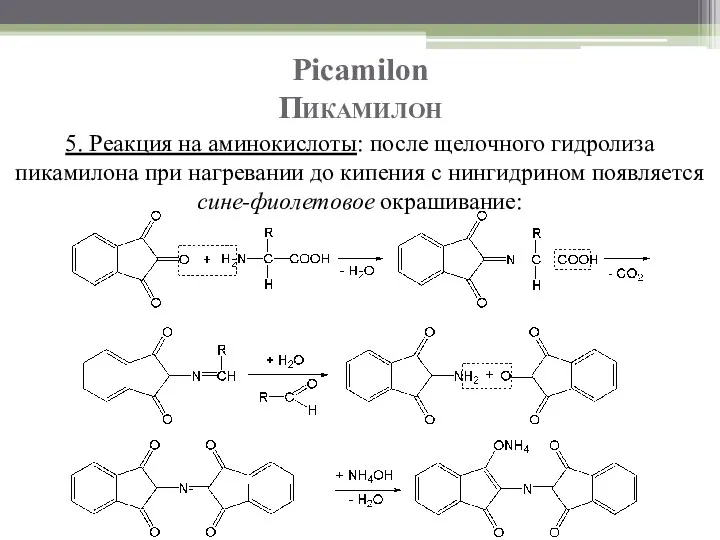
- 39. Picamilon Пикамилон 5. Реакция на аминокислоты: после щелочного гидролиза пикамилона при нагревании до кипения с нингидрином
- 40. Picamilon Пикамилон Испытания на чистоту Прозрачность, цветность, кислотность или щелочность раствора. Содержание примесей (хлоридов, сульфатов, тяжелых
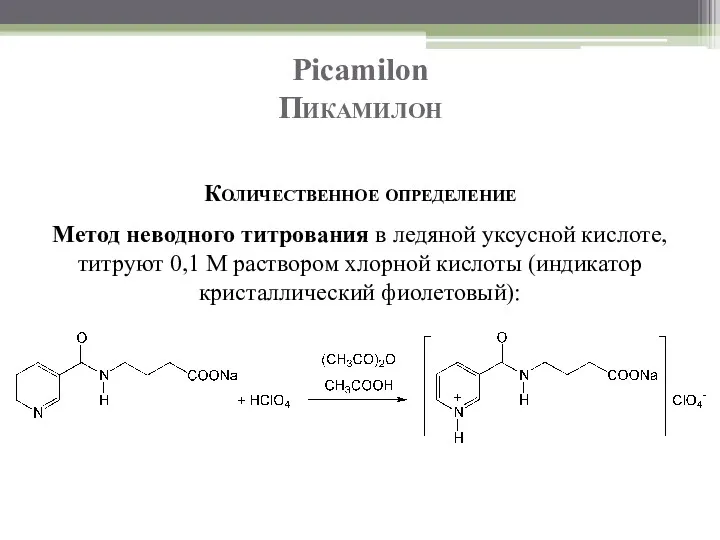
- 41. Picamilon Пикамилон Количественное определение Метод неводного титрования в ледяной уксусной кислоте, титруют 0,1 М раствором хлорной
- 42. Picamilon Пикамилон Хранение Список Б, в хорошо укупоренной таре, предохраняющей от действия света, в сухом месте.
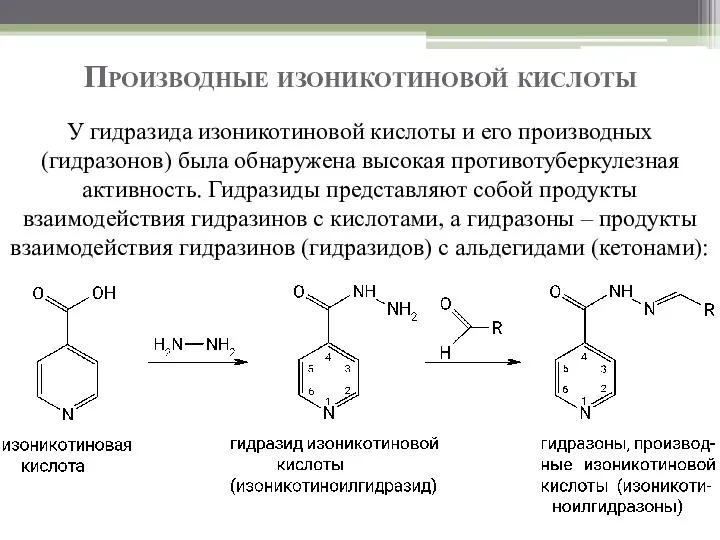
- 43. Производные изоникотиновой кислоты У гидразида изоникотиновой кислоты и его производных (гидразонов) была обнаружена высокая противотуберкулезная активность.
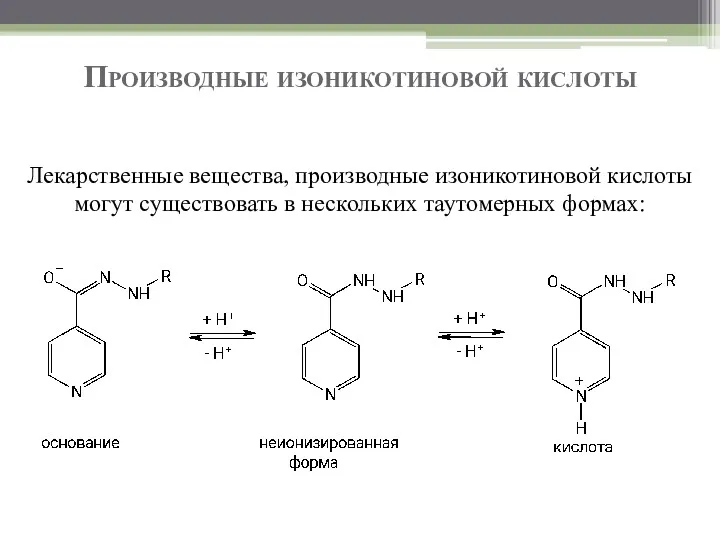
- 44. Производные изоникотиновой кислоты Лекарственные вещества, производные изоникотиновой кислоты могут существовать в нескольких таутомерных формах:
- 45. Производные изоникотиновой кислоты При этом они могут проявлять в растворах как кислотные, так и основные свойства.
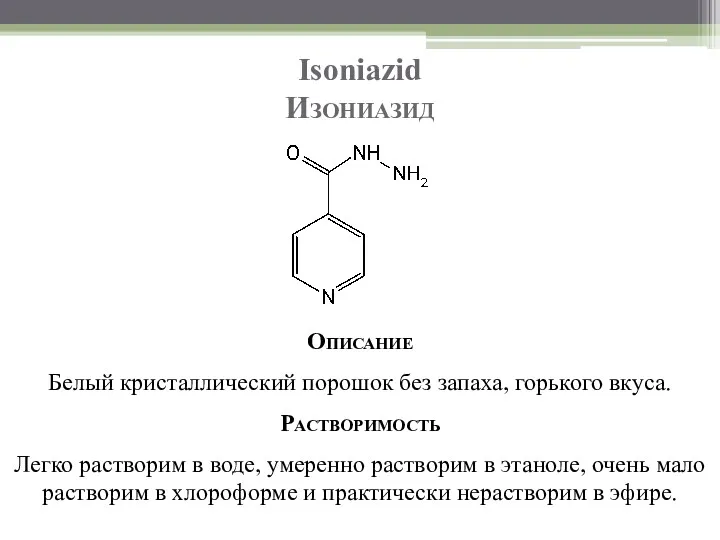
- 46. Isoniazid Изониазид Описание Белый кристаллический порошок без запаха, горького вкуса. Растворимость Легко растворим в воде, умеренно
- 47. Isoniazid Изониазид Подлинность Т. пл. 170–174 °C. ИК-спектроскопия (ИК-спектры, снятые в вазелиновом масле в области 3700-400
- 48. Isoniazid Изониазид Реакции на третичный атом азота: С реактивом Зоненштейна (фосфорномолибденовая кислота) выпадает желтый осадок, который
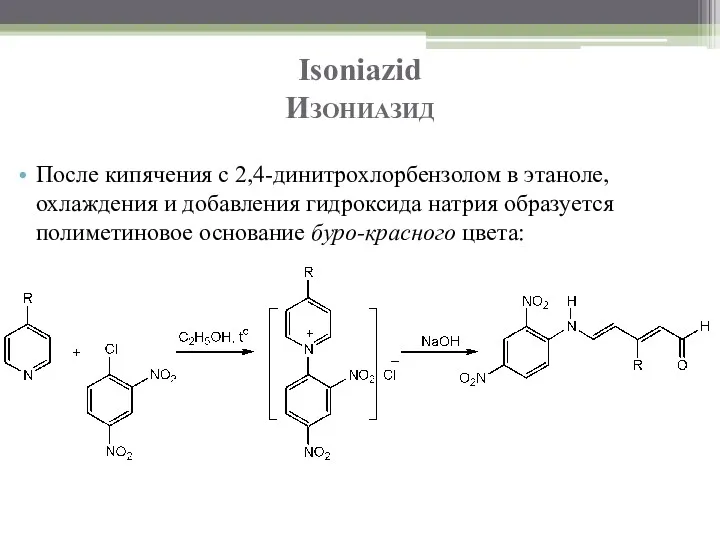
- 49. Isoniazid Изониазид После кипячения с 2,4-динитрохлорбензолом в этаноле, охлаждения и добавления гидроксида натрия образуется полиметиновое основание
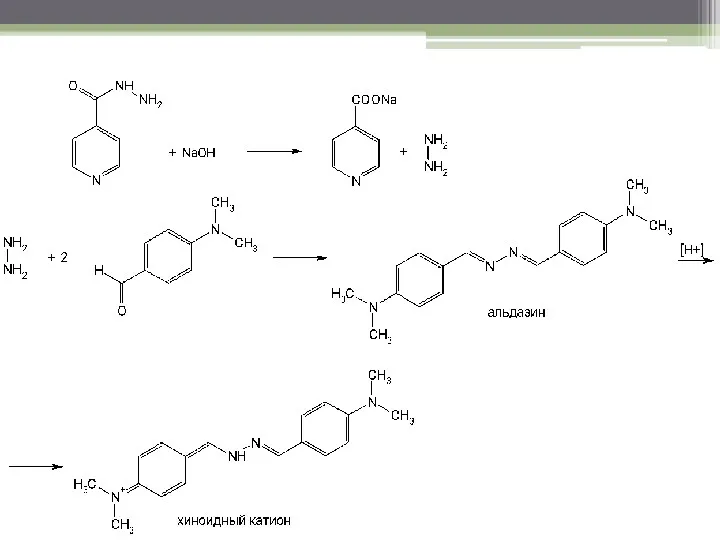
- 50. Isoniazid Изониазид Реакция щелочного гидролиза: при нагревании с раствором щелочи образуется гидразин, который конденсируют с n-диметиламинобензальдегидом
- 52. Isoniazid Изониазид Реакция «серебряного зеркала»: с аммиачным раствором нитрата серебра выделяется серебро в виде осадка серого
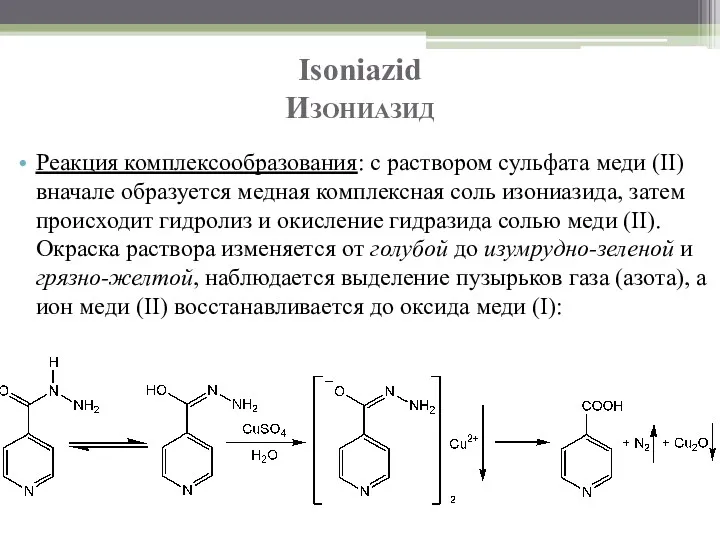
- 53. Isoniazid Изониазид Реакция комплексообразования: с раствором сульфата меди (II) вначале образуется медная комплексная соль изониазида, затем
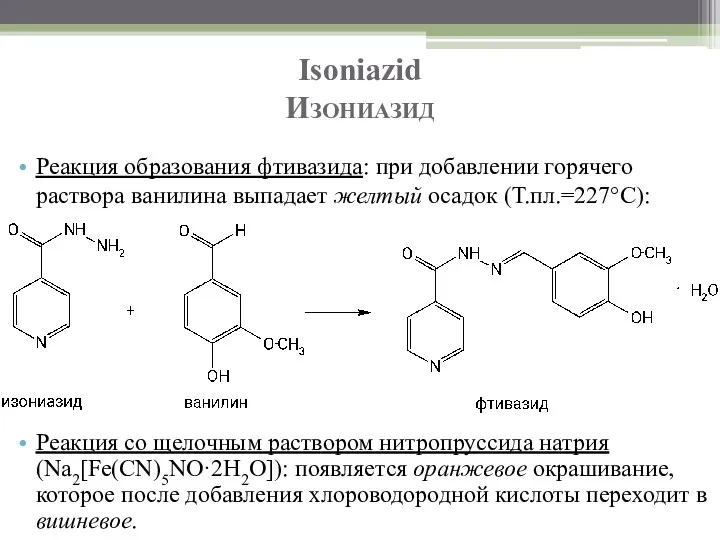
- 54. Isoniazid Изониазид Реакция образования фтивазида: при добавлении горячего раствора ванилина выпадает желтый осадок (Т.пл.=227°C): Реакция со
- 55. Isoniazid Изониазид Испытания на чистоту Кислотность и щелочность, прозрачность и цветность раствора. Предельно допустимые количества примесей
- 56. Isoniazid Изониазид Количественное определение Метод обратной йодометрии: основан на окислении продуктов гидролиза препарата йодом в слабощелочной
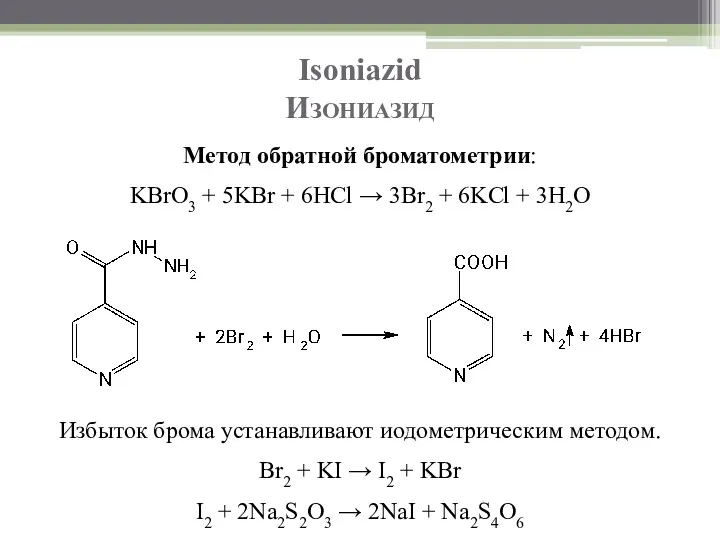
- 57. Isoniazid Изониазид Метод обратной броматометрии: KBrO3 + 5KBr + 6HCl → 3Br2 + 6KCl + 3H2O
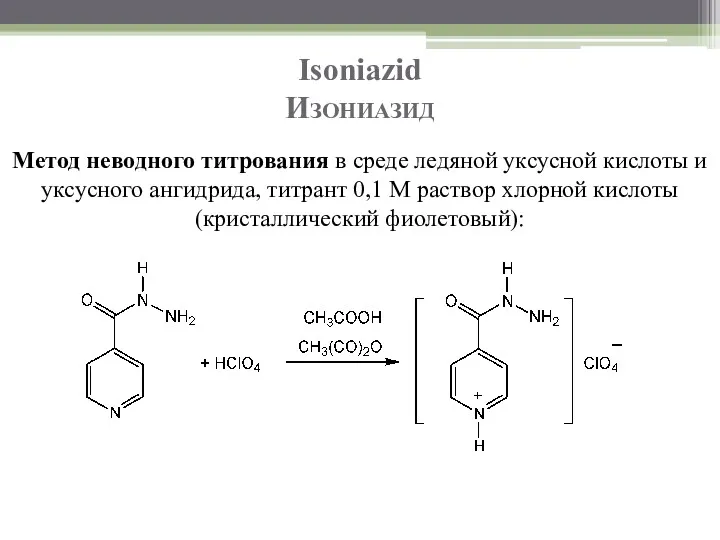
- 58. Isoniazid Изониазид Метод неводного титрования в среде ледяной уксусной кислоты и уксусного ангидрида, титрант 0,1 М
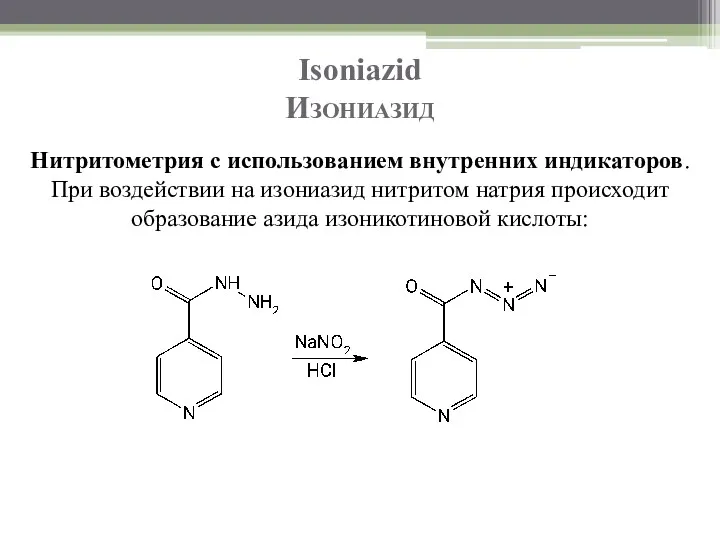
- 59. Isoniazid Изониазид Нитритометрия с использованием внутренних индикаторов. При воздействии на изониазид нитритом натрия происходит образование азида
- 60. Isoniazid Изониазид Фотометрический метод основан на образовании изониазида окрашенных продуктов с различными реактивами (п-диметиламинобензальдегидом). Спектрофотометрическое определение
- 61. Isoniazid Изониазид Хранение Список Б, в хорошо укупоренной таре, в прохладном, защищенном от света сухом месте.
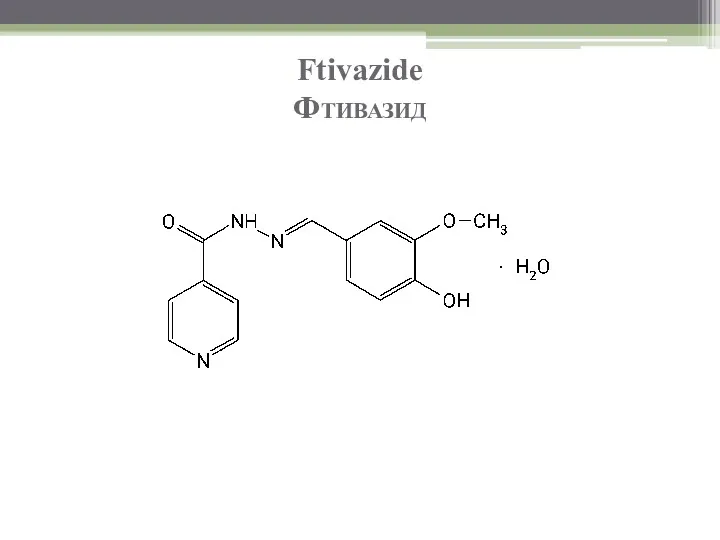
- 62. Ftivazide Фтивазид
- 63. Ftivazide Фтивазид Описание Светло-желтый мелкокристаллический порошок со слабым запахом ванилина, без вкуса. Растворимость Практически нерастворим в
- 64. Ftivazide Фтивазид Подлинность ИК-спектроскопия (ИК-спектры, снятые в вазелиновом масле в области 3700-400 см–1 должны полностью совпадать
- 65. Ftivazide Фтивазид Реакции на третичный атом азота: с реактивом Зоненштейна (фосфорномолибденовая кислота) выпадает осадок, который при
- 66. Ftivazide Фтивазид Реакция с камфорой: при добавлении к раствору препарата концентрированной серной кислоты и камфоры появляется
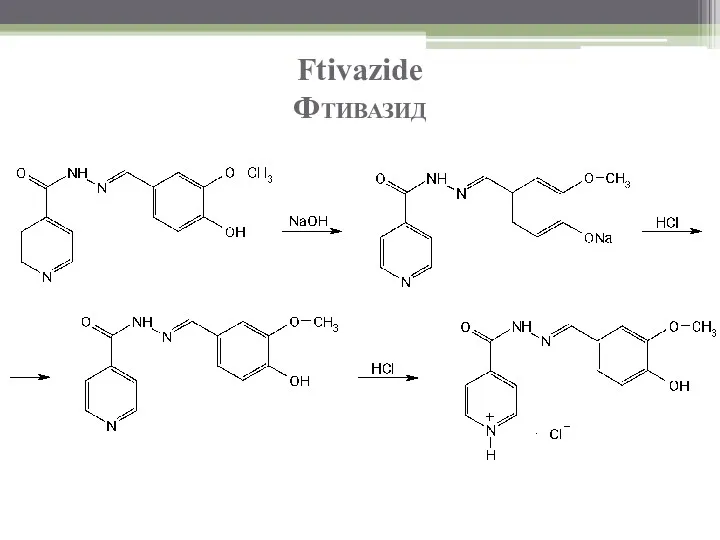
- 67. Ftivazide Фтивазид
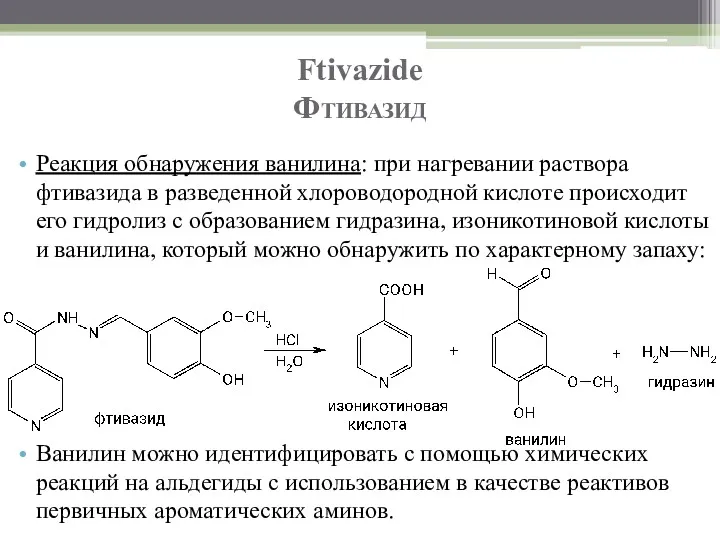
- 68. Ftivazide Фтивазид Реакция обнаружения ванилина: при нагревании раствора фтивазида в разведенной хлороводородной кислоте происходит его гидролиз
- 69. Ftivazide Фтивазид Испытания на чистоту ПДК примесей (хлоридов, сульфатов, тяжелых металлов). Примесь гидразида изоникотиновой кислоты обнаруживают
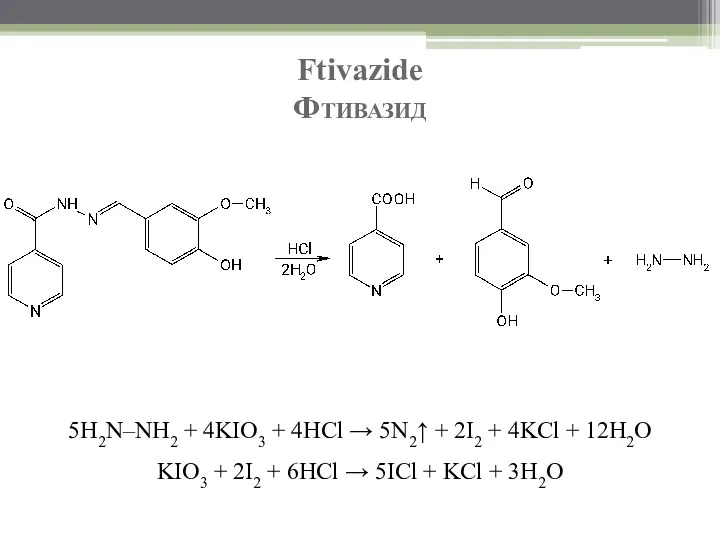
- 70. Ftivazide Фтивазид Количественное определение Йодатометрический метод: после предварительного гидролиза в солянокислой среде. Выделяющийся при гидролизе гидразин
- 71. Ftivazide Фтивазид 5H2N–NH2 + 4KIO3 + 4HCl → 5N2↑ + 2I2 + 4KCl + 12H2O KIO3
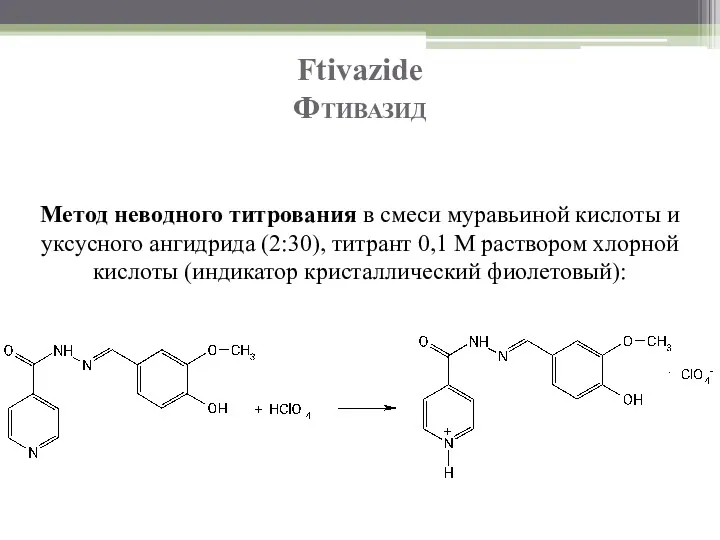
- 72. Ftivazide Фтивазид Метод неводного титрования в смеси муравьиной кислоты и уксусного ангидрида (2:30), титрант 0,1 М
- 73. Ftivazide Фтивазид Фотометрический метод основан на образовании фтивазида окрашенных продуктов с различными реактивами. Спектрофотометрическое определение можно
- 74. Ftivazide Фтивазид Хранение Список Б, в хорошо укупоренной таре, в прохладном, защищенном от света сухом месте.
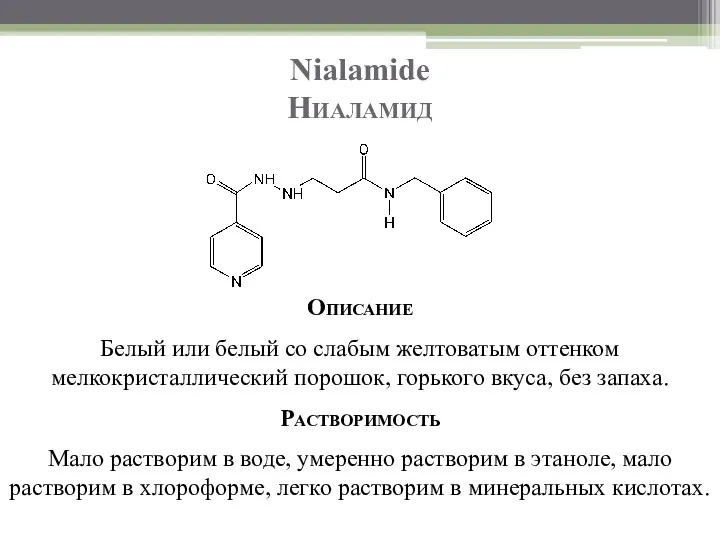
- 75. Nialamide Ниаламид Описание Белый или белый со слабым желтоватым оттенком мелкокристаллический порошок, горького вкуса, без запаха.
- 76. Nialamide Ниаламид Подлинность Т.пл. 151–153 °C УФ-спектроскопия (раствор ниаламида в 0,1 М растворе хлороводородной кислоты имеет
- 77. Nialamide Ниаламид Испытания на чистоту ПДК примесей (хлоридов, сульфатов, тяжелых металлов). Посторонние примеси (не более 1%)
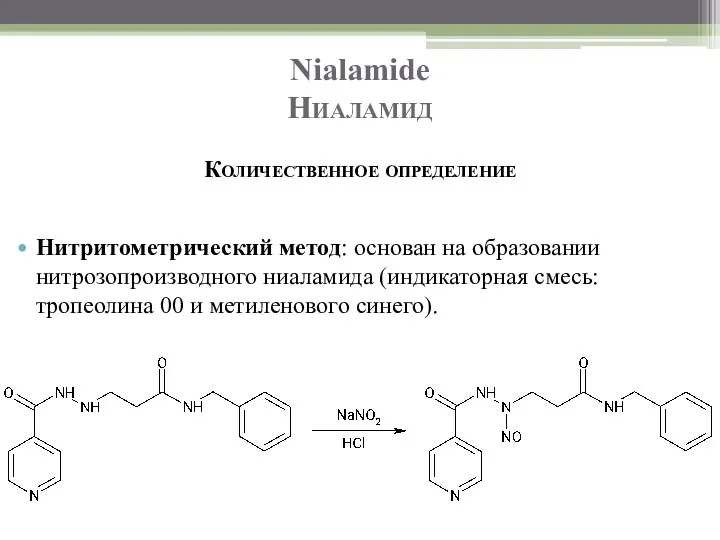
- 78. Nialamide Ниаламид Количественное определение Нитритометрический метод: основан на образовании нитрозопроизводного ниаламида (индикаторная смесь: тропеолина 00 и
- 79. Nialamide Ниаламид Фотометрический метод основан на образовании фтивазида окрашенных продуктов с различными реактивами. Спектрофотометрическое определение можно
- 80. Nialamide Ниаламид Хранение Список Б, в хорошо укупоренной таре, в прохладном, защищенном от света сухом месте.
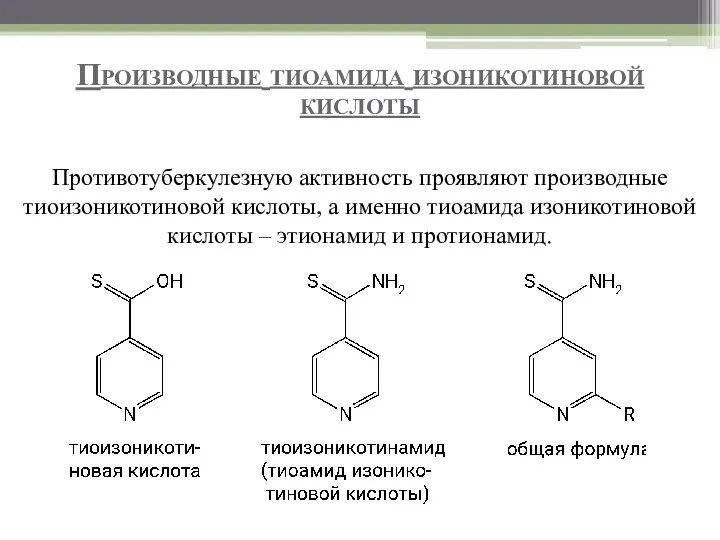
- 81. Производные тиоамида изоникотиновой кислоты Противотуберкулезную активность проявляют производные тиоизоникотиновой кислоты, а именно тиоамида изоникотиновой кислоты –
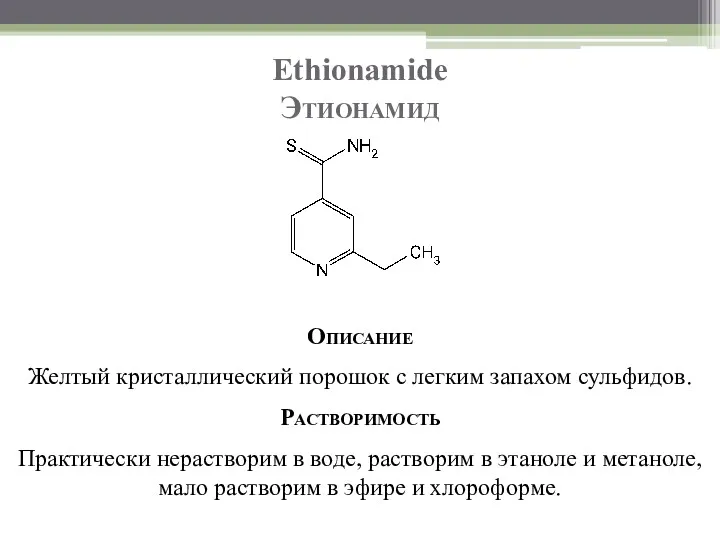
- 82. Ethionamide Этионамид Описание Желтый кристаллический порошок с легким запахом сульфидов. Растворимость Практически нерастворим в воде, растворим
- 83. Ethionamide Этионамид Подлинность Т. пл. 158–164 °C. ИК-спектроскопия: ИК-спектры, снятые в области 4000-625 см–1 должны полностью
- 84. Ethionamide Этионамид Реакции на третичный атом азота: С реактивом Зоненштейна (фосфорномолибденовая кислота) выпадает желтый осадок, который
- 85. Ethionamide Этионамид Реакции на пиридиновый цикл: При нагревании на кипящей водяной бане с уксусным ангидридом в
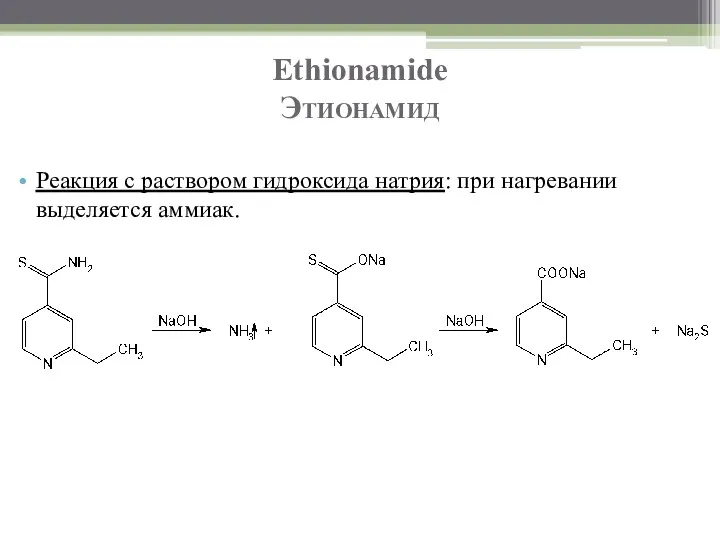
- 86. Ethionamide Этионамид Реакция с раствором гидроксида натрия: при нагревании выделяется аммиак.
- 87. Ethionamide Этионамид Реакция на органически связанную серу: при нагревании смеси этионамида с хлороводородной кислотой выделяющиеся пары
- 88. Ethionamide Этионамид Испытания на чистоту Посторонние примеси (не более 0,5%) определяют методом ТСХ, используя в качестве
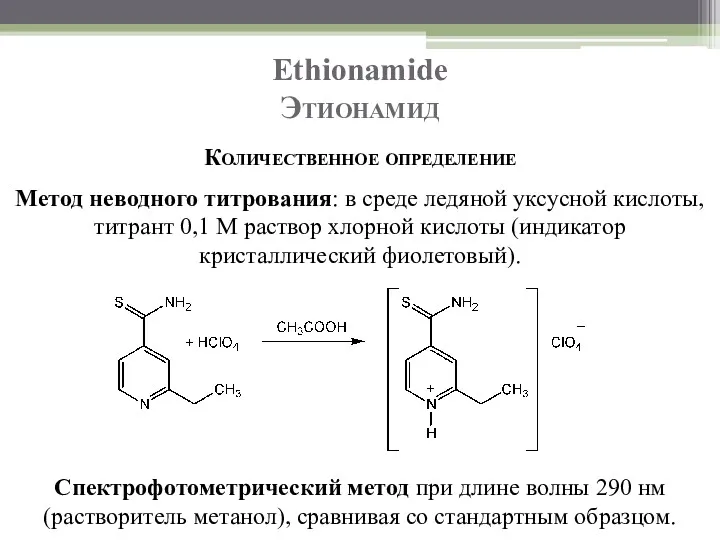
- 89. Ethionamide Этионамид Количественное определение Метод неводного титрования: в среде ледяной уксусной кислоты, титрант 0,1 М раствор
- 90. Ethionamide Этионамид Хранение Список Б, в плотно укупоренной таре, предохраняющей от действия света и влаги, при
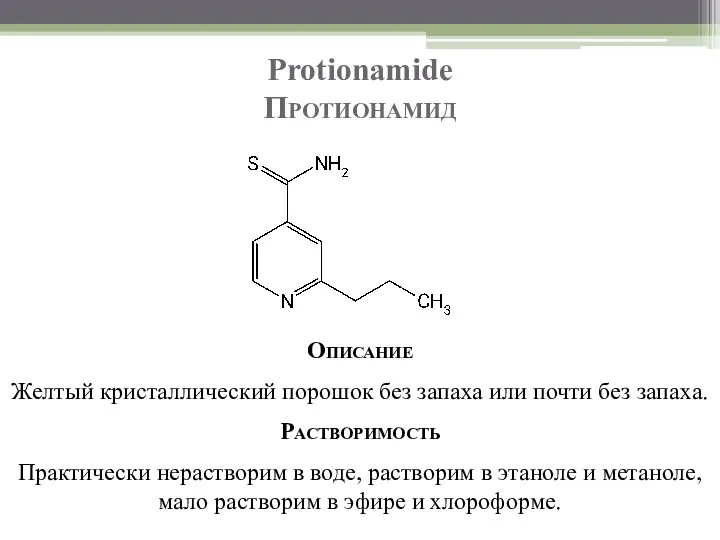
- 91. Protionamide Протионамид Описание Желтый кристаллический порошок без запаха или почти без запаха. Растворимость Практически нерастворим в
- 92. Protionamide Протионамид Подлинность Т. пл. 140–143 °C. ИК-спектроскопия: ИК-спектры, снятые в области 4000-625 см–1 должны полностью
- 93. Protionamide Протионамид Реакции на третичный атом азота. Реакция на пиридиновый цикл. Реакция с раствором гидроксида натрия:
- 94. Protionamide Протионамид Испытания на чистоту Посторонние примеси (не более 0,5%) определяют методом ТСХ, используя в качестве
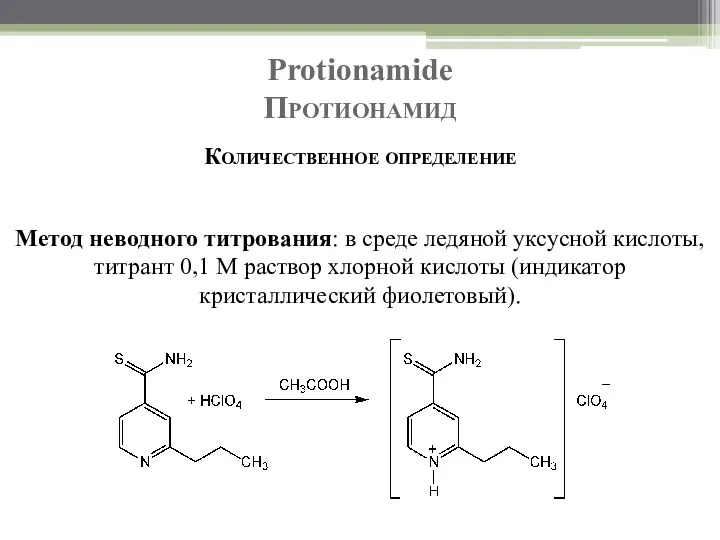
- 95. Protionamide Протионамид Количественное определение Метод неводного титрования: в среде ледяной уксусной кислоты, титрант 0,1 М раствор
- 97. Скачать презентацию

















































 Строение электронных оболочек атомов химических элементов 8 класс
Строение электронных оболочек атомов химических элементов 8 класс Моно- та дикарбонові кислоти. Функціональні похідні карбонових кислот
Моно- та дикарбонові кислоти. Функціональні похідні карбонових кислот Alcohols. Learning Objectives
Alcohols. Learning Objectives Аммиак. Состав вещества
Аммиак. Состав вещества Кислородные соединения углерода
Кислородные соединения углерода Природный и попутный нефтяные газы
Природный и попутный нефтяные газы Сущность процесса электролиза
Сущность процесса электролиза Разработка и добыча нефти и газа. (Тема 1.5)
Разработка и добыча нефти и газа. (Тема 1.5) Серная кислота. 9 класс
Серная кислота. 9 класс Сахароза
Сахароза Фосфонсірке қышқылының антипирендік қасиеттерін зерттеу
Фосфонсірке қышқылының антипирендік қасиеттерін зерттеу Медь. Физические свойства
Медь. Физические свойства Кислотно-основное титрование
Кислотно-основное титрование Амины и их свойства
Амины и их свойства Ферум та його сполуки
Ферум та його сполуки Галогенопроизводные. Растворимость, общие закономерности
Галогенопроизводные. Растворимость, общие закономерности Синтез, фото- и ионохромные свойства спиропиранов на основе гидроксихинолинового альдегида
Синтез, фото- и ионохромные свойства спиропиранов на основе гидроксихинолинового альдегида Природные источники углеводородов
Природные источники углеводородов Методика обучения и воспитания на уроках химии
Методика обучения и воспитания на уроках химии 20231113_tipy_him._reaktsiy_prezentatsiya
20231113_tipy_him._reaktsiy_prezentatsiya Минералы свинца
Минералы свинца Кремний и его соединения
Кремний и его соединения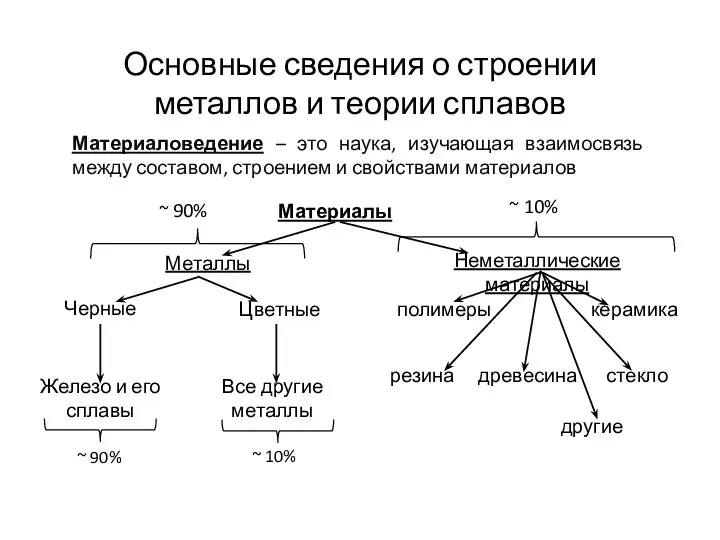 Основные сведения о строении металлов и теории сплавов
Основные сведения о строении металлов и теории сплавов Коррозия металлов. Часть 2. Лекция №11
Коррозия металлов. Часть 2. Лекция №11 Карбоксильные соединения. Гидроксикислоты, кетонокислоты
Карбоксильные соединения. Гидроксикислоты, кетонокислоты Зелена хімія
Зелена хімія Високомолекулярні сполуки. Полімери
Високомолекулярні сполуки. Полімери Місце хімії серед наук про природу
Місце хімії серед наук про природу