Содержание
- 2. ЦЕЛИ ЛЕКЦИИ ОБУЧАЮЩАЯ: сформировать знания о строении, номенклатуре и реакционной способности карбоновых кислот, гидроксикислот и кетонокислот.
- 3. ПЛАН ЛЕКЦИИ Классификация карбоновых кислот Химические свойства карбоновых кислот Салициловая кислота, фарм. препараты на её основе
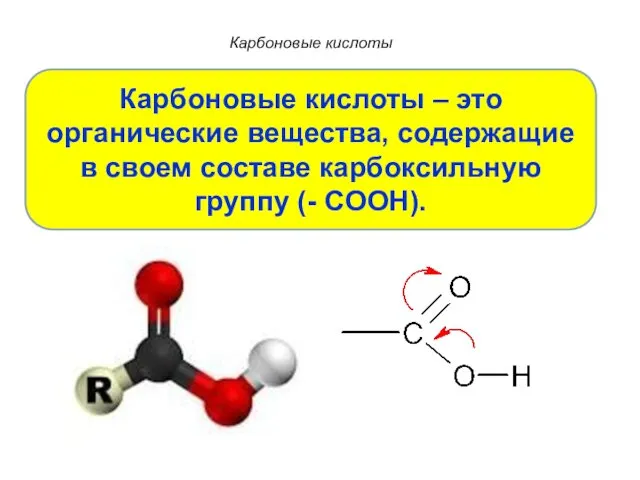
- 4. Карбоновые кислоты Карбоновые кислоты – это органические вещества, содержащие в своем составе карбоксильную группу (- COOH).
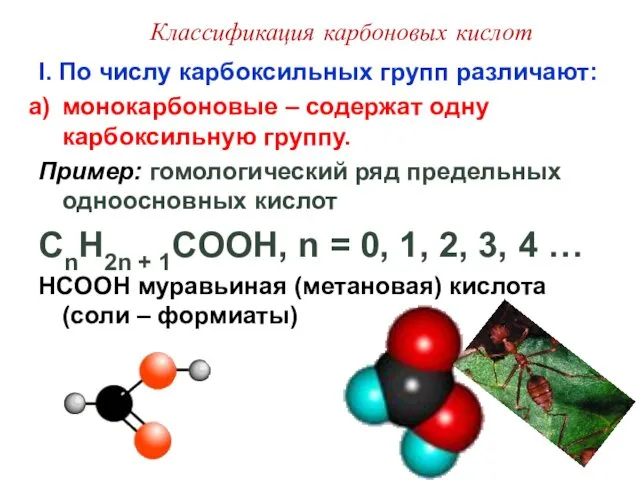
- 5. Классификация карбоновых кислот I. По числу карбоксильных групп различают: монокарбоновые – содержат одну карбоксильную группу. Пример:
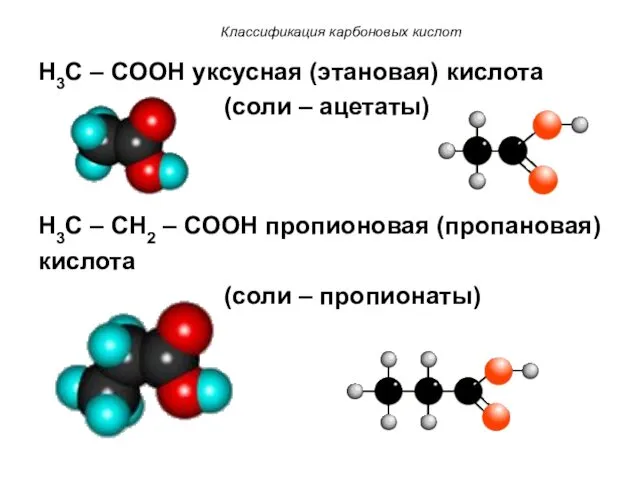
- 6. Классификация карбоновых кислот H3C – COOH уксусная (этановая) кислота (соли – ацетаты) H3C – CH2 –
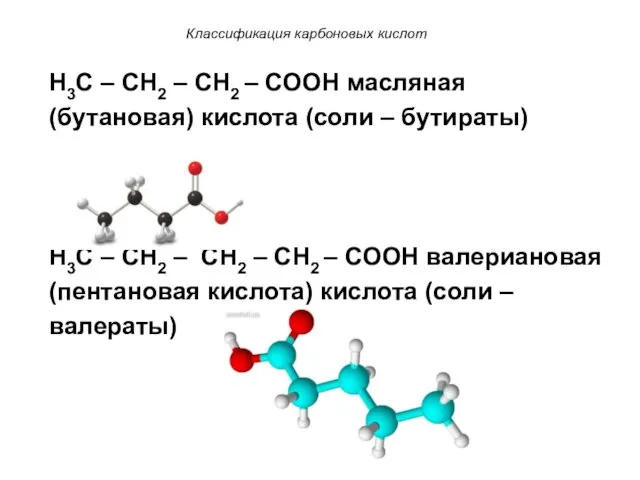
- 7. Классификация карбоновых кислот H3C – CH2 – CH2 – COOH масляная (бутановая) кислота (соли – бутираты)
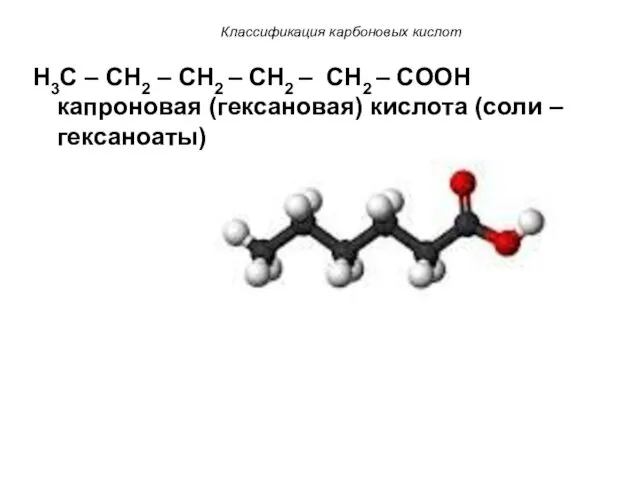
- 8. Классификация карбоновых кислот H3C – CH2 – CH2 – CH2 – CH2 – COOH капроновая (гексановая)
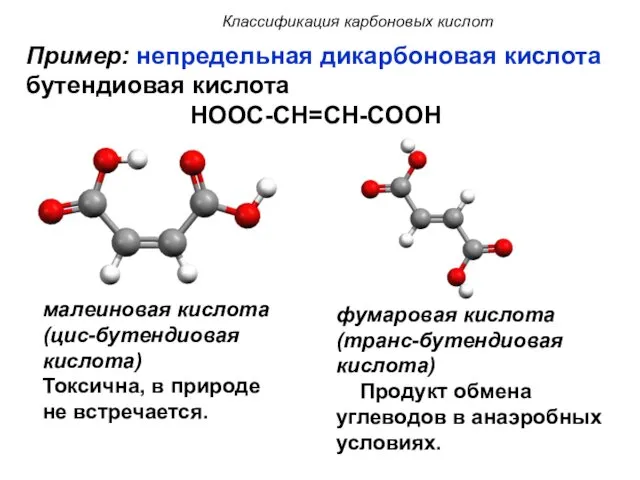
- 9. Классификация карбоновых кислот b) поликарбоновые – содержат в своем составе две и более карбоксильные группы. Пример:
- 10. малеиновая кислота (цис-бутендиовая кислота) Токсична, в природе не встречается. фумаровая кислота (транс-бутендиовая кислота) Продукт обмена углеводов
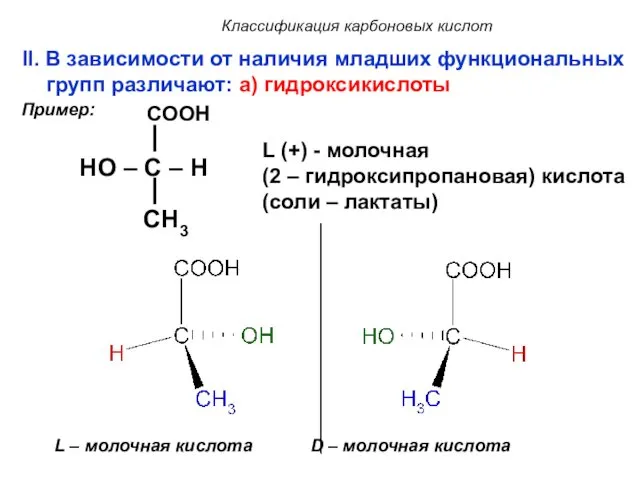
- 11. Классификация карбоновых кислот II. В зависимости от наличия младших функциональных групп различают: a) гидроксикислоты COOH HO
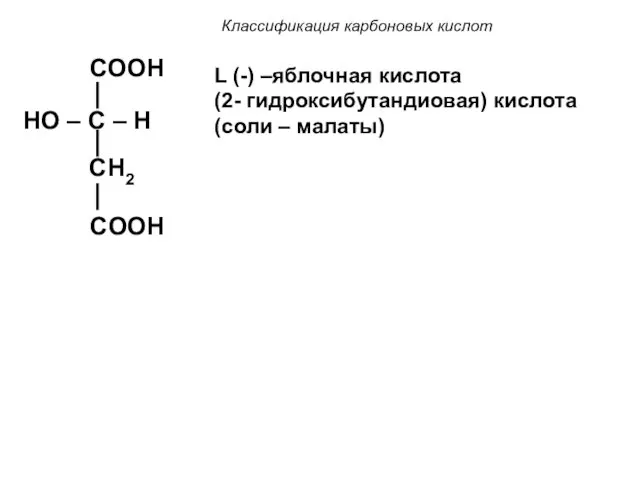
- 12. Классификация карбоновых кислот COOH HO – C – H CH2 COOH L (-) –яблочная кислота (2-
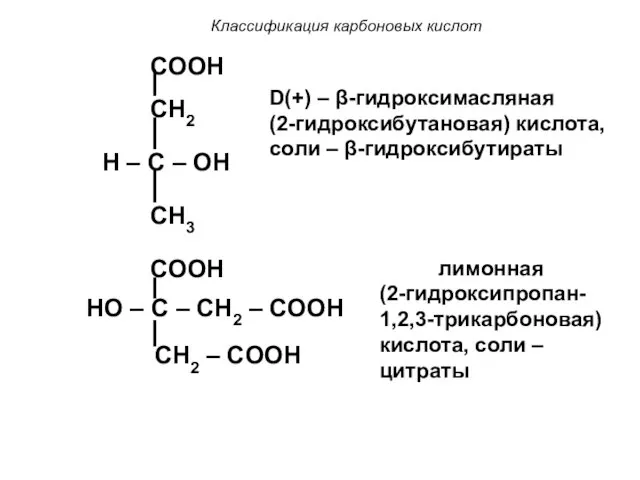
- 13. Классификация карбоновых кислот COOH CH2 H – C – OH CH3 D(+) – β-гидроксимасляная (2-гидроксибутановая) кислота,
- 14. Классификация карбоновых кислот Гидроксикислоты являются, как правило, твёрдыми телами. Рацемическая молочная кислота может быть жидкой (т.
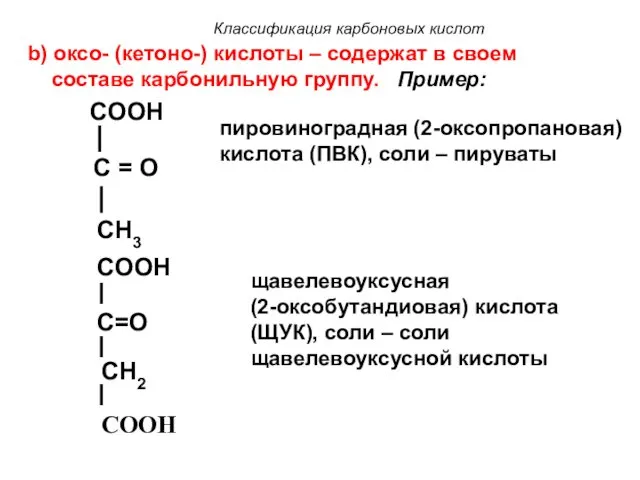
- 15. Классификация карбоновых кислот b) оксо- (кетоно-) кислоты – содержат в своем составе карбонильную группу. Пример: COOH
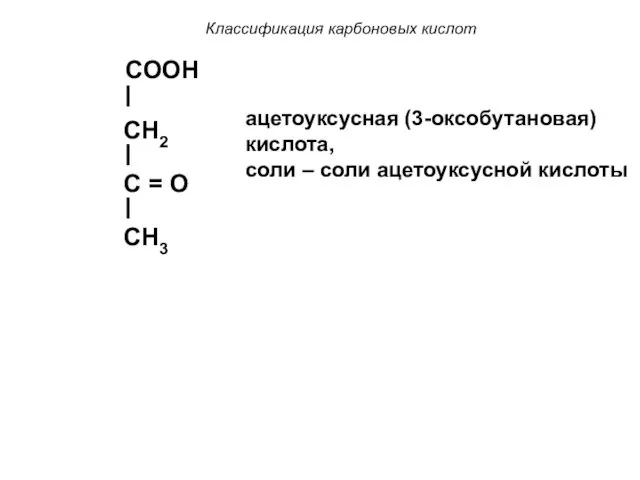
- 16. Классификация карбоновых кислот COOH CH2 C = O CH3 ацетоуксусная (3-оксобутановая) кислота, cоли – соли ацетоуксусной
- 17. Классификация карбоновых кислот III. Особую группу составляют высшие (жирные) карбоновые кислоты (ВЖК); входят в состав липидов.
- 18. b) непредельные. Пример: C17H33COOH – олеиновая кислота (одна двойная связь), C17H31COOH – линолевая кислота (две двойных
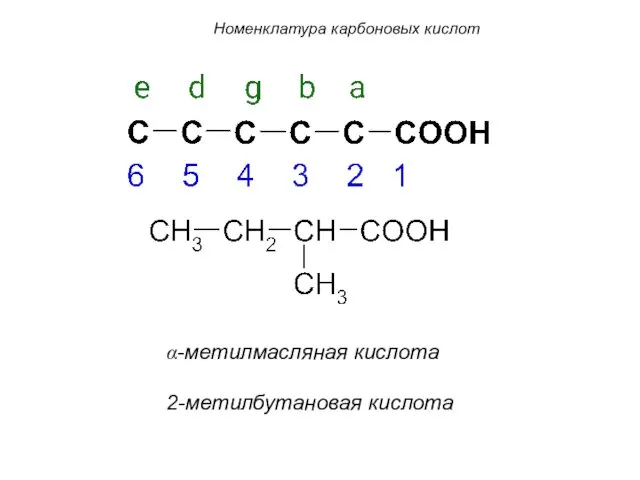
- 19. α-метилмасляная кислота 2-метилбутановая кислота Номенклатура карбоновых кислот
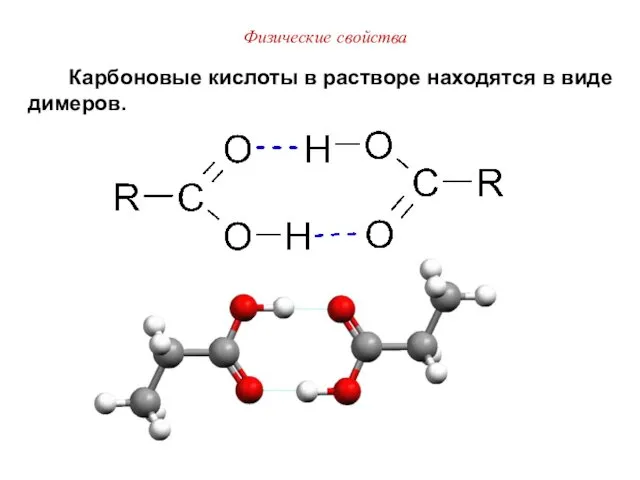
- 20. Физические свойства Карбоновые кислоты в растворе находятся в виде димеров.
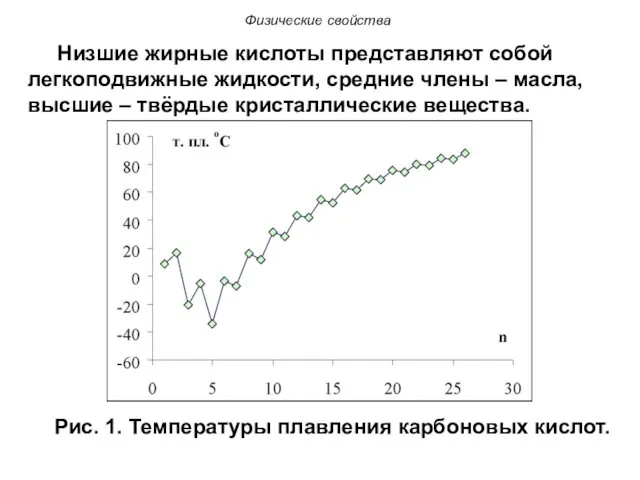
- 21. Физические свойства Низшие жирные кислоты представляют собой легкоподвижные жидкости, средние члены – масла, высшие – твёрдые
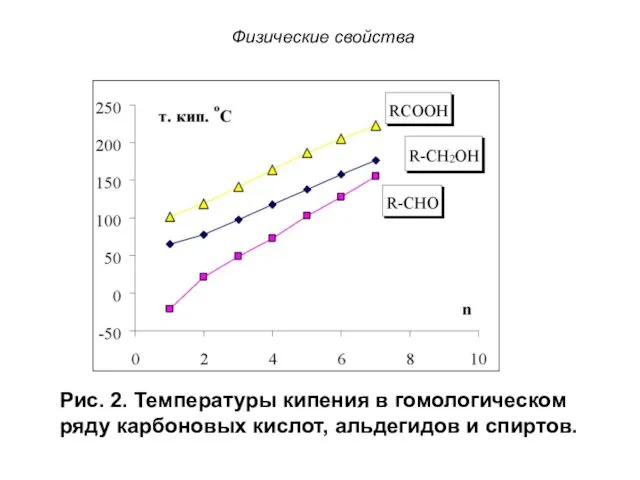
- 22. Физические свойства Рис. 2. Температуры кипения в гомологическом ряду карбоновых кислот, альдегидов и спиртов.
- 23. Физические свойства Первые члены гомологического ряда карбоновых кислот обладают резким запахом, средние – прогорклым, неприятным, например,
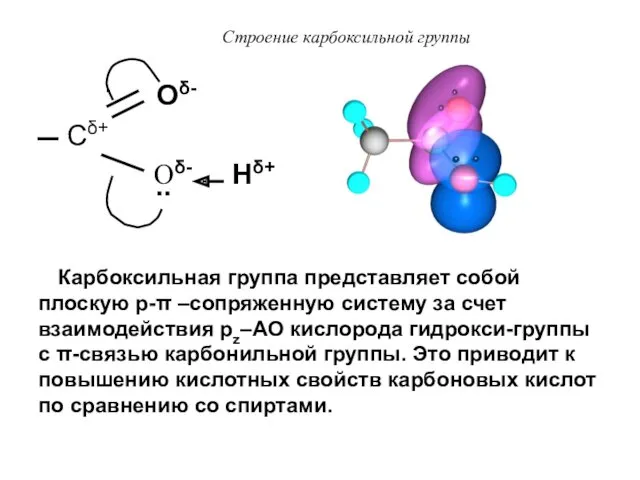
- 24. Строение карбоксильной группы Оδ- Сδ+ Оδ- Нδ+ .. Карбоксильная группа представляет собой плоскую p-π –сопряженную систему
- 25. В карбоновых кислотах частичный положительный заряд на атоме углерода меньше, чем в альдегидах и кетонах, поэтому
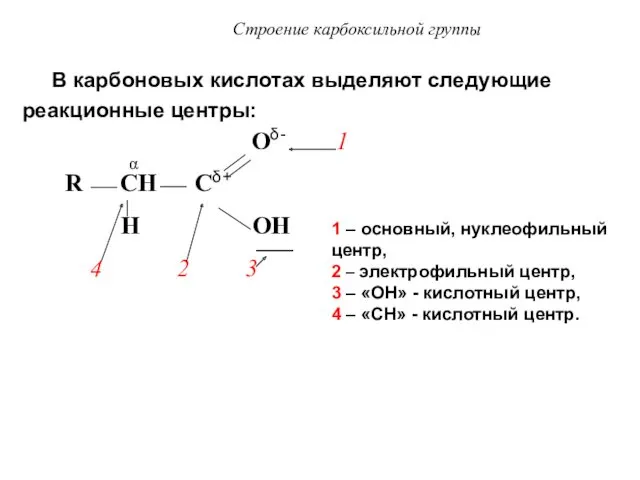
- 26. Строение карбоксильной группы В карбоновых кислотах выделяют следующие реакционные центры: Oδ- 1 R CH Cδ+ H
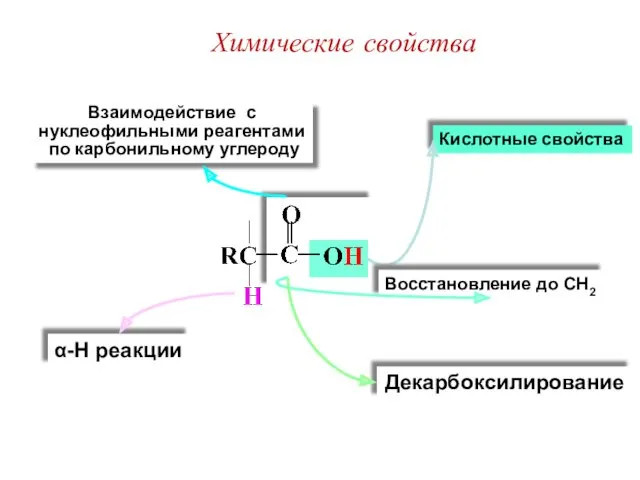
- 27. Кислотные свойства Взаимодействие с нуклеофильными реагентами по карбонильному углероду Восстановление до CH2 Декарбоксилирование α-H реакции Химические
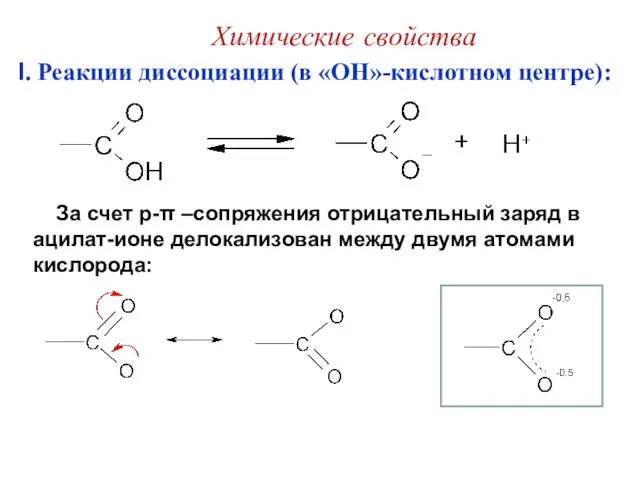
- 28. I. Реакции диссоциации (в «OH»-кислотном центре): За счет p-π –сопряжения отрицательный заряд в ацилат-ионе делокализован между
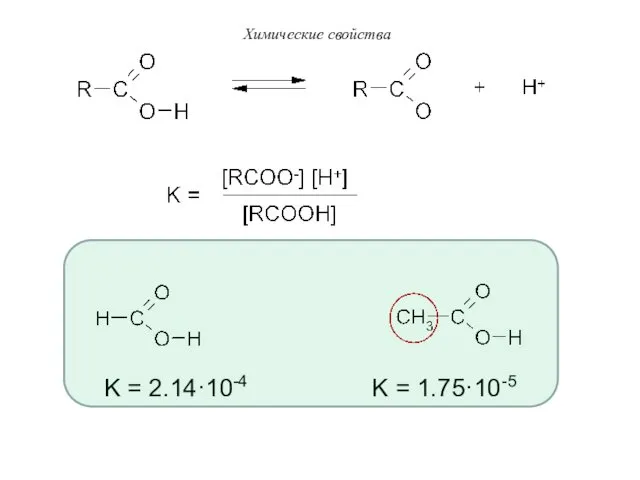
- 29. K = 2.14·10-4 K = 1.75·10-5 Химические свойства
- 30. Химические свойства II. Образование солей: а) С активными металлами: 2 CH3COOH + Mg → (CH3COO)2Mg +
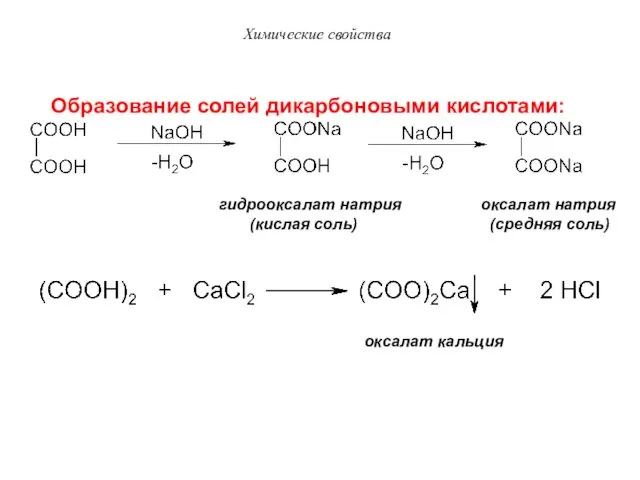
- 31. Образование солей дикарбоновыми кислотами: гидрооксалат натрия оксалат натрия (кислая соль) (средняя соль) оксалат кальция Химические свойства
- 32. Около 80% почечных камней образуется из оксалата кальция. Химические свойства
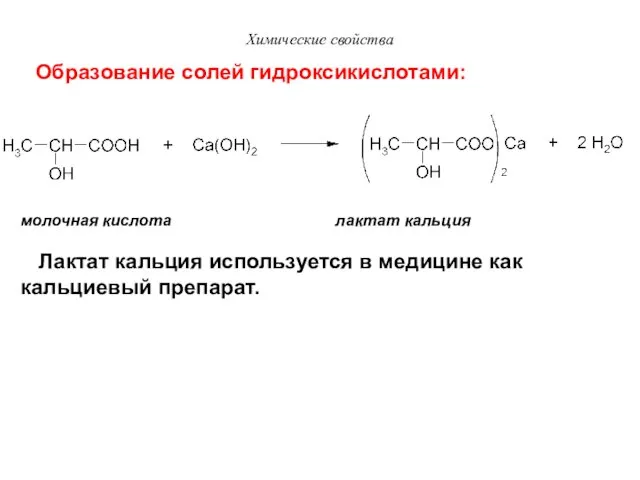
- 33. Химические свойства молочная кислота лактат кальция Образование солей гидроксикислотами: Лактат кальция используется в медицине как кальциевый
- 34. Химические свойства III. Реакции галогенирования (в СН - кислотном центре): CH3 CH2 COOH + Br2 CH3
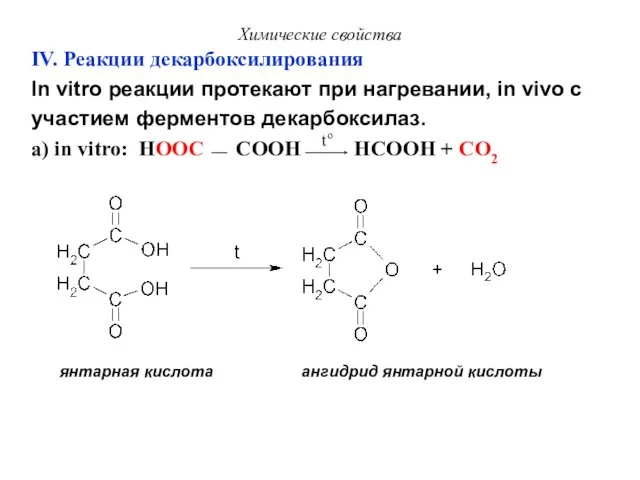
- 35. Химические свойства IV. Реакции декарбоксилирования In vitro реакции протекают при нагревании, in vivo с участием ферментов
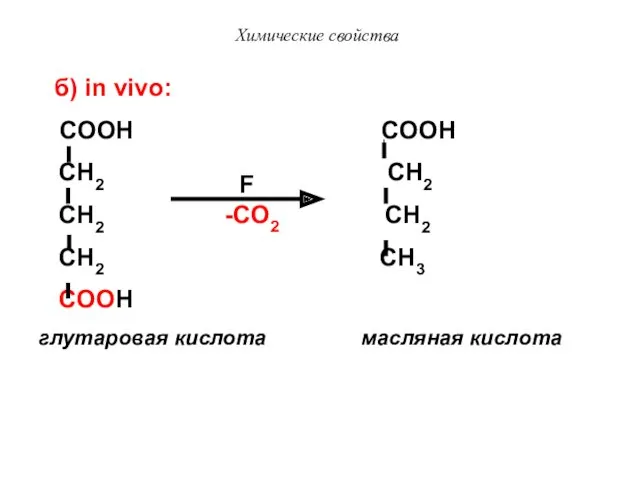
- 36. Химические свойства COOH COOH CH2 CH2 CH2 CH2 CH2 CH3 COOH глутаровая кислота масляная кислота F
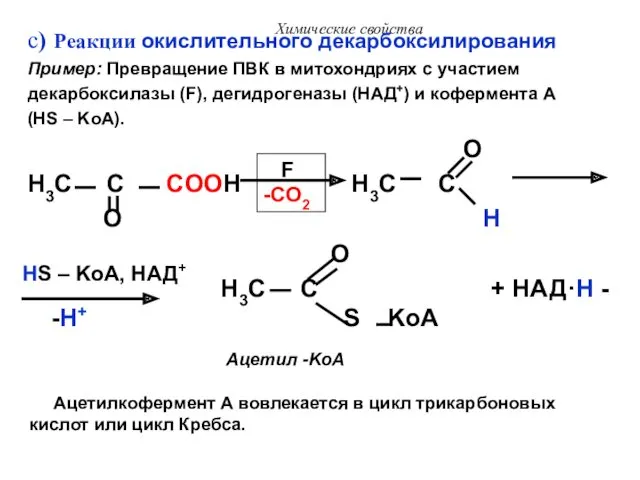
- 37. Химические свойства c) Реакции окислительного декарбоксилирования Пример: Превращение ПВК в митохондриях с участием декарбоксилазы (F), дегидрогеназы
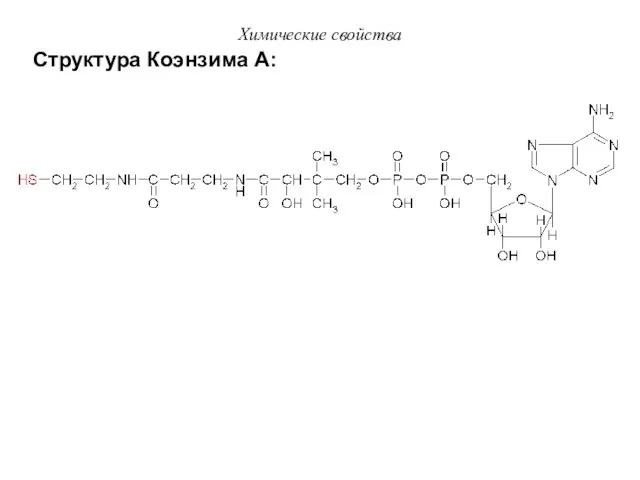
- 38. Структура Коэнзима А: Химические свойства
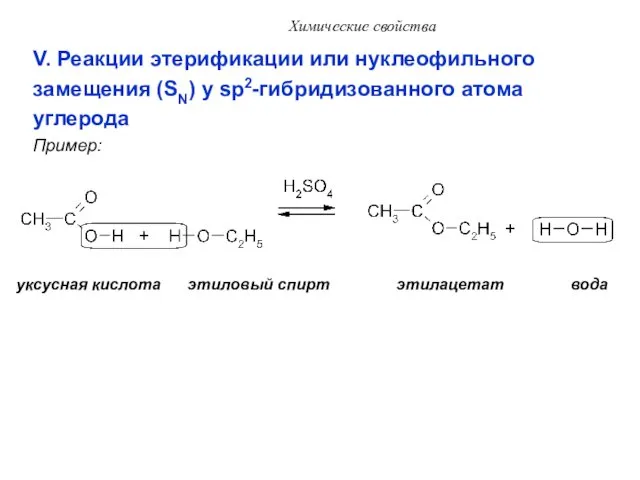
- 39. Химические свойства V. Реакции этерификации или нуклеофильного замещения (SN) у sp2-гибридизованного атома углерода Пример: уксусная кислота
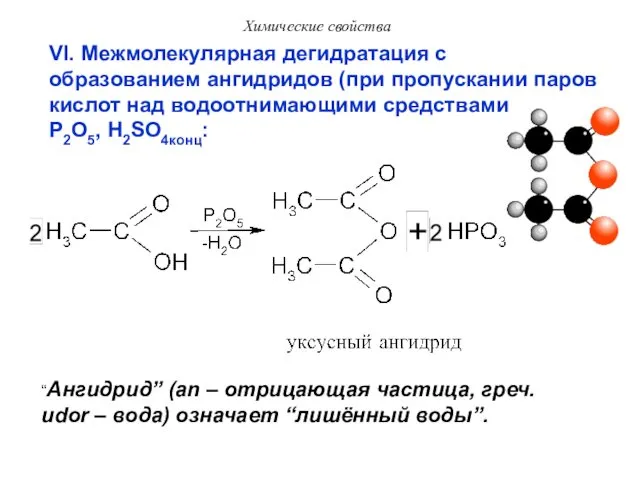
- 40. Химические свойства VI. Межмолекулярная дегидратация с образованием ангидридов (при пропускании паров кислот над водоотнимающими средствами P2O5,
- 41. Химические свойства VII. Окисление карбоновых кислот В организме карбоновые кислоты окисляются в основном за счёт т.н.
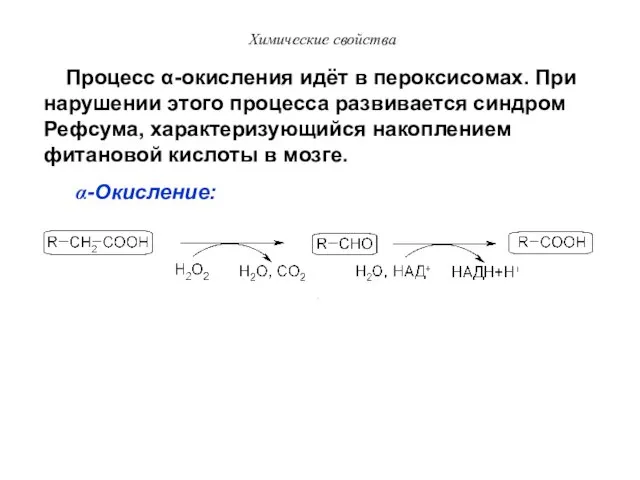
- 42. Химические свойства Процесс α-окисления идёт в пероксисомах. При нарушении этого процесса развивается синдром Рефсума, характеризующийся накоплением
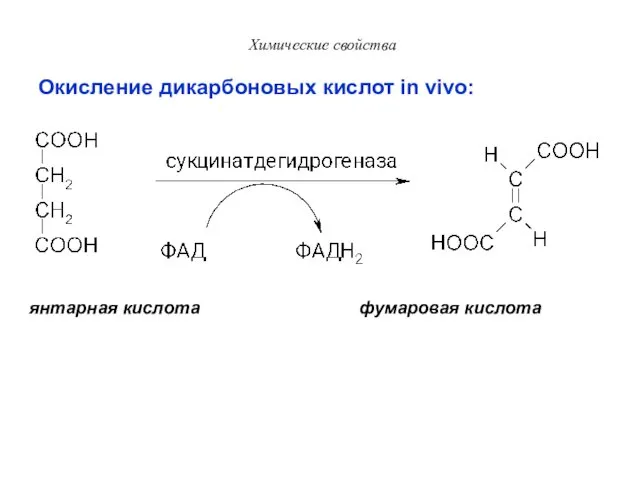
- 43. Химические свойства Окисление дикарбоновых кислот in vivo: янтарная кислота фумаровая кислота
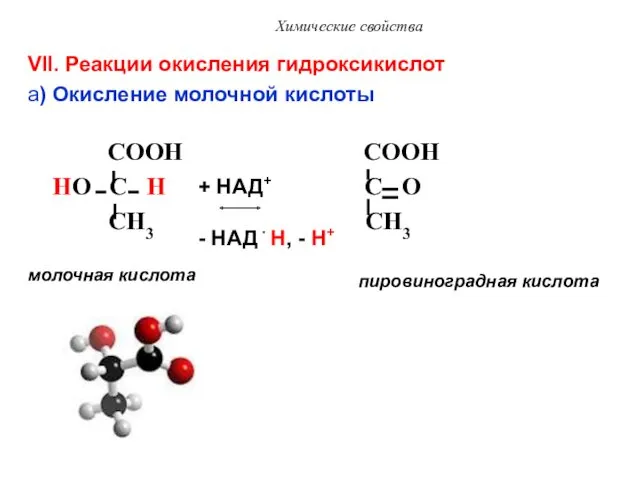
- 44. Химические свойства VII. Реакции окисления гидроксикислот a) Окисление молочной кислоты COOH COOH HO C H C
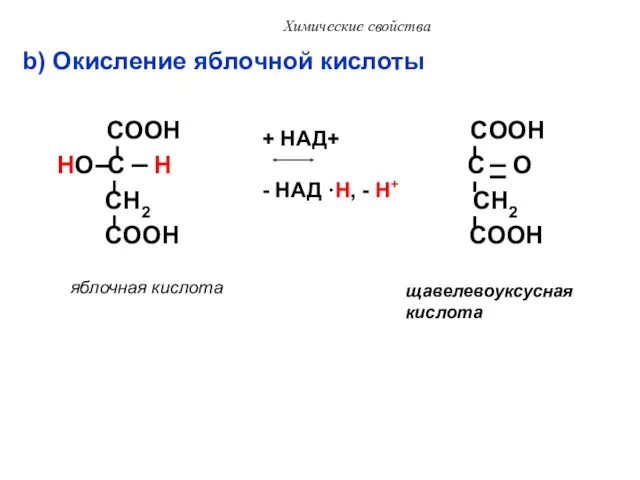
- 45. Химические свойства b) Окисление яблочной кислоты COOH COOH HO C H C O CH2 CH2 COOH
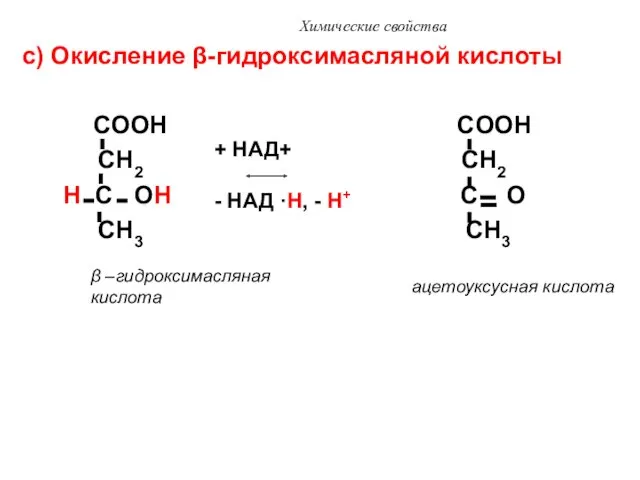
- 46. Химические свойства с) Окисление β-гидроксимасляной кислоты COOH COOH CH2 CH2 H C OH C O CH3
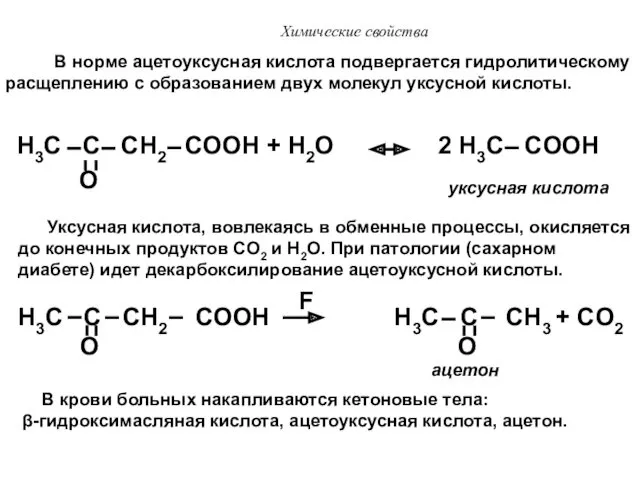
- 47. Химические свойства H3C C CH2 COOH + H2O 2 H3C COOH O В норме ацетоуксусная кислота
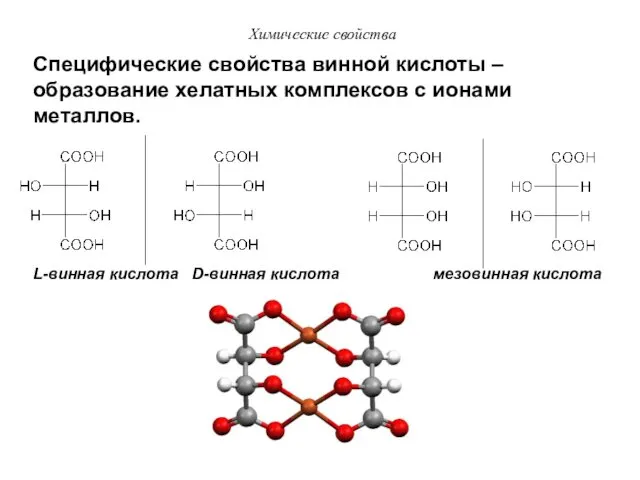
- 48. Химические свойства Специфические свойства винной кислоты – образование хелатных комплексов с ионами металлов. L-винная кислота D-винная
- 49. Салициловая кислота, фарм. препараты на её основе Салициловая кислота: (о-гидроксибензойная кислота) Обладает большей кислотностью, чем бензойная
- 50. Салициловая кислота, фарм. препараты на её основе Салициловая кислота применяется в медицине в виде спиртовых растворов
- 51. Метилсалицилат: Используется как противовоспалительное, анальгетическое средство наружно (в виде мазей). Салициловая кислота, фарм. препараты на её
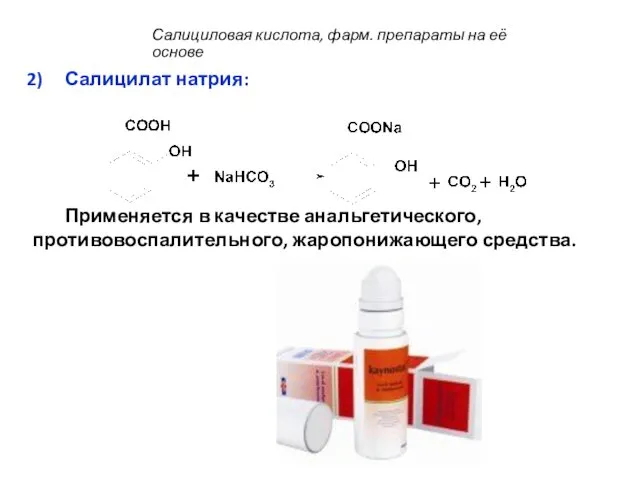
- 52. Салицилат натрия: Применяется в качестве анальгетического, противовоспалительного, жаропонижающего средства. Салициловая кислота, фарм. препараты на её основе
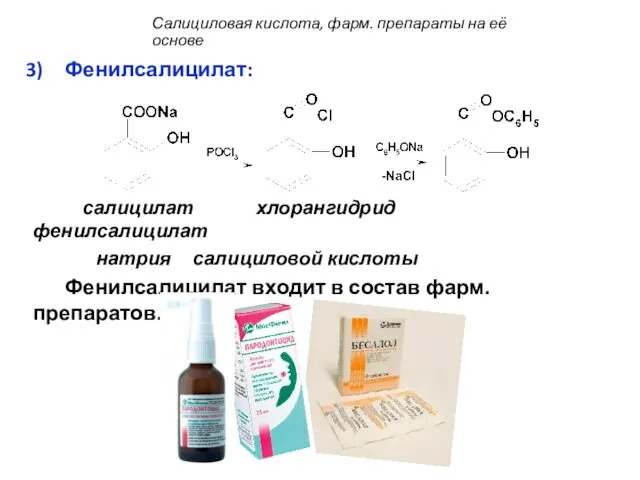
- 53. Фенилсалицилат: салицилат хлорангидрид фенилсалицилат натрия салициловой кислоты Фенилсалицилат входит в состав фарм. препаратов. Салициловая кислота, фарм.
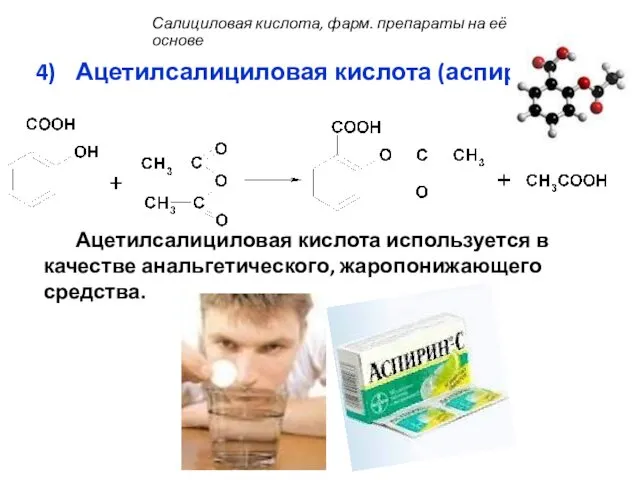
- 54. Ацетилсалициловая кислота (аспирин): Ацетилсалициловая кислота используется в качестве анальгетического, жаропонижающего средства. Салициловая кислота, фарм. препараты на
- 55. Салициловая кислота и её производные со свободной гидроксильной группой дают с раствором хлорида железа (III) фиолетовое
- 57. Скачать презентацию
















 Галогены. Строение атома
Галогены. Строение атома История хроматографии. Виды хроматографических методов
История хроматографии. Виды хроматографических методов Anionic Polymerization
Anionic Polymerization Сложные эфиры. Жиры и масла
Сложные эфиры. Жиры и масла Процессы природного минералообразования. Формы природных выделений минералов
Процессы природного минералообразования. Формы природных выделений минералов Основания, их классификация и свойства в свете теории электролитической диссоциации
Основания, их классификация и свойства в свете теории электролитической диссоциации Растворы
Растворы fosfor_и его соед
fosfor_и его соед Валентность и степень окисления атомов в молекуле
Валентность и степень окисления атомов в молекуле Электролиз. Электролиз раствора и электролиз расплава электролита
Электролиз. Электролиз раствора и электролиз расплава электролита Твердые вещества
Твердые вещества Анализ анионов. Анализ смеси солей
Анализ анионов. Анализ смеси солей Азот, фосфор и их соединения
Азот, фосфор и их соединения Alcohols. Learning Objectives
Alcohols. Learning Objectives Текстуры метаморфических пород
Текстуры метаморфических пород Минералогический состав почв
Минералогический состав почв Aluminium
Aluminium Энергетика химических процессов
Энергетика химических процессов Источники углеводородов
Источники углеводородов Знакомство с лабораторным оборудованием
Знакомство с лабораторным оборудованием Ендотермічні реакції на службі людини
Ендотермічні реакції на службі людини Необоротні і оборотні хімічні процеси. Хімічна рівновага. Принцип Ле Шательє
Необоротні і оборотні хімічні процеси. Хімічна рівновага. Принцип Ле Шательє Устранение жёсткости воды на промышленных предприятиях
Устранение жёсткости воды на промышленных предприятиях Алюминий и его соединения
Алюминий и его соединения Алкени і алкіни
Алкени і алкіни Кристаллография и основы кристаллохимии. Лекция 8
Кристаллография и основы кристаллохимии. Лекция 8 Тұнбалар мен қайнатпаларды алу принциптері
Тұнбалар мен қайнатпаларды алу принциптері Вода. Практическая работа
Вода. Практическая работа