Слайд 2

Понятие
Сахароза – дисахарид из группы олигосахаридов, состоящий из двух моносахаридов: α-глюкозы
и β-фруктозы.
Слайд 3
Строение
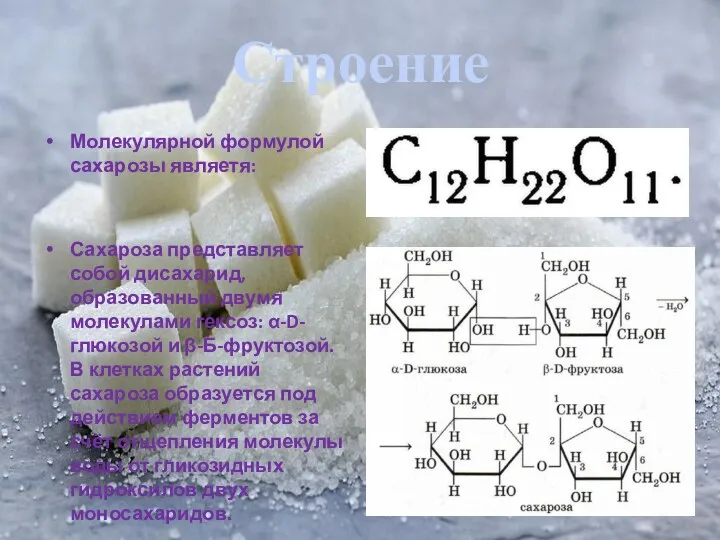
Молекулярной формулой сахарозы являетя:
Сахароза представляет собой дисахарид, образованный двумя молекулами
гексоз: α-D-глюкозой и β-Б-фруктозой. В клетках растений сахароза образуется под действием ферментов за счёт отщепления молекулы воды от гликозидных гидроксилов двух моносахаридов.
Слайд 4

Физические свойства
Сахароза: бесцветные моноклинные кристаллы, сладкие на вкус, t пл =
184-185 С, растворимость (1 грамм=100 грамм): в воде 179(0 С) И 487 (100 С), в этаноле 0,9 (20 С).
Малорастворима в метаноле. Не растворима в диэтиловом эфире. Плотность сахарозы = 1,5879 г/см^3 (15 С). При охлаждении жидким воздухом, после освещения ярким светом кристаллы сахарозы фосфоресцируют.
Слайд 5

Химические свойства
Сахароза имеет более сложное строение, чем глюкоза. Молекула сахарозы состоит
из остатков глюкозы и фруктозы, соединенных друг с другом за счет взаимодействия полуацетальных гидроксилов (1→2)-гликозидной связью:
Наличие гидроксильных групп в молекуле сахарозы легко подтверждается реакцией с гидроксидами металлов.
Если раствор сахарозы прилить к гидроксиду меди (II), образуется ярко-синий раствор сахарата меди (качественная реакция многоатомных спиртов).
Альдегидной группы в сахарозе нет: при нагревании с аммиачным раствором оксида серебра (I) она не дает «серебряного зеркала», при нагревании с гидроксидом меди (II) не образует красного оксида меди (I).
Сахароза, в отличие от глюкозы, не является альдегидом. Сахароза, находясь в растворе, не вступает в реакцию "серебряного зеркала", так как не способна превращаться в открытую форму, содержащую альдегидную группу. Подобные дисахариды не способны окисляться (т.е. быть восстановителями) и называются невосстанавливающими сахарами.
Слайд 6

Химические свойства
Реакция сахарозы с водой.
Важное химическое свойство сахарозы – способность подвергаться
гидролизу (при нагревании в присутствии ионов водорода). При этом из одной молекулы сахарозы образуется молекула глюкозы и молекула фруктозы:
С12Н22О11 + Н2О t, H2SO4→ С6Н12O6 + С6Н12O6
Из числа изомеров сахарозы, имеющих молекулярную формулу С12Н22О11, можно выделить мальтозу и лактозу.
При гидролизе различные дисахариды расщепляются на составляющие их моносахариды за счёт разрыва связей между ними (гликозидных связей):
Таким образом, реакция гидролиза дисахаридов является обратной процессу их образования из моносахаридов.
Слайд 7

Получение
Сахарозу преимущественно получают из сахарной свеклы и сахарного тросника.
Слайд 8

Применение
Сахароза находит многочисленное применение и в первую очередь как пищевой продукт
— сахар. Она также служит в качестве исходного вещества в различных ферментационных процессах получения этилового спирта, глицерина, лимонной кислоты. Применяется также для изготовления лекарств.
Слайд 9

Задача
Сколько граммов сахарозы надо растворить в 250 г воды, чтобы получить
раствор с массовой долей сахарозы 0,3 (30%)?








 Свойства простых веществ в свете ОВР
Свойства простых веществ в свете ОВР Уход за волосами
Уход за волосами Характеристика элементов VIII-Б группы. Семейство железа
Характеристика элементов VIII-Б группы. Семейство железа Маңызды химиялық өндірістер
Маңызды химиялық өндірістер Кислоты
Кислоты Ағзаның барлық жасушасындағы белок алмасу. Аминқышқылдарының дезаминденуі, пурин және пиримидиндердің ыдырауынан
Ағзаның барлық жасушасындағы белок алмасу. Аминқышқылдарының дезаминденуі, пурин және пиримидиндердің ыдырауынан Кристаллы. Кристаллические вещества
Кристаллы. Кристаллические вещества Оксиды, их классификация и свойства (8 класс)
Оксиды, их классификация и свойства (8 класс) Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции Понятия и определения химической термодинамики. (Лекция 11)
Понятия и определения химической термодинамики. (Лекция 11) Карбоновые кислоты. Классификация карбоновых кислот
Карбоновые кислоты. Классификация карбоновых кислот Тотығутотықсыздану титрлеу әдістері. Дәріс № 7
Тотығутотықсыздану титрлеу әдістері. Дәріс № 7 Кремний и его соединения
Кремний и его соединения Фенол. Состав молекулы фенола
Фенол. Состав молекулы фенола История хроматографии. Виды хроматографических методов
История хроматографии. Виды хроматографических методов Склад і основні фізико-хімічні властивості молочного білку
Склад і основні фізико-хімічні властивості молочного білку Обмен липидов
Обмен липидов Oxygen, O2
Oxygen, O2 Изомеры – это вещества, имеющие одинаковый состав
Изомеры – это вещества, имеющие одинаковый состав Химическое равновесие
Химическое равновесие Оксиды. Номенклатура, классификация, физические свойства
Оксиды. Номенклатура, классификация, физические свойства Хімічні властивості карбонових кислот
Хімічні властивості карбонових кислот Альдегиды, свойства, получение, применение
Альдегиды, свойства, получение, применение Основы коррозии и защиты металлов. Методы исследования коррозии
Основы коррозии и защиты металлов. Методы исследования коррозии Углеводы. Молекулярные формулы
Углеводы. Молекулярные формулы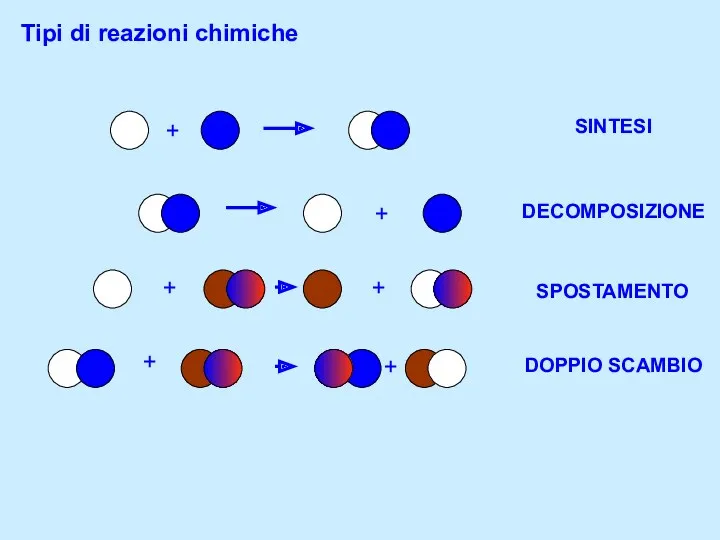 Tipi di reazioni chimiche
Tipi di reazioni chimiche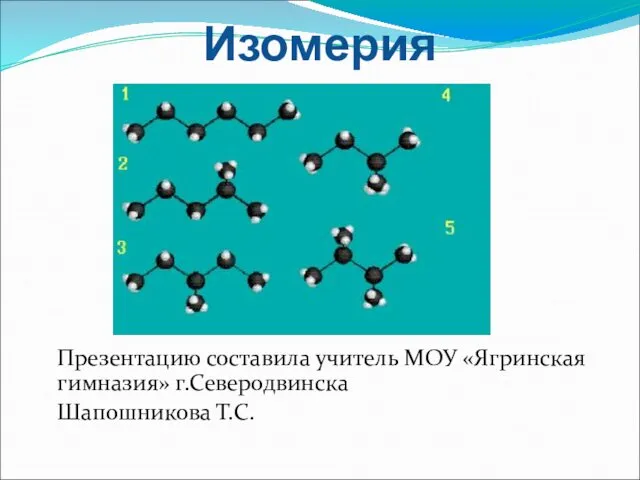 Изомерия и ее виды
Изомерия и ее виды Диссоциация электролитов
Диссоциация электролитов