Слайд 2

Состав молекулы фенола: С6Н5ОН
Фенол рассматривают как производное бензола, в котором один
атом водорода замещён на группу –ОН.
Структурная формула фенола:
СН
СН С–О–Н
СН СН
СН
Слайд 3

Физические свойства фенола
Фенол – твёрдое вещество (с характерным запахом).
Высокие температуры кипения
и плавления фенола объясняются наличием межмолекулярных водородных связей, которые прочнее, чем между молекулами предельных одноатомных спиртов.
Слайд 4
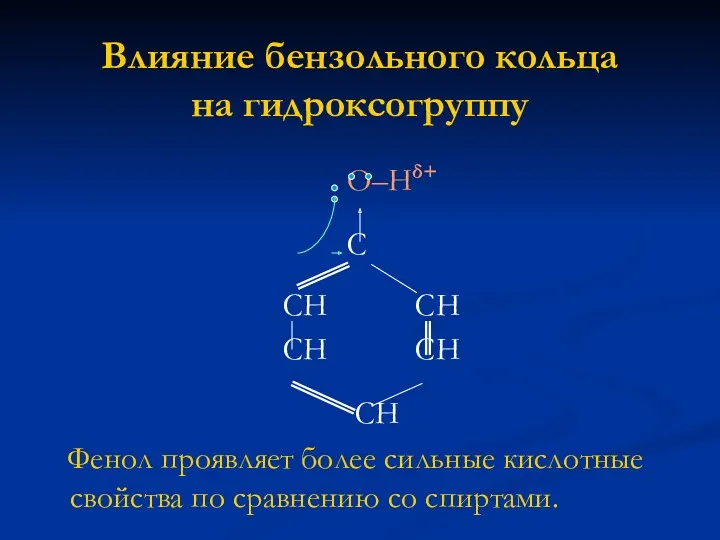
Влияние бензольного кольца на гидроксогруппу
О–Нδ+
С
СН СН
СН СН
СН
Фенол проявляет более сильные кислотные свойства по сравнению со спиртами.
Слайд 5

Кислотные свойства фенола
1. Взаимодействие с активными металлами:
2С6Н5–ОН + 2Na →
2С6Н5–ОNa + H2
фенолят натрия
2. Взаимодействие с основаниями:
С6Н5–ОН + NaОН → С6Н5–ОNa + H2О
фенолят натрия
3. Взаимодействие с солями:
с FeCl3 → комплексное соединение
(сине-фиолетовый раствор)
Слайд 6
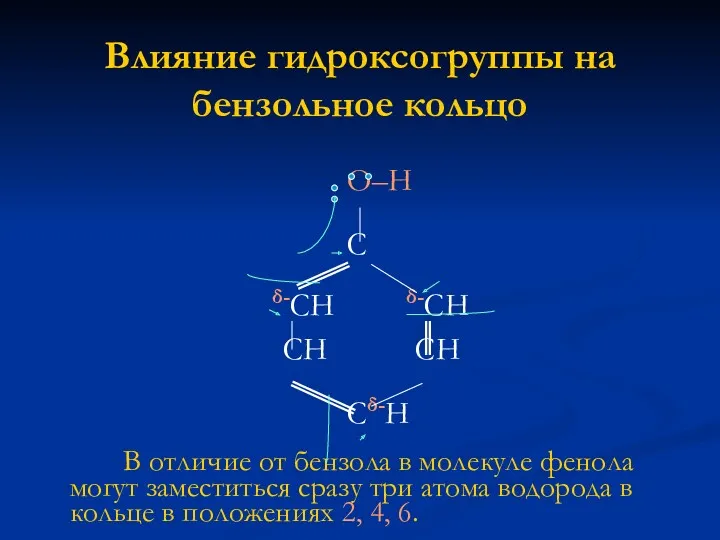
Влияние гидроксогруппы на бензольное кольцо
О–Н
С
δ-СН δ-СН
СН СН
Сδ-Н
В отличие от бензола в молекуле фенола могут заместиться сразу три атома водорода в кольце в положениях 2, 4, 6.
Слайд 7
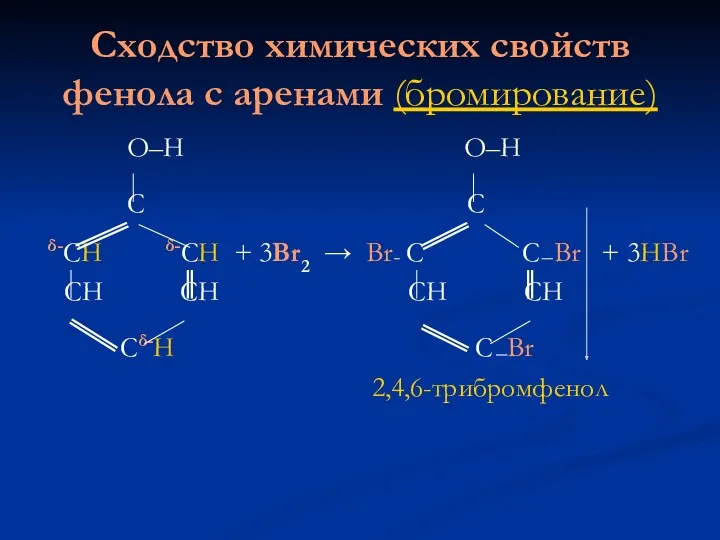
Сходство химических свойств фенола с аренами (бромирование)
О–Н О–Н
С С
δ-СН δ-СН + 3Br2 → Br С С Br + 3HBr
СН СН СН СН
Сδ-Н С Br
2,4,6-трибромфенол
Слайд 8
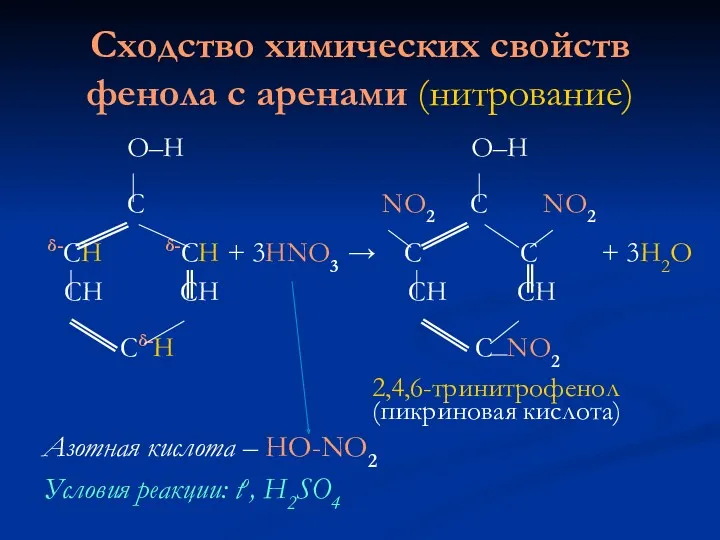
Сходство химических свойств фенола с аренами (нитрование)
О–Н О–Н
С NO2
С NO2
δ-СН δ-СН + 3HNO3 → С С + 3H2O
СН СН СН СН
Сδ-Н С NO2
2,4,6-тринитрофенол
(пикриновая кислота)
Азотная кислота – HO-NO2
Условия реакции: tо, H2SO4
Слайд 9

Слайд 10









 Биогенді (s.p.d) элементтермен олардың қосылыстарының медициналық және биологиялық маңызы
Биогенді (s.p.d) элементтермен олардың қосылыстарының медициналық және биологиялық маңызы Кислоты, их состав и названия
Кислоты, их состав и названия Карбоновые кислоты и их функциональные производные
Карбоновые кислоты и их функциональные производные Ароматические углеводороды
Ароматические углеводороды Гетерофазный катализ. (Лекция 20)
Гетерофазный катализ. (Лекция 20) Горение топлива
Горение топлива Використання радіоактивних ізотопів, як індикаторів у тваринництві і археології
Використання радіоактивних ізотопів, як індикаторів у тваринництві і археології Основные классы неорганических соединений
Основные классы неорганических соединений Соли, их классификация и свойства
Соли, их классификация и свойства Органічна хімія
Органічна хімія Розв’язування задач за рівняннями реакцій з використанням розчинів із певною масовою часткою розчиненої речовини. Урок 13-14
Розв’язування задач за рівняннями реакцій з використанням розчинів із певною масовою часткою розчиненої речовини. Урок 13-14 Жёсткость воды
Жёсткость воды Полисахариды: крахмал и целлюлоза
Полисахариды: крахмал и целлюлоза Растворы. Часть 2. Лекция №7
Растворы. Часть 2. Лекция №7 Химия атмосферы. Химические процессы в тропосфере
Химия атмосферы. Химические процессы в тропосфере Буферные системы
Буферные системы Белки. Строение
Белки. Строение Классификация химических элементов. Составитель. 8 класс
Классификация химических элементов. Составитель. 8 класс Минералы для ИЗБ
Минералы для ИЗБ Концентрация растворов. Массовая доля растворенного вещества. Урок 1
Концентрация растворов. Массовая доля растворенного вещества. Урок 1 Химический элемент медь
Химический элемент медь Кинетика химических реакций
Кинетика химических реакций Кремний и его соединения
Кремний и его соединения Галогены. Расположите галогены в порядке их открытия
Галогены. Расположите галогены в порядке их открытия Важнейшие реакции в органической химии
Важнейшие реакции в органической химии Технология производства аминоальдегидных смол
Технология производства аминоальдегидных смол Углерод. Физические и химические свойства
Углерод. Физические и химические свойства Гидролиз солей
Гидролиз солей