Содержание
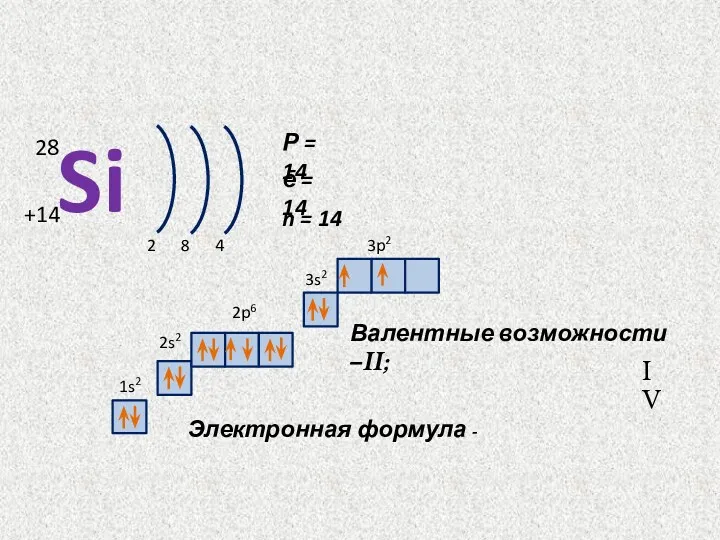
- 2. Si +14 28 2 Р = 14 ē = 14 n = 14 8 4 1s2
- 3. Природные соединения кремния опал халцедон Горный хрусталь песок яшма
- 4. Речной песок, кварцевый песок, кремнезем – SiO2
- 5. Кристалл кварца
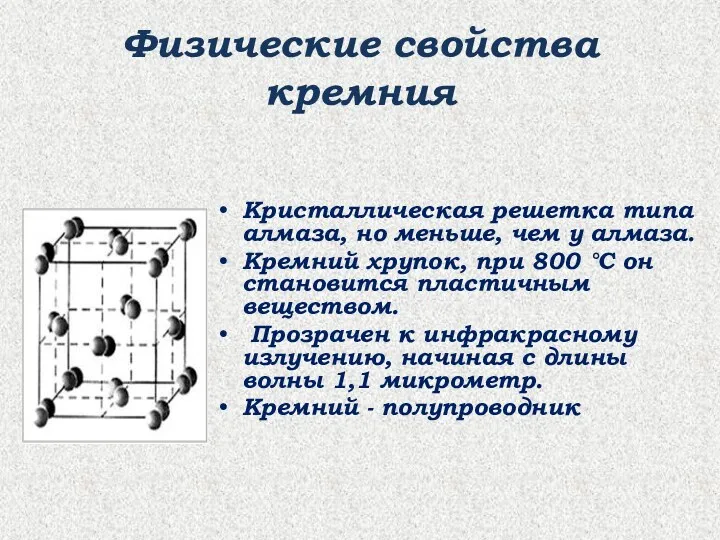
- 6. Физические свойства кремния Кристаллическая решетка типа алмаза, но меньше, чем у алмаза. Кремний хрупок, при 800
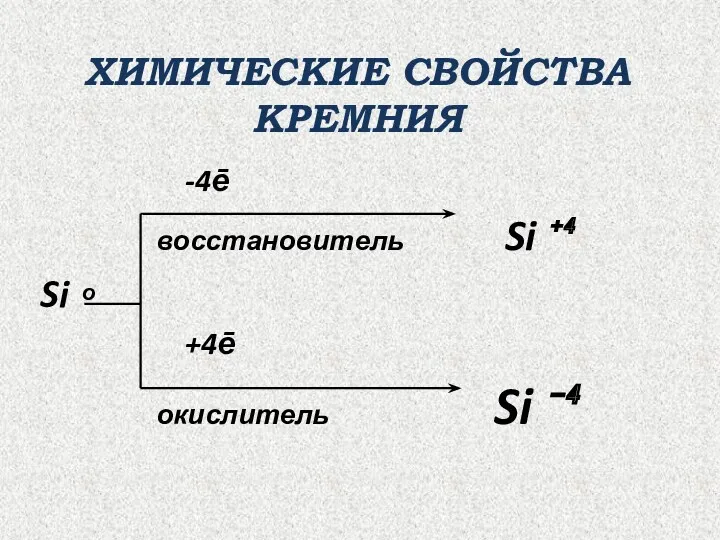
- 7. ХИМИЧЕСКИЕ СВОЙСТВА КРЕМНИЯ -4ē восстановитель Si ⁺⁴ Si ͦ +4ē окислитель Si ⁻⁴
- 8. O2 Si + = SiO2 2Cl2 Si + = SiCl4 C Si + = SiC 2F2
- 9. ОКСИД КРЕМНИЯ (IV) КИСЛОТНЫЕ СВОЙСТВА SiO2 + H2O = SiO2 + CaO = CaSiO3 SiO2 +
- 10. СИЛАН Получение силана Mg2Si + 4H2O = SiH4 + 2Mg(ОH) 2 Горение силана SiH4 + 2О2
- 11. КРЕМНИЕВАЯ КИСЛОТА Получение Na2SiO3 + 2HCl = H2SiO3 + 2NaCl 2Na+ + SiO3 2 – +
- 12. Применение кремния Кремний — основной материал для электроники и солнечной энергетики. Кремний — материал для зеркал
- 13. ПРИМЕНЕНИЕ СОЕДИНЕНИЙ КРЕМНИЯ Силикатный клей Кремнийорганический полимер - силикон
- 14. Солнечные батареи В качестве материала для производства солнечных элементов сегодня используется кремний. Извлечь из песка чистый
- 15. Солнечные батареи — один из основных способов получения электрической энергии на космических аппаратах
- 16. КАРБОРУНД Используют для шлифовальных кругов, наждачной бумаги, абразивных порошков, полировальных составов, а также в огнеупорных блоках
- 17. Продукты силикатной промышленности стекло кирпич бетон
- 18. Биологическая роль кремния Кремний в больших количествах концентрируют морские организмы —диатомовые водоросли, радиолярии, губки. Много кремния
- 20. Скачать презентацию














 Удивительные свойства воды
Удивительные свойства воды Electronică aplicată. (Curs 2)
Electronică aplicată. (Curs 2) Пространственное строение органических соединений. (Лекция 2)
Пространственное строение органических соединений. (Лекция 2) 20230416_urok_na_20.02.2023
20230416_urok_na_20.02.2023 Неізогіпсичні перетворення функціональних груп. Реакції окиснення
Неізогіпсичні перетворення функціональних груп. Реакції окиснення Виды присадок к моторным топливам. Присадки к дизельному топливу
Виды присадок к моторным топливам. Присадки к дизельному топливу Электронная конфигурация К. Классификация химических элементов. 8 класс
Электронная конфигурация К. Классификация химических элементов. 8 класс Спирты. Физические и химические свойства
Спирты. Физические и химические свойства Сучасні методи органічного синтезу. Ізогіпсичні перетворення функціональних груп. Реакції приєднання. Гідроборування
Сучасні методи органічного синтезу. Ізогіпсичні перетворення функціональних груп. Реакції приєднання. Гідроборування 20230321_obobshchenie_po_elektroliticheskoy_dissotsiatsii
20230321_obobshchenie_po_elektroliticheskoy_dissotsiatsii Классификация органических соединений, углеводородов
Классификация органических соединений, углеводородов Типовые процессы технологии неорганических веществ. (Тема 3)
Типовые процессы технологии неорганических веществ. (Тема 3) ЕГЭ Химия. Задание №5
ЕГЭ Химия. Задание №5 Изучение строения и свойств глюкозы
Изучение строения и свойств глюкозы Железо и его соединения
Железо и его соединения Химические превращения веществ
Химические превращения веществ Белки. Функции белков
Белки. Функции белков Високомолекулярні сполуки. Полімери
Високомолекулярні сполуки. Полімери Простые спектры 1Н ЯМР
Простые спектры 1Н ЯМР Значення хімічних процесів у природі
Значення хімічних процесів у природі Реакції йонного обміну між електролітами у водних розчинах. Практична робота №1. 9 клас
Реакції йонного обміну між електролітами у водних розчинах. Практична робота №1. 9 клас Реакции ионного обмена
Реакции ионного обмена Жиры. Мыла. 10 класс
Жиры. Мыла. 10 класс Группа редкоземельных элементов
Группа редкоземельных элементов Аммиак. № 12 зертханалық тәжірибе Аммиак молекуласының моделі
Аммиак. № 12 зертханалық тәжірибе Аммиак молекуласының моделі Железо
Железо Crystallography. Part 4: Crystal Forms Twinning
Crystallography. Part 4: Crystal Forms Twinning Функциональные производные с простой связью C-“Э. Галогенпроизводные. (Лекция 5)
Функциональные производные с простой связью C-“Э. Галогенпроизводные. (Лекция 5)