Содержание
- 2. Термодинамические свойства разделяют на экстенсивные, которые пропорциональны массе системы (например, объем, теплоемкость, внутренняя энергия) и интенсивные,
- 3. Если к системе подвести какое-либо количество тепла, то оно пойдет на изменение внутренней энергии системы и
- 4. Закон Гесса. Тепловой эффект химической реакции Тепловым эффектом химической реакции называют количество теплоты, которое выделяется (поглощается)
- 5. Зависимость теплового эффекта реакции от температуры. Уравнения Кирхгоффа Для расчетов необходимо знать значения теплоемкостей при различных
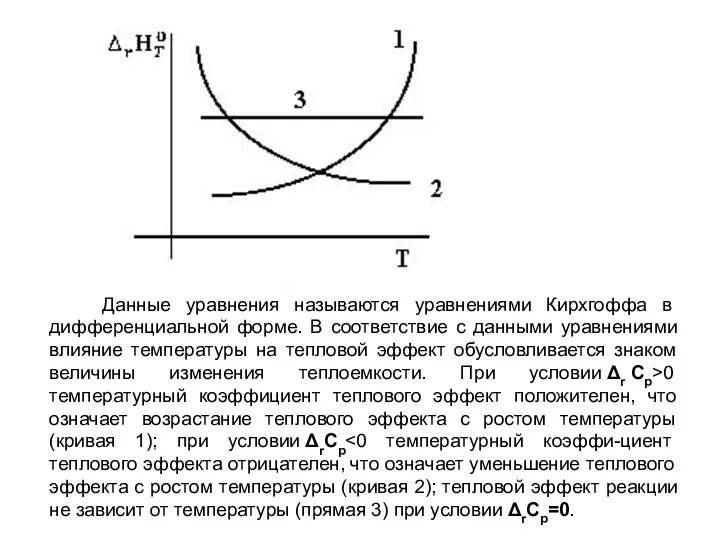
- 6. Данные уравнения называются уравнениями Кирхгоффа в дифференциальной форме. В соответствие с данными уравнениями влияние температуры на
- 7. Первый закон термодинамики позволяет составлять энергетические балансы термодинамических процессов, но не позволяет судить о возможности или
- 8. Если неравновесный процесс протекает в изолированной системе, то δQ = 0, U = const, V =
- 9. Третий закон термодинамики. Абсолютное значение энтропии Предположим, что какое-либо вещество при абсолютном нуле находится в виде
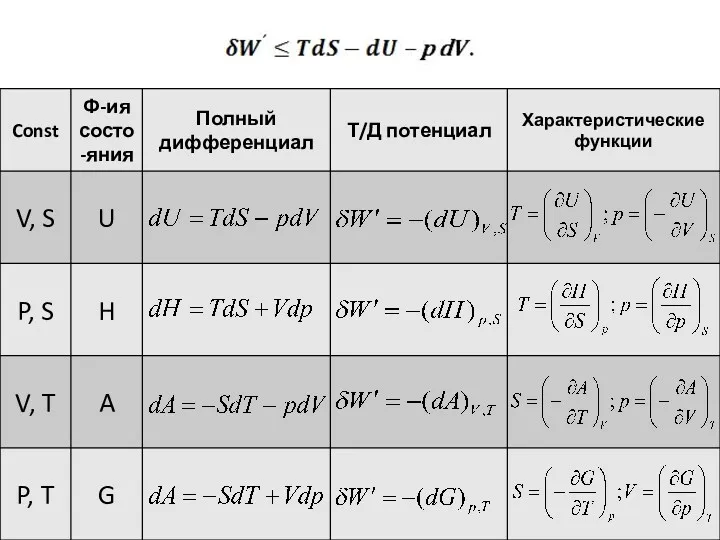
- 10. Термодинамические потенциалы. Характеристические функции На основании математических выражений первого и второго законов термодинамики можно получить следующее
- 12. Если в изолированной системе критерием направленности самопроизвольного процесса и равновесия является изменение энтропии, то в закрытых
- 13. При протекании многих процессов количества веществ в системе изменяются. Это происходит, например, при фазовых превращениях или
- 14. Химическое равновесие. Закон действующих масс Подставим выражение в уравнение для изменения энергии Гиббса : В момент
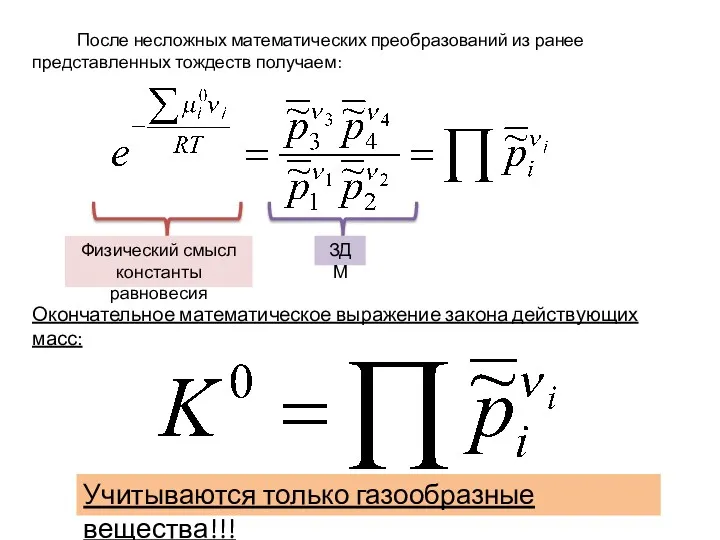
- 15. После несложных математических преобразований из ранее представленных тождеств получаем: Окончательное математическое выражение закона действующих масс: Физический
- 16. Практические константы изменение числа моль газообразных веществ в ходе одного пробега реакции.
- 17. Уравнения изотермы и изобары химической реакции (Для реакции ) Если реакция совершила один пробег при постоянных
- 18. Из уравнения Вант-Гоффа следует, что если соблюдается соотношение то изменение энергии Гиббса имеет отрицательное значение, и
- 19. Для оценки влияния температуры на химическое равновесие продифференцируем уравнение изотермы по температуре при постоянстве давления: Подставим
- 20. Согласно полученному уравнению влияние температуры на равновесие определяется знаком теплового эффекта. Если реакция экзотермическая, то есть
- 21. Влияние давление на равновесие химической реакции Влияние давление на равновесие химической реакции можно рассмотреть, используя уравнение
- 22. Иногда в реакционную систему вводят добавки инертного газа. Для анализа влияния этой добавки можно использовать следующее
- 24. Скачать презентацию


















 Химиялық реакцияның жылдамдығы
Химиялық реакцияның жылдамдығы Оттекті органикалық қосылыстар тақырыбын пәнаралық байланыс арқылы оқыту әдістемесі
Оттекті органикалық қосылыстар тақырыбын пәнаралық байланыс арқылы оқыту әдістемесі Спирт. Спирты в природе. Влияние спирта на человека
Спирт. Спирты в природе. Влияние спирта на человека Побочная подгруппа. 8 группы
Побочная подгруппа. 8 группы Свойства растворов высокомолекулярных соединений
Свойства растворов высокомолекулярных соединений Твердость минералов и их применение
Твердость минералов и их применение Липиды; классификация; строение; значение для жизнедеятельности организмов
Липиды; классификация; строение; значение для жизнедеятельности организмов Функциональные производные углеводородов. Галогенопроизводные углеводородов
Функциональные производные углеводородов. Галогенопроизводные углеводородов Элементы пятой-А группы. Азот и фосфор
Элементы пятой-А группы. Азот и фосфор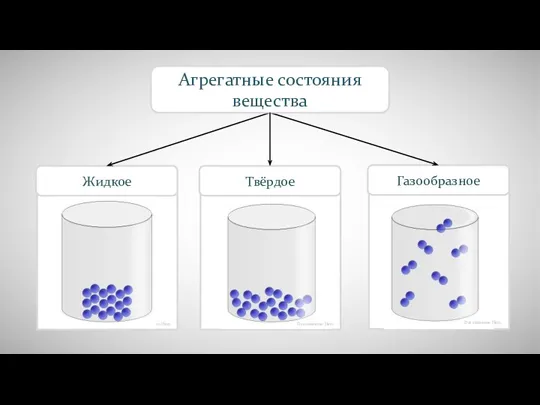 Агрегатные состояния вещества
Агрегатные состояния вещества Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы
Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы Сложные углеводы. Олигосахариды и полисахариды
Сложные углеводы. Олигосахариды и полисахариды Химиялық өнеркәсіп
Химиялық өнеркәсіп Ізомери у природі
Ізомери у природі Азот и его соединения
Азот и его соединения Ауыл шаруашылығындағы пестицидтер
Ауыл шаруашылығындағы пестицидтер Феноли (бензенол)
Феноли (бензенол) c0198e3edf1db804a5527004a7864ed1
c0198e3edf1db804a5527004a7864ed1 Основания
Основания Роль металлов в истории человеческой цивилизации
Роль металлов в истории человеческой цивилизации Титан және оның қорытпалары. Титанның физика-химиялық қасиеттері
Титан және оның қорытпалары. Титанның физика-химиялық қасиеттері Основы химической термодинамики
Основы химической термодинамики Основная. Первоначальные представления об органических веществах
Основная. Первоначальные представления об органических веществах Строение и свойства углеводов и липидов
Строение и свойства углеводов и липидов Жёсткость воды и способы её устранения
Жёсткость воды и способы её устранения Анализ галогенидов щелочных металлов
Анализ галогенидов щелочных металлов Металлы. Общие свойства и получение
Металлы. Общие свойства и получение Правила ДСС
Правила ДСС