Содержание
- 2. Высокомолекулярные соединения… … вещества, молекулярная масса которых, по данным одних авторов составляет от 104 до 106
- 3. Сходства и различия растворов ВМС и коллоидных растворов
- 4. Растворы ВМС … … лиофильные коллоидные системы, термодинамически устойчивы; … молекулярнодисперсные системы, в которых взвешенными частицами
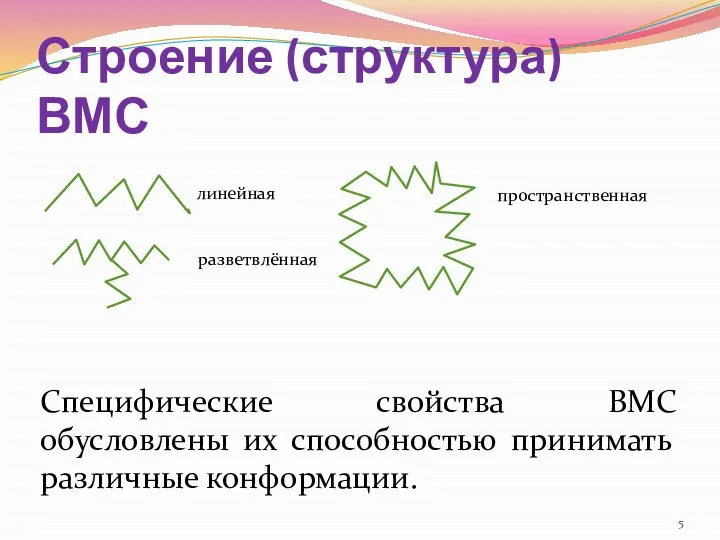
- 5. Строение (структура) ВМС линейная разветвлённая пространственная Специфические свойства ВМС обусловлены их способностью принимать различные конформации.
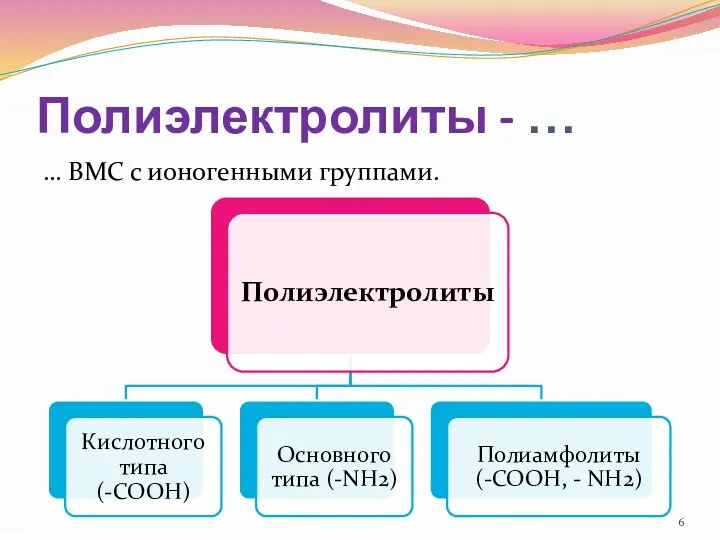
- 6. Полиэлектролиты - … … ВМС с ионогенными группами.
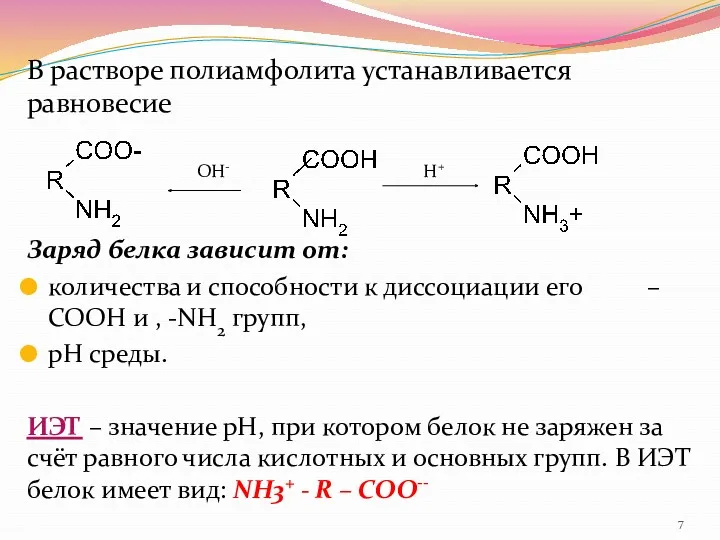
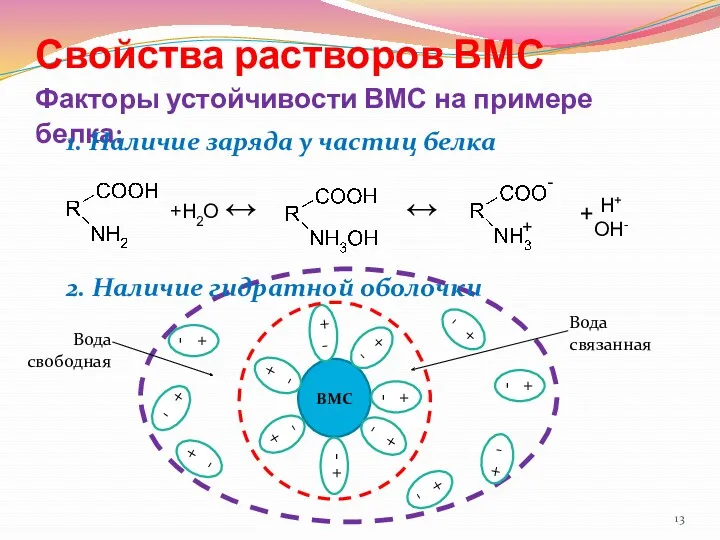
- 7. В растворе полиамфолита устанавливается равновесие Заряд белка зависит от: количества и способности к диссоциации его –СООН
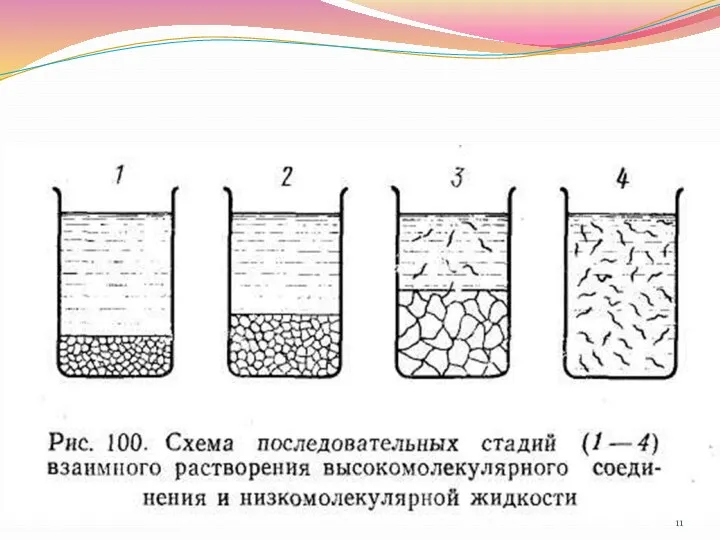
- 8. Особенности растворения ВМС Взаимодействие ВМС с водой начинается с процесса набухания. Набухание – самопроизвольный процесс поглощения
- 9. Ограниченное набухание Сопровождается образованием студня. Студень – пространственная сетка из цепей макромолекул, заполненная НМС. Оно характерно
- 10. Неограниченное набухание Ведёт к растворению ВМС.
- 12. Количественная оценка набухания Степень набухания где m0, V0 – масса и объём ВМС до набухания. m,
- 13. Свойства растворов ВМС Факторы устойчивости ВМС на примере белка: 1. Наличие заряда у частиц белка 2.
- 14. Пути коагуляции растворов ВМС К коагуляции растворов приводит: одновременная нейтрализация заряда частицы ВМС и полное разрушение
- 15. Высаливание… …нарушение устойчивости растворов ВМС при действии неорганических солей. Высаливающее действие соли заключается в её собственной
- 16. ГОФМЕЙСТЕРА РЯДЫ - последовательность, в которую могут быть расположены различные анионы или катионы по силе своего
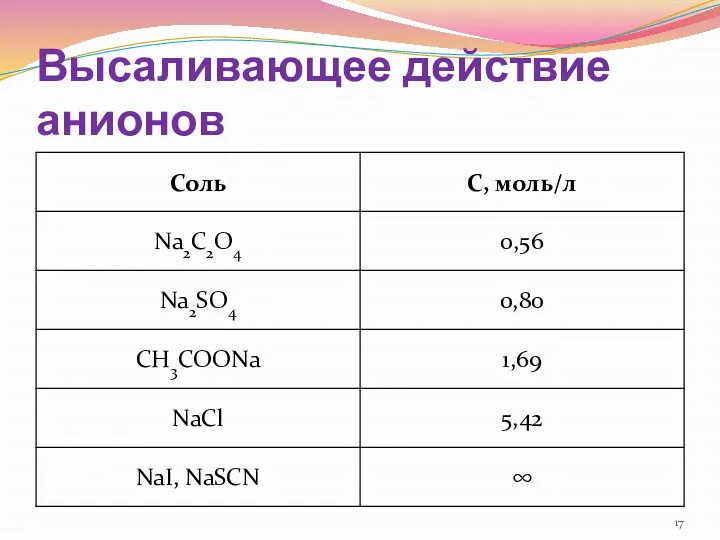
- 17. Высаливающее действие анионов
- 18. Ряды Гофмейстера C2O42- > SO42- > CH3COO- > Cl- > NO3- > I- > SCN- высаливающее
- 19. Большое влияние на процесс высаливания оказывает длина макромолекулы и молекулярная масса ВМС: чем они больше, тем
- 20. Застудневание растворов ВМС - переход растворов к нетекучей, эластичной форме.
- 21. Основу студня составляет пространственная сетка из цепей полимера, заполненная молекулами НМС. Студни со слабыми связями (водородными
- 23. Скачать презентацию














 Комплексные соединения
Комплексные соединения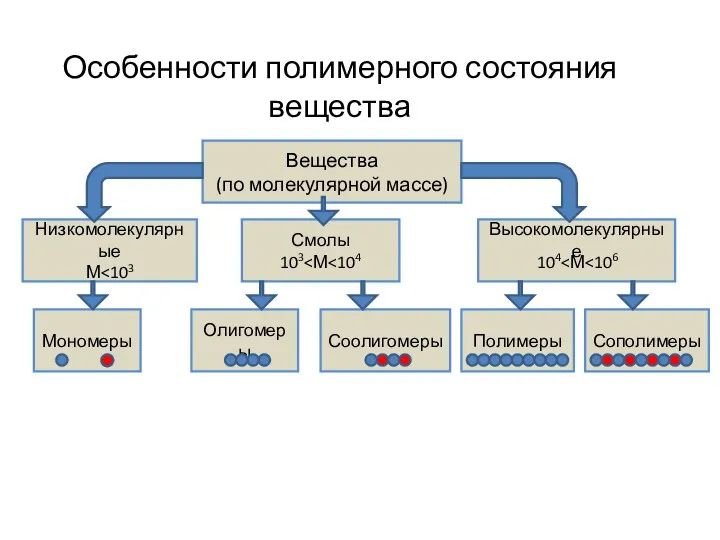 Особенности полимерного состояния вещества
Особенности полимерного состояния вещества Бинарные соединения АхБу. Номенклатура бинарных соединений
Бинарные соединения АхБу. Номенклатура бинарных соединений Каменный уголь. Фенол
Каменный уголь. Фенол Металдар. металдардың периодтық жүйедегі орны. Металдардың құрылысы
Металдар. металдардың периодтық жүйедегі орны. Металдардың құрылысы Аналитическая химия
Аналитическая химия Алкадиены
Алкадиены Химия 20 века
Химия 20 века Коррозия металлов
Коррозия металлов Акриловые волокна
Акриловые волокна Синтетичні волокна
Синтетичні волокна ОСНОВАНИЯ, ИХ КЛАССИФИКАЦИЯ И СВОЙСТВА
ОСНОВАНИЯ, ИХ КЛАССИФИКАЦИЯ И СВОЙСТВА Кислород. Общая характеристика, получение и свойства
Кислород. Общая характеристика, получение и свойства Электролиз
Электролиз Кислород и озон
Кислород и озон Получение и приминение этилена
Получение и приминение этилена Происхождение рибосомы, белкового синтеза и генетического кода
Происхождение рибосомы, белкового синтеза и генетического кода Історичні відомості про спроби класифікації хімічних елементів. Відкриття періодичного закону Д.І. Менделєєва
Історичні відомості про спроби класифікації хімічних елементів. Відкриття періодичного закону Д.І. Менделєєва Связующие для полимерных композиционных материалов. (Тема 2)
Связующие для полимерных композиционных материалов. (Тема 2) Супрамолекулярные системы – мост между неживой и живой материей
Супрамолекулярные системы – мост между неживой и живой материей Решение задач. Органическая химия
Решение задач. Органическая химия Закон сохранения массы веществ. Химические уравнения
Закон сохранения массы веществ. Химические уравнения Функціональні матеріали для високоенергетичної електроніки. (Лекція 1)
Функціональні матеріали для високоенергетичної електроніки. (Лекція 1) Нуклеиновые кислоты
Нуклеиновые кислоты Анализ начальных участков изотерм адсорбции
Анализ начальных участков изотерм адсорбции V и III группы периодической системы элементов Д.И. Менделеева
V и III группы периодической системы элементов Д.И. Менделеева Қатты әсер ететін уландырғыш заттар
Қатты әсер ететін уландырғыш заттар Органические и неорганические кислоты
Органические и неорганические кислоты