Слайд 2
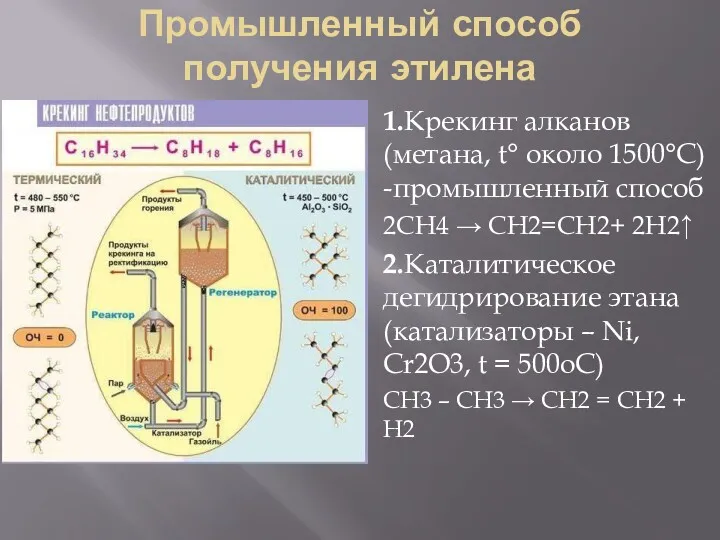
Промышленный способ получения этилена
1.Крекинг алканов (метана, t° около 1500°С)
-промышленный способ
2СН4 → СН2=СН2+ 2Н2↑
2.Каталитическое дегидрирование этана (катализаторы – Ni, Cr2O3, t = 500oC)
CH3 – CH3 → CH2 = CH2 + H2
Слайд 3
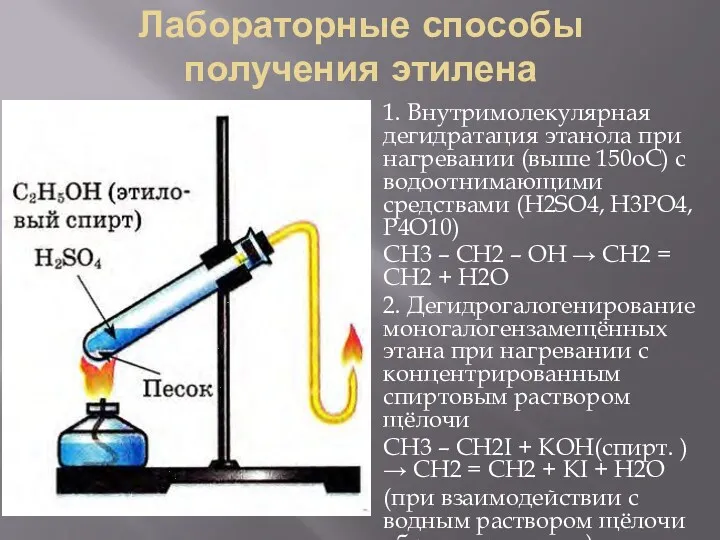
Лабораторные способы получения этилена
1. Внутримолекулярная дегидратация этанола при нагревании (выше 150оС)
с водоотнимающими средствами (H2SO4, H3PO4, Р4О10)
CH3 – CH2 – OH → CH2 = CH2 + H2O
2. Дегидрогалогенирование моногалогензамещённых этана при нагревании с концентрированным спиртовым раствором щёлочи
CH3 – CH2I + KOH(спирт. ) → CH2 = CH2 + KI + H2O
(при взаимодействии с водным раствором щёлочи образуется этанол)
Слайд 4

Применение этилена
Этилен является одним из базовых продуктов промышленной химии и стоит
в основании ряда цепочек синтеза. Основное направление использования этилена — в качестве мономера при получении полиэтилена (наиболее крупнотоннажный полимер в мировом производстве) . В зависимости от условий полимеризации получают полиэтилены низкого давления и полиэтилены высокого давления.
Слайд 5

Также полиэтилен применяют для производства ряда сополимеров, в том числе с
пропиленом, стиролом, винилацетатом и другими. Этилен является сырьем для производства окиси этилена; как алкилирующий агент – при производстве этилбензола, диэтилбензола, триэтилбензола.
Слайд 6
Этилен применяют как исходный материал для производства ацетальдегида и синтетического этилового
спирта. Также он используется для синтеза этилацетата, стирола, винилацетата, хлористого винила; при производстве 1,2-дихлорэтана, хлористого этила.
Слайд 7

Этилен используют для ускорения созревания плодов — например, помидоров, дынь, апельсинов,
мандаринов, лимонов, бананов; дефолиации растений, снижения предуборочного опадения плодов, для уменьшения прочности прикрепления плодов к материнским растениям, что облегчает механизированную уборку урожая.






 Кислоты. Растворы всех кислот
Кислоты. Растворы всех кислот Хімія та їжа
Хімія та їжа Химическая связь
Химическая связь Литий
Литий Классификация органических соединений
Классификация органических соединений Гидролиз солей
Гидролиз солей Аминокислоты. Пептиды. Белки
Аминокислоты. Пептиды. Белки Кремний и его соединения
Кремний и его соединения Гідроліз солей
Гідроліз солей Периодический закон Менделеева
Периодический закон Менделеева Изучение строения и свойств глюкозы
Изучение строения и свойств глюкозы Минералы. Принципы классификации минералов
Минералы. Принципы классификации минералов Лекция 6. Электрофильное присоединение к кратным связям
Лекция 6. Электрофильное присоединение к кратным связям Прикладные аспекты химии поверхностно-активных веществ
Прикладные аспекты химии поверхностно-активных веществ Фенолы
Фенолы Физико-химические процессы в системе свинец - сталь - кислород, для энергетических ядерных реакторов
Физико-химические процессы в системе свинец - сталь - кислород, для энергетических ядерных реакторов Теория строения органических соединений А.М. Бутлерова
Теория строения органических соединений А.М. Бутлерова Катионная полимеризация (Лекция 6)
Катионная полимеризация (Лекция 6) Теорія сильних і слабких електролітів. Рівновага в розчинах малорозчинних електролітів
Теорія сильних і слабких електролітів. Рівновага в розчинах малорозчинних електролітів Алюминий. Строение и свойство атомов
Алюминий. Строение и свойство атомов Методы исследования гидрохимического режима водоемов
Методы исследования гидрохимического режима водоемов Алкадиены
Алкадиены Кремний и его соединения. Простое вещество - кристаллический кремний Si
Кремний и его соединения. Простое вещество - кристаллический кремний Si Аналитическая химия. Предмет и задачи
Аналитическая химия. Предмет и задачи Вода. Практическая работа
Вода. Практическая работа Спирти
Спирти Электролитическая диссоциация. Вещества в растворах
Электролитическая диссоциация. Вещества в растворах Твердое состояние вещества. Плавление
Твердое состояние вещества. Плавление