Содержание
- 2. Как же химики судят о том, является ли данное вещество кислотой? Растворы всех кислот на вкус
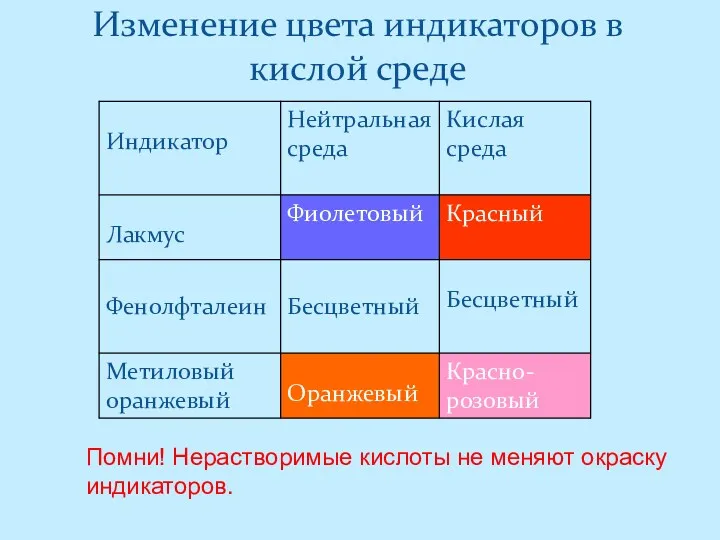
- 3. Изменение цвета индикаторов в кислой среде Помни! Нерастворимые кислоты не меняют окраску индикаторов.
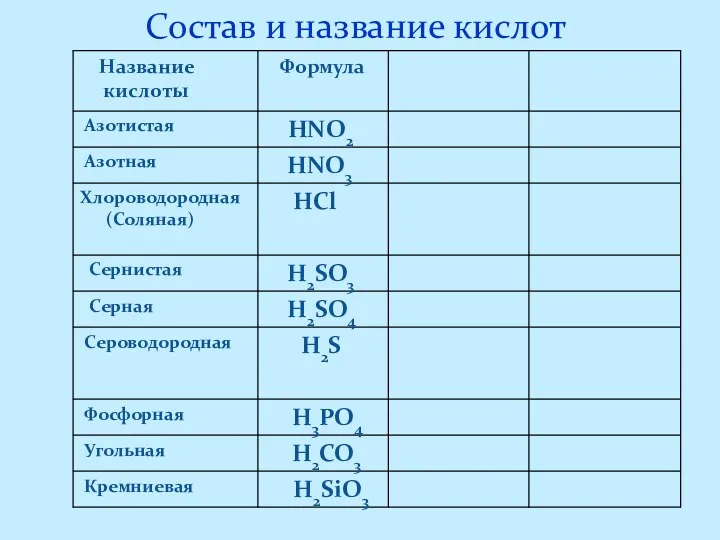
- 4. Состав и название кислот
- 5. Кислоты – это сложные вещества, молекулы, которых состоят из атомов водорода и кислотных остатков.
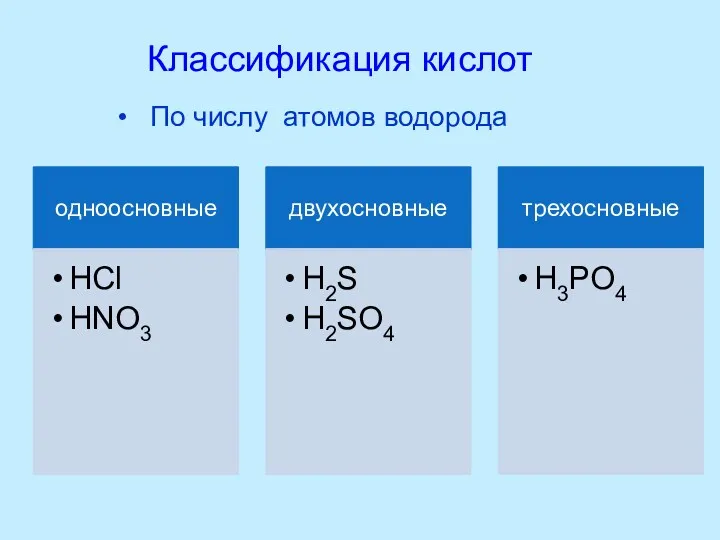
- 6. По числу атомов водорода Классификация кислот
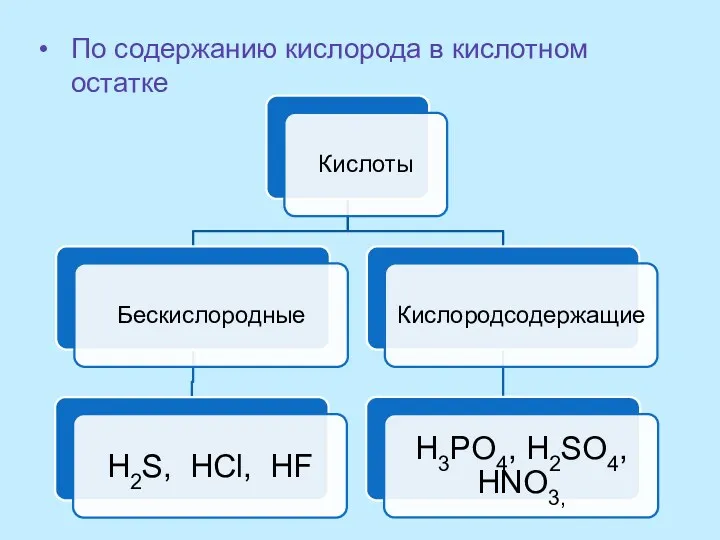
- 7. По содержанию кислорода в кислотном остатке
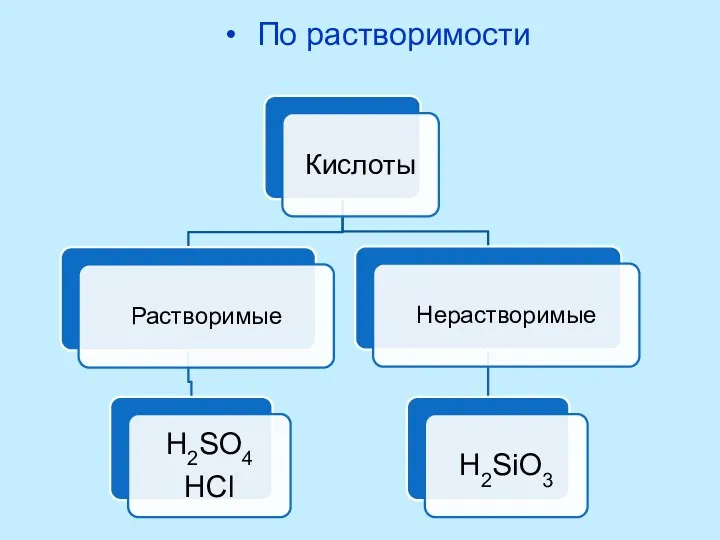
- 8. По растворимости
- 11. Серная кислота бесцветная , вязкая жидкость, без запаха, вдвое тяжелее воды, поглощает влагу из воздуха и
- 12. Обугливание лучинки серной кислотой
- 13. Обугливание сахара серной кислотой
- 14. Обугливание бумаги серной кислотой
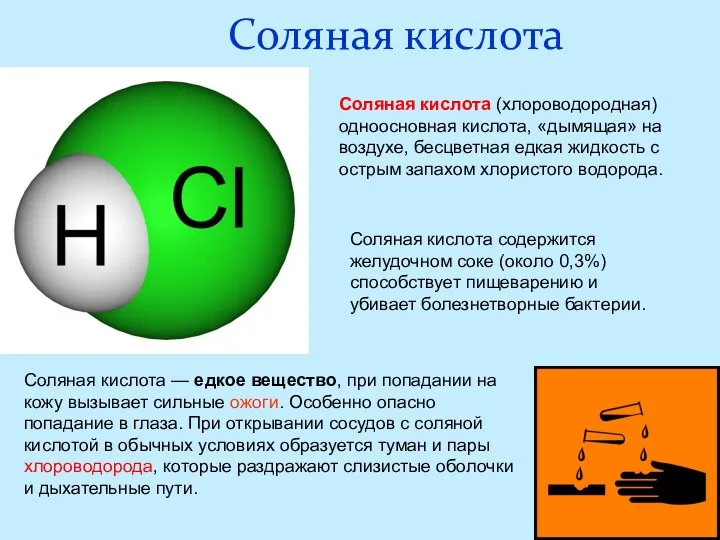
- 15. Соляная кислота Соляная кислота содержится желудочном соке (около 0,3%) способствует пищеварению и убивает болезнетворные бактерии. Соляная
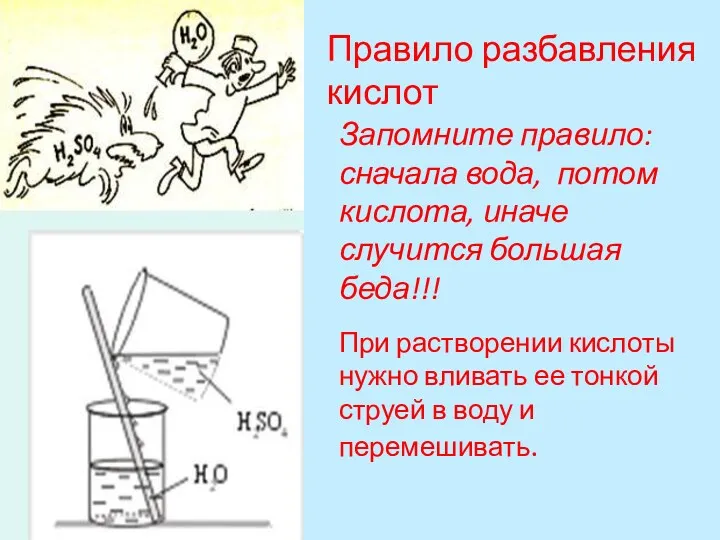
- 16. Правило разбавления кислот При растворении кислоты нужно вливать ее тонкой струей в воду и перемешивать. Запомните
- 17. ЕСЛИ КИСЛОТА ПОПАЛА НА КОЖУ. Пораженный участок кожи промывают сильно скользящей струей холодной воды в течение
- 18. H2CO3 → CO2↑ + H2O H2SO3 → SO2↑ + H2O В свободном виде не существуют. Они
- 19. Как узнать какие оксиды соответствуют данным кислотам? Помните, что суммарная степень окисления атомов всех элементов в
- 20. Проверь себя Выберите группу веществ, в состав которой входят только кислоты HCl, SO3, NaOH,CuCl2 HNO3, H2S,
- 21. Проверь себя Выберите группу веществ, в состав которой входят только двухосновные кислоты HNO3, H2S, HCl, H3PO4
- 22. HNO3, H2S, HCl, H2CO3 HCl, H2SO4, H2SiO3, H2SO3 H2S, HNO3, H2SO3, H3PO4 HNO3, H2SO4, H3PO4, HNO2
- 23. Проверь себя В кислой среде синий лакмус становится: фиолетовым красным малиновым не изменяет окраску
- 25. Скачать презентацию














 Основания. Состав, классификация, свойства, получение
Основания. Состав, классификация, свойства, получение Газы, применяемые при сварке
Газы, применяемые при сварке Сера. Аллотропия серы. Физические и химические свойства серы. Применение серы
Сера. Аллотропия серы. Физические и химические свойства серы. Применение серы Crystallography. Part 4: Crystal Forms Twinning
Crystallography. Part 4: Crystal Forms Twinning Менделеевские уроки. День науки
Менделеевские уроки. День науки Неметаллические материалы
Неметаллические материалы Основные сведения о строении атома
Основные сведения о строении атома Решение комбинированных задач. Задачи на смеси
Решение комбинированных задач. Задачи на смеси Соли, их классификация и свойства
Соли, их классификация и свойства Кремний и его соединения
Кремний и его соединения Изучение свойств тиосульфата натрия
Изучение свойств тиосульфата натрия Поливинилхлорид (ПВХ, PVC)
Поливинилхлорид (ПВХ, PVC) Теория радикалов (30 гг. XIX в Й.Берцелиус, Ю.Либих, Ж.Дюма)
Теория радикалов (30 гг. XIX в Й.Берцелиус, Ю.Либих, Ж.Дюма) Электролитическая диссоциация
Электролитическая диссоциация Бензен як представник ароматичних вуглеводнів
Бензен як представник ароматичних вуглеводнів Кислородсодержащие соединения серы
Кислородсодержащие соединения серы Механизмы органических реакций
Механизмы органических реакций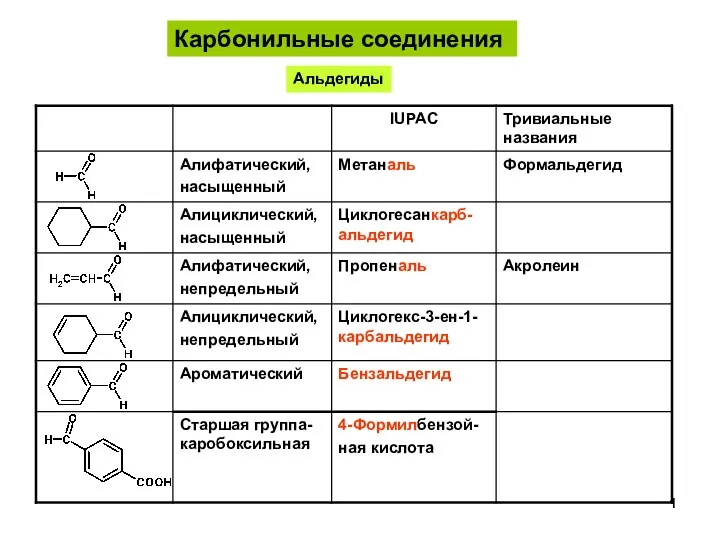 АльдегидыКетоны-1
АльдегидыКетоны-1 Белки. Определение
Белки. Определение Ферменты и гормоны. (10-11 класс)
Ферменты и гормоны. (10-11 класс) Химические свойства алканов
Химические свойства алканов Хімічні властивості кислот
Хімічні властивості кислот большая стирка
большая стирка Пищевые добавки
Пищевые добавки Химическое загрязнение атмосферы
Химическое загрязнение атмосферы Обмен липидов
Обмен липидов Кинетика химических реакций и химическое равновесие
Кинетика химических реакций и химическое равновесие Максимально очищенные фитопрепараты. Технология и стандартизация
Максимально очищенные фитопрепараты. Технология и стандартизация