Содержание
- 2. Натрия гидрокарбонат Natrii hydrocarbonas NaHCO3 Ф а р м а ц е в т и ч
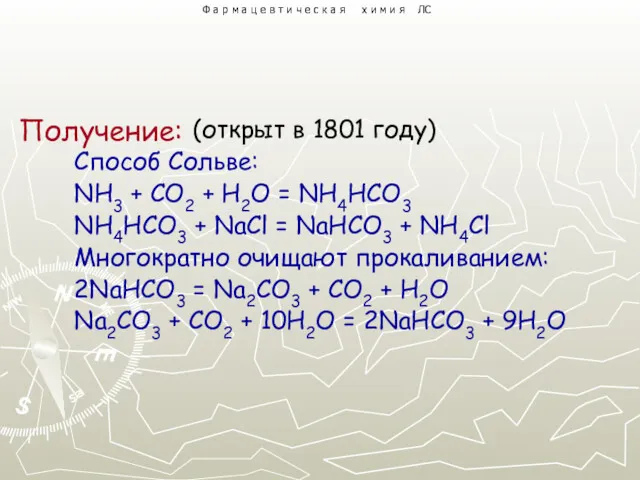
- 3. (открыт в 1801 году) Способ Сольве: NH3 + CO2 + H2O = NH4HCO3 NH4HCO3 + NaCl
- 4. Белый кристаллический порошок без запаха, солено-щелочного вкуса, устойчив в сухом воздухе, медленно разлагается во влажном. Водные
- 5. Хорошо растворяется в воде, нерастворим в 95% спирте. Водный 0,1н раствор препарата не должен окрашиваться от
- 6. 1) Na+ - пирохимическая реакция 2) на карбонат - ион NaHCO3 + HCl = NaCl +
- 7. - прозрачность и цветность раствора - не допускается NH4+, тяжелые металлы - допустимое предельное содержание Cl-,
- 8. Метод нейтрализации, ацидиметрия Рабочий раствор- 0,1н HCl Ind - м/о NaHCO3 + HCl = NaCl +
- 9. в хорошо укупоренной таре Ф а р м а ц е в т и ч е
- 10. Кислота борная Acidum boricum H3BO3 М.м. 61,83 Ф а р м а ц е в т
- 11. В промышленности борную кислоту получают из борсодержащих минералов (ашарита Mg2OB2O5*H2O) действием концентрированной серной кислоты Ф а
- 12. Жирные на ощупь, бесцветные, прозрачные чешуйчатые кристаллы или мелкий белый кристаллический порошок без запаха. Ф а
- 13. В холодной воде растворяется плохо, в горячей – хорошо. Растворима в спирте 1/25, хуже в глицерине
- 14. 1) с этанолом в присутствии конц. H2SO4, при этом образуется борно-этиловый эфир, который дает пламя с
- 15. 2) с куркумовой бумажкой, одновременно добавляя несколько капель HCl – появляется розовый или буровато-красный цвет. Если
- 16. - прозрачность и цветность; - допускается присутствие примесей: кальция, железа, тяжелых металлов, мышьяка, сульфатов в количестве,
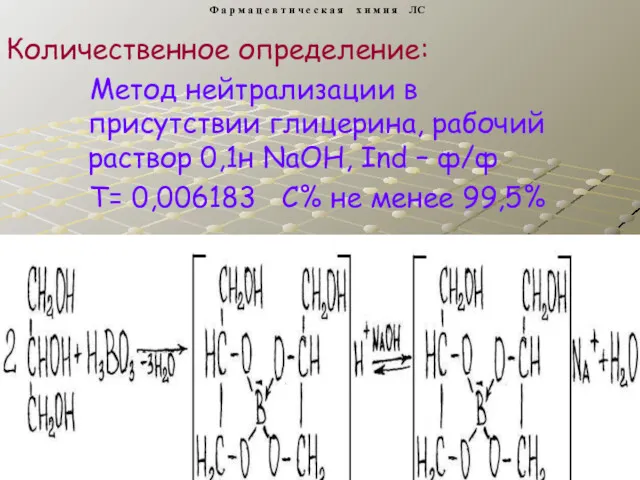
- 17. Метод нейтрализации в присутствии глицерина, рабочий раствор 0,1н NaOH, Ind – ф/ф Т= 0,006183 С% не
- 18. - как антисептическое средство в виде 2-3% растворов для полоскания горла, в мазях и присыпках; -
- 19. В хорошо укупоренной таре Ф а р м а ц е в т и ч е
- 20. Натрия тетроборат. Бура Natrii tetraboras Borax Na2B4O7*10H2O М.м. 381,37 Ф а р м а ц е
- 21. В природе встречается в свободном состоянии. В промышленности получают из борной кислоты действием водного раствора карбоната
- 22. бесцветные прозрачные легковыветривающиеся кристаллы или белый кристаллический порошок Ф а р м а ц е в
- 23. Хорошо растворяется в воде, лучше в горячей. Легко в глицерине, не растворяется в спирте Ф а
- 24. а) Na+: пирохимическая реакция -окрашивание пламени в желтый цвет б) бура дает все реакции, характерные для
- 25. - не должно быть примесей карбонатов; - допускаются примеси мышьяка, хлоридов, сульфатов, железа Ф а р
- 26. Метод нейтрализации (ацидиметрия) Рабочий раствор – 0,1N HCL Ind – м/о Na2B4O7 * 10H2O + 2HCl
- 27. Ф а р м а ц е в т и ч е с к а я
- 29. Скачать презентацию
























 Технология получения многослойного и малослойного графена
Технология получения многослойного и малослойного графена Жири як представники естерів. Класифікація жирів, їхні хімічні властивості
Жири як представники естерів. Класифікація жирів, їхні хімічні властивості 20230816_belki_2
20230816_belki_2 Халькогены
Халькогены Растворы. (Лекция 7)
Растворы. (Лекция 7) Химические элементы азот и фосфор
Химические элементы азот и фосфор Альдегиды и кетоны
Альдегиды и кетоны Буферное кислотно - основное взаимодействие
Буферное кислотно - основное взаимодействие Наглядное пособие Динамические модели. Кристаллы. Немолекулярные вещества. Простые вещества
Наглядное пособие Динамические модели. Кристаллы. Немолекулярные вещества. Простые вещества Химическая связь
Химическая связь Биологически активные вещества и их содержание в лекарственных растениях
Биологически активные вещества и их содержание в лекарственных растениях Основания. Степени окисления элементов в соединениях
Основания. Степени окисления элементов в соединениях Общая характеристика элементов V группы главной подгруппы
Общая характеристика элементов V группы главной подгруппы Диффузия вокруг нас
Диффузия вокруг нас Франций (Francium)
Франций (Francium) Термодинамика химических процессов
Термодинамика химических процессов Закон сохранения массы веществ. Химические уравнения
Закон сохранения массы веществ. Химические уравнения Качественные реакции
Качественные реакции Минералы горных пород
Минералы горных пород Химический элемент радон
Химический элемент радон Осадочные и метаморфические горные породы
Осадочные и метаморфические горные породы Мило та миловаріння
Мило та миловаріння Кислотність та основність органічних сполук
Кислотність та основність органічних сполук Проведение лабораторных анализов образцов почвы
Проведение лабораторных анализов образцов почвы Подгруппа углерода
Подгруппа углерода Химический элемент алюминий
Химический элемент алюминий Пластические массы и изделия на их основе
Пластические массы и изделия на их основе Зависимость биохимических изменений в мясе от условий хранения
Зависимость биохимических изменений в мясе от условий хранения