Содержание
- 2. Способы содержания вещества в растворе Массовая доля растворенного вещества (процентная концентрация (ω)) показывает число г растворенного
- 3. Молярная концентрация (С) показывает число моль растворенного вещества (n) в 1 дм³ раствора (V): Выражается в
- 4. Молярная концентрация эквивалента (нормальная, нормальность, эквивалентная) – это число молей-эквивалентов растворенного вещества в 1 дм³ раствора
- 5. Моляльность (Сm) показывает число моль (n) растворенного вещества в 1 кг (1000 г) растворителя (mр-ля): Выражается
- 6. Титр по растворённому веществу или просто титр — масса растворённого вещества (в граммах), содержащаяся в одном
- 7. Взаимосвязь концентраций Молярная концентрация эквивалента и Титр. С (1/zА) М(1/zА) = Т 1000 Молярная концентрация эквивалента
- 8. Правило смешения (КРЕСТА) Правило креста (диагональная модель «конверта Пирсона») – диагональная схема правила смешения: При расчетах
- 9. Приготовление растворов из кристаллогидратов m кр m бс Mкр M бс
- 10. В практической работе важно уметь быстро переходить от одних единиц концентрации к другим, поэтому важно помнить,
- 11. Современная теория растворения Процесс растворения является сложным физико-химическим процессом, в котором наиболее ярко проявляется взаимодействие между
- 12. Коллигативные свойства растворов В конце XIX века Рауль, Вант-Гофф, Аррениус установили весьма важные закономерности, связывающие концентрацию
- 13. Первый закон Рауля (1887): относительное понижение давления насыщенного пара растворителя над раствором нелетучего неэлектролита равно мольной
- 14. Второй закон Рауля Абсолютное понижение температуры замерзания или абсолютное повышение температуры кипения разбавленных растворов неэлектролитов прямо
- 15. Криоскопическая постоянная показывает абсолютное понижение температуры замерзания раствора неэлектролита, который в одном кг растворителя содержит один
- 16. Закон Вант-Гоффа Осмотическое давление растворенного вещества в разбавленном растворе равно тому газовому давлению, которое производило бы
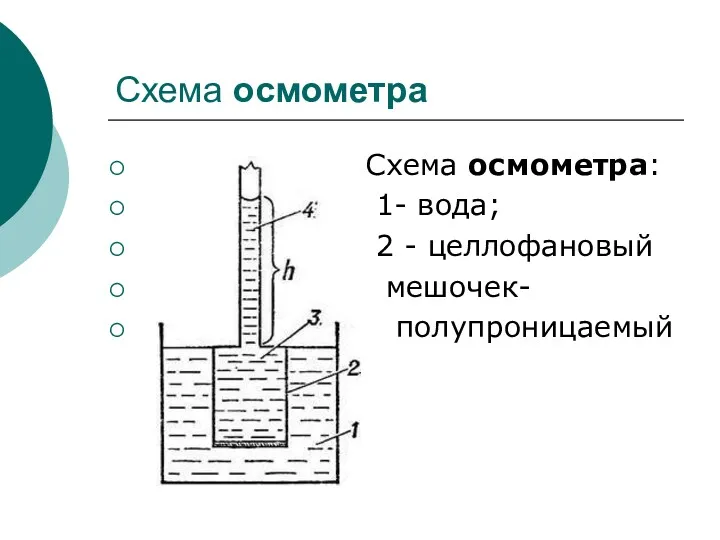
- 17. Осмотическое давление – это давление, которое наблюдается в растворах и вызывается ударами частиц растворенного вещества о
- 18. Схема осмометра Схема осмометра: 1- вода; 2 - целлофановый мешочек- полупроницаемый
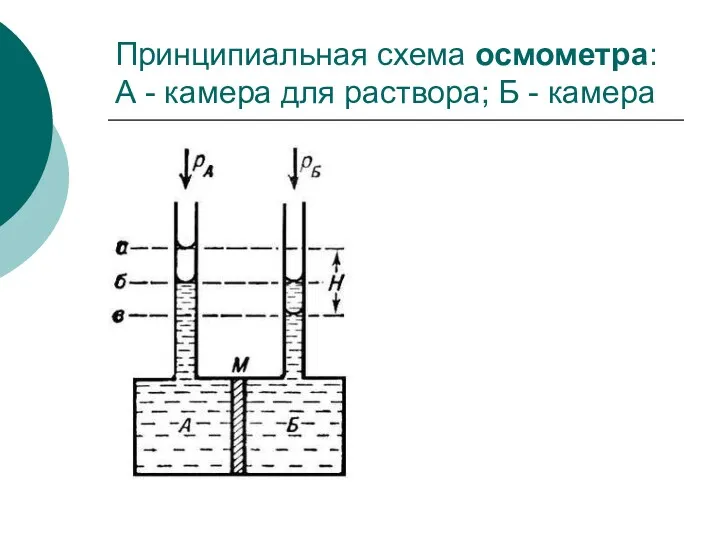
- 19. Принципиальная схема осмометра: А - камера для раствора; Б - камера
- 20. Осмометр 3250 представляет собой прибор для измерения осмотической концентрации. Аппарат разработан фирмой Advanced Instruments на основе
- 21. Для растворов электролитов осмотическое давление, определенное на осмометре всегда больше, чем рассчитанное по уравнению (7.11). Это
- 22. Изотонический коэффициент меняется в пределах от 1 до 5 и относится только к растворенному веществу. Для
- 23. Законы Рауля и Вант-Гоффа соблюдаются лишь в разбавленных растворах. C повышением концентрации растворенного вещества возрастают отклонения
- 24. Типы жидких растворов. Растворимость Одни вещества способны растворяться неограниченно (вода и спирт), другие – лишь в
- 25. Закон Генри Зависимость растворимости газов от давления выражается законом Генри (1803): растворимость данного газа в жидкости
- 26. Растворы жидкостей в жидкостях. В зависимости от природы жидкости могут: 1) смешиваются друг с другом в
- 27. Закон распределения Нернста-Шилова Если в систему, состоящую из двух взаимно нерастворимых жидкостей, ввести третье вещество, которое
- 28. Растворы твердых тел в жидкостях. Растворимость твердых веществ также определяется природой растворителя и растворенного вещества и
- 29. Свойства слабых электролитов При растворении в воде или других растворителях, состоящих из полярных молекул, электролиты подвергаются
- 30. где аН+, аА-, аНА – активность ионов и кислоты (а = αС). Константа равновесия для процесса
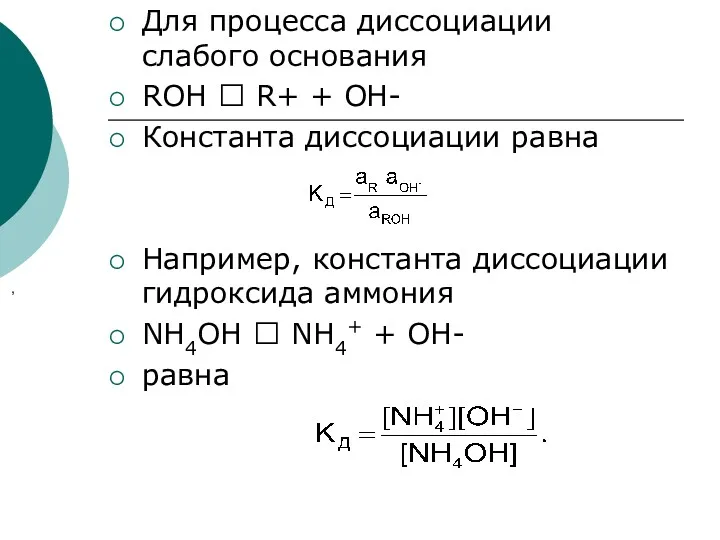
- 31. Для процесса диссоциации слабого основания ROH ⮀ R+ + OH- Константа диссоциации равна Например, константа диссоциации
- 32. Для слабых электролитов константа диссоциации зависит от природы диссоциирующего вещества и растворителя, температуры, но не зависит
- 33. Для многоосновных слабых электролитов константа диссоциации расписывается для каждой ступени диссоциации. Например, для ортофосфорной кислоты (Н3РО4)
- 34. Основываясь на законе действующих масс, можно вывести уравнение, которое связывает константу диссоциации КД электролита со степенью
- 35. где С – молярная концентрация электролита, моль/дм³. Выведенная формула (7.26) является аналитическим выражением закона разбавления Оствальда.
- 36. Последнее соотношение показывает, что при разбавлении раствора (т. е. при уменьшении концентрации электролита С) степень диссоциации
- 37. Ионное произведение воды Химически чистая вода является очень слабым электролитом, который при диссоциации образует ионы водорода
- 38. где КW – ионное произведение воды. При 295 К КW = 10-14, поэтому [H+] = [OH-]
- 39. Произведение растворимости В насыщенном растворе малорастворимого электролита устанавливается равновесие между осадком (твердой фазой) электролита и ионами
- 40. Исходя из значений ПР, можно вычислить растворимость малорастворимых электролитов в воде и растворах, содержащих другие электролиты.
- 41. Свойства сильных электролитов Электролиты, практически полностью диссоциирующие в водных растворах, называются сильными электролитами. К сильным электролитам
- 42. Теория сильных электролитов Разработана П. Дебаем и Э. Хюккелем (1923). Согласно этой теории, в растворах сильных
- 43. По определению, для сильных электролитов истинная степень диссоциации α = 1.В их растворах не обнаружено недиссоциированных
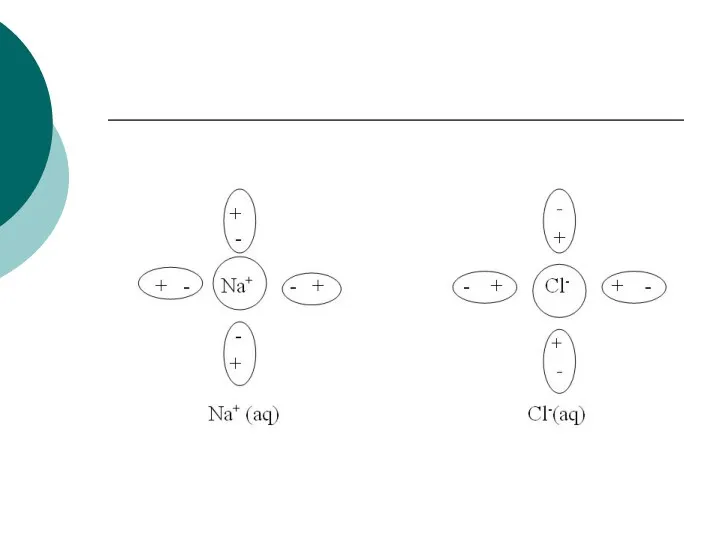
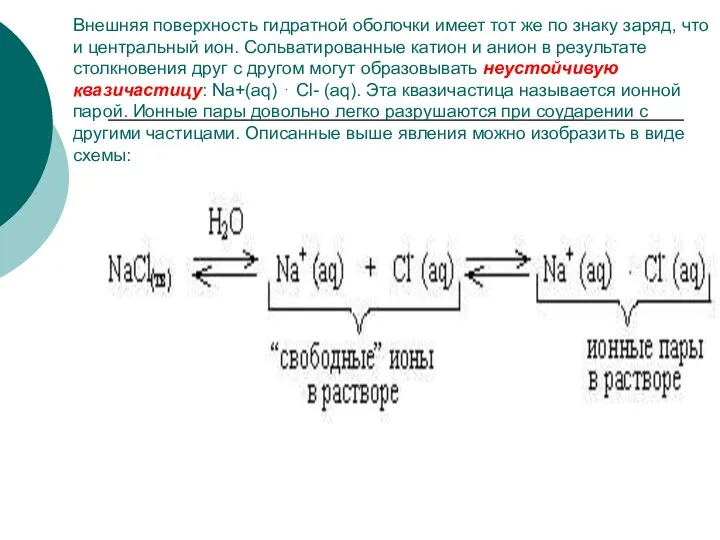
- 45. Внешняя поверхность гидратной оболочки имеет тот же по знаку заряд, что и центральный ион. Сольватированные катион
- 46. Для описания состояния ионов в растворе пользуются их активностью, т. е. условной (эффективной) концентрацией ионов, в
- 47. Например, ионная сила раствора хлорида алюминия с концентрацией 0.01 моль/дм³, диссоциирующего AlCl3 ⮀ Al+3 + 3Cl-,
- 48. Для разбавленных растворов, ионная сила которых не превышает 0,01, коэффициент активности ионов связан с ионной силой
- 50. Скачать презентацию










































 Хімічні властивості кислот
Хімічні властивості кислот Радикальные реакции. (Лекция 9)
Радикальные реакции. (Лекция 9) Полимерлер-біздің болашағымыз
Полимерлер-біздің болашағымыз Почему нефть называют черным золотом
Почему нефть называют черным золотом Карбоновые кислоты. Изомерия. Физические, химические свойства. Получение, применение
Карбоновые кислоты. Изомерия. Физические, химические свойства. Получение, применение Производство водорода
Производство водорода Общие свойства металлов
Общие свойства металлов Основные положения теории растворов электролитов, используемых в аналитической химии. (Лекция 3)
Основные положения теории растворов электролитов, используемых в аналитической химии. (Лекция 3) Растворы электролитов и неэлектролитов. Ионное произведение воды
Растворы электролитов и неэлектролитов. Ионное произведение воды Минералы и горные породы
Минералы и горные породы Enantioselective Total Synthesis
Enantioselective Total Synthesis Основы химической термодинамики и кинетики химических реакций
Основы химической термодинамики и кинетики химических реакций Общая характеристика галогенов
Общая характеристика галогенов Алканы. Получение, свойства и применение
Алканы. Получение, свойства и применение Термодинамика химических процессов
Термодинамика химических процессов Углеводы (особенности строения, реакционной способности и методы синтеза альдегидо- и кетоспиртов)
Углеводы (особенности строения, реакционной способности и методы синтеза альдегидо- и кетоспиртов) Свойства воды. Оценка качества
Свойства воды. Оценка качества Вычисление массы растворённого вещества, содержащегося в определённой массе раствора с известной массовой долей
Вычисление массы растворённого вещества, содержащегося в определённой массе раствора с известной массовой долей Гетерогенді химиялық реакциялар
Гетерогенді химиялық реакциялар Кобальт. Нахождение в природе. Получение
Кобальт. Нахождение в природе. Получение Группа галогенов в периодической системе
Группа галогенов в периодической системе Подгруппа азота
Подгруппа азота Липиды. Классификация
Липиды. Классификация Химический элемент титан
Химический элемент титан Металлы в природе. Получение
Металлы в природе. Получение Кислоты. Состав кислот
Кислоты. Состав кислот Курс биохимии. Биохимия крови
Курс биохимии. Биохимия крови Гетерофункциональные соединения
Гетерофункциональные соединения