Содержание
- 2. Водород: история и перспективы Генри КАВЕНДИШ (1731 г. –1810) Показал, что существуют разные типы воздуха «негорючий
- 3. 1950 Акира Митсуи – производство водорода с помощью микроорганизмов 1959 Френсис Бэкон – первый практический водородно
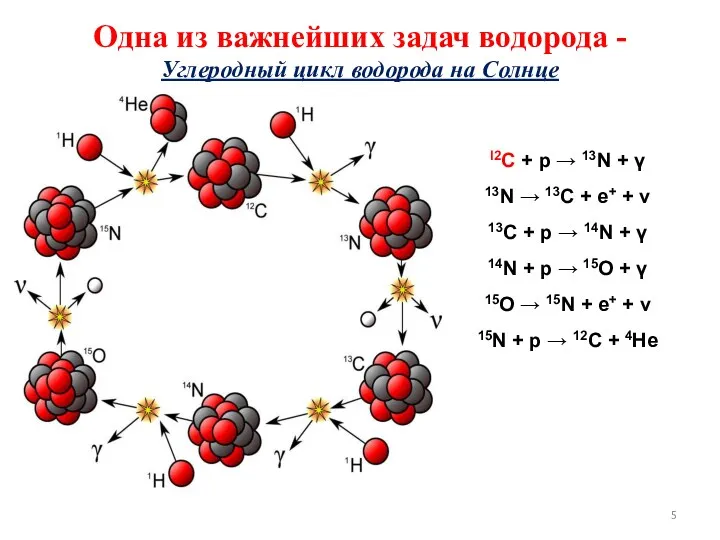
- 5. Одна из важнейших задач водорода - Углеродный цикл водорода на Солнце l2C + p → 13N
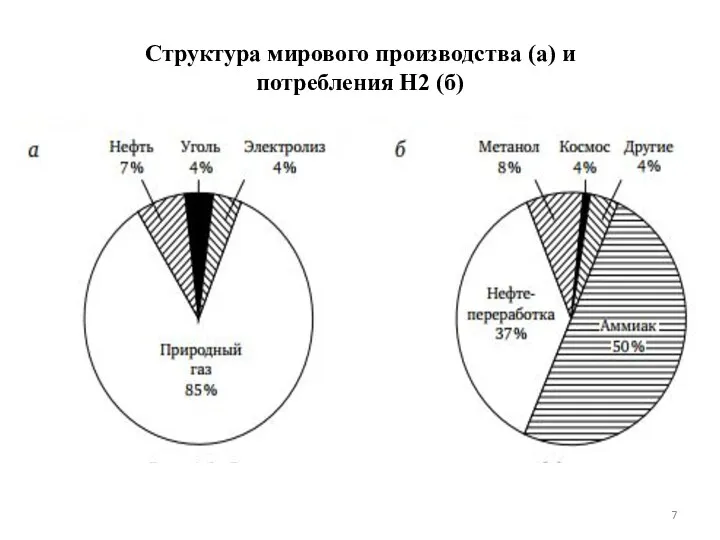
- 7. Структура мирового производства (а) и потребления Н2 (б)
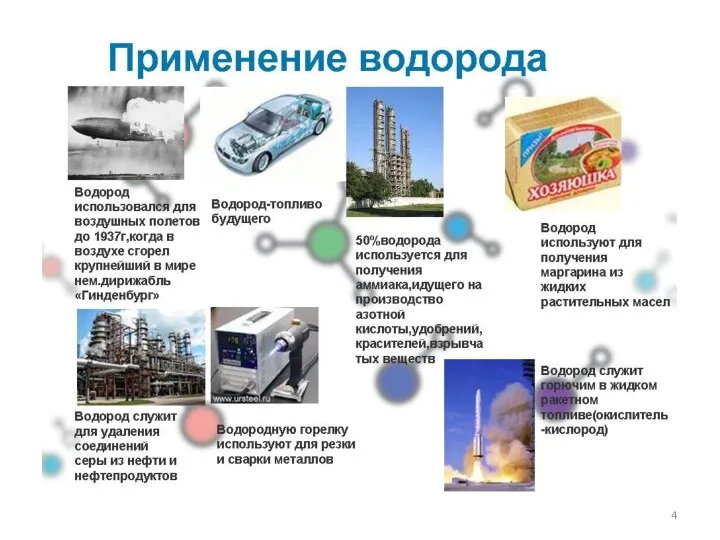
- 8. Применение водорода в химической промышленности
- 10. Возможные способы производства водорода Водород из природных ископаемых и УВ 1.1 Газификация угля 1.2 Паровая конверсия
- 11. 1.1 Производство Н2 газификацией угля
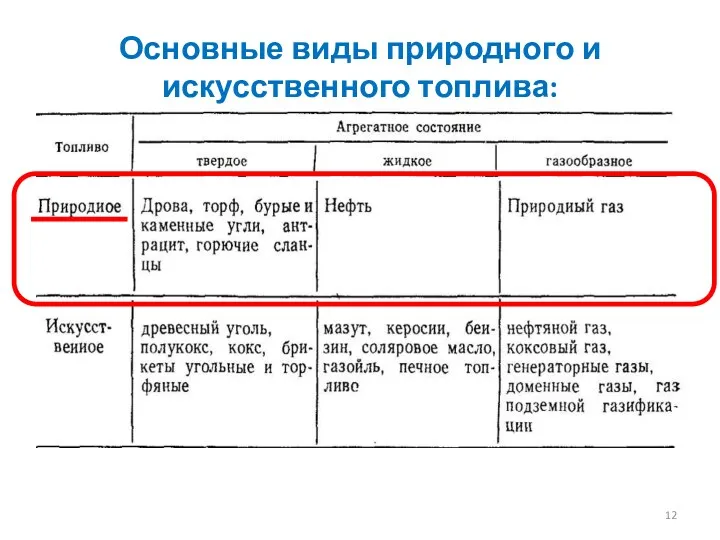
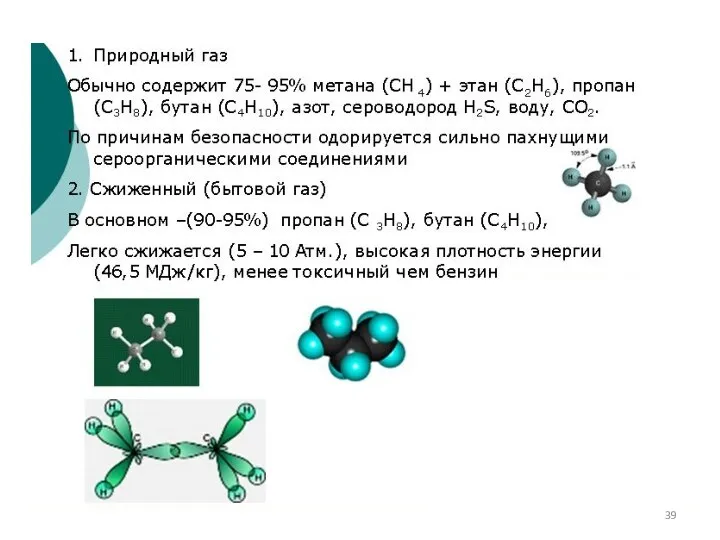
- 12. Основные виды природного и искусственного топлива:
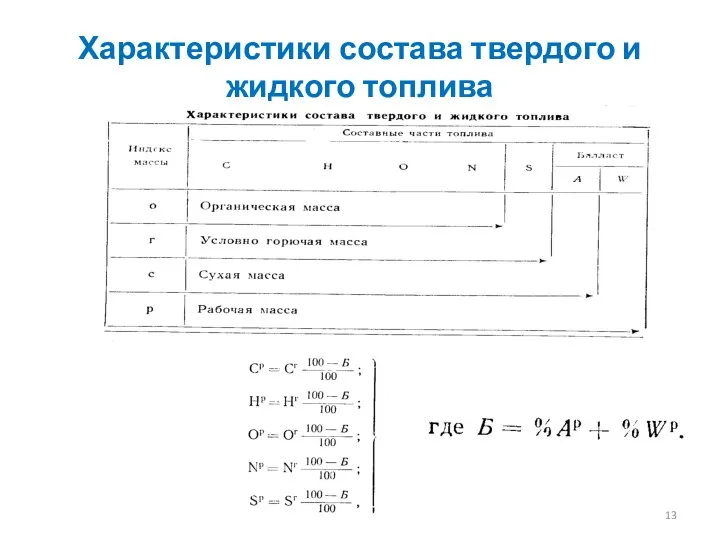
- 13. Характеристики состава твердого и жидкого топлива
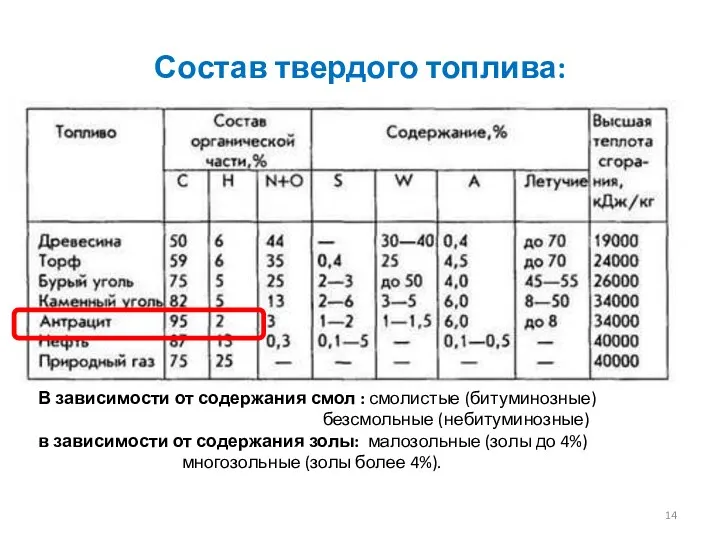
- 14. Состав твердого топлива: В зависимости от содержания смол : смолистые (битуминозные) безсмольные (небитуминозные) в зависимости от
- 15. Преимущества: Около 96% Н2 производится из ископаемых УВ (газ – 48%, нефть – 38%, уголь –
- 16. В зависимости от способа подвода теплоты процесс газификации делится на: Автотермический Теплота, необходимая для проведения реакций,
- 17. Газификация угля C + H2O → CO + H2 (эндотермическая) C+ ½ O2 → CO (экзотермическая)
- 19. Термодинамические характеристики парокислородной газификации угля
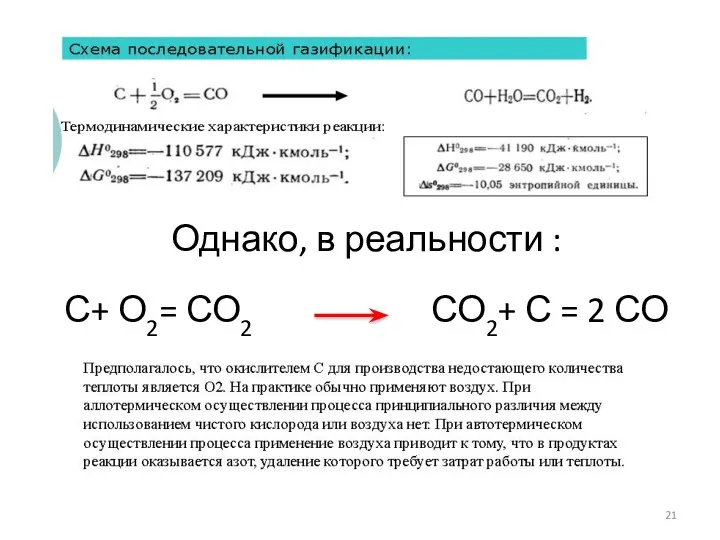
- 21. Однако, в реальности : С+ О2= СО2 СО2+ С = 2 СО
- 22. Классификация процессов газификации угля: Для различных видов горючего были разработаны газогенераторы типов: — газогенераторы прямого процесса
- 23. Технология и особенности процесса газификации углей, а также состав газа варьируются в зависимости от: Особенностей взаимодействия
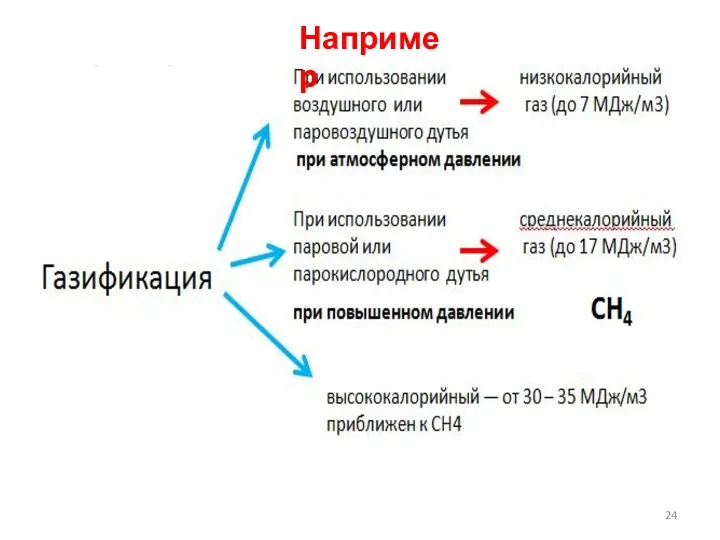
- 24. Например
- 25. Низкокалорийный газ Воздушный газ : 2С+ О2+3,76N2 →2CO +3,76 N2 Водяной газ : С+ Н2О →CO
- 26. Среднекалорийный газ По составу они представляют собой смеси оксидов углерода и водорода с небольшими количествами метана
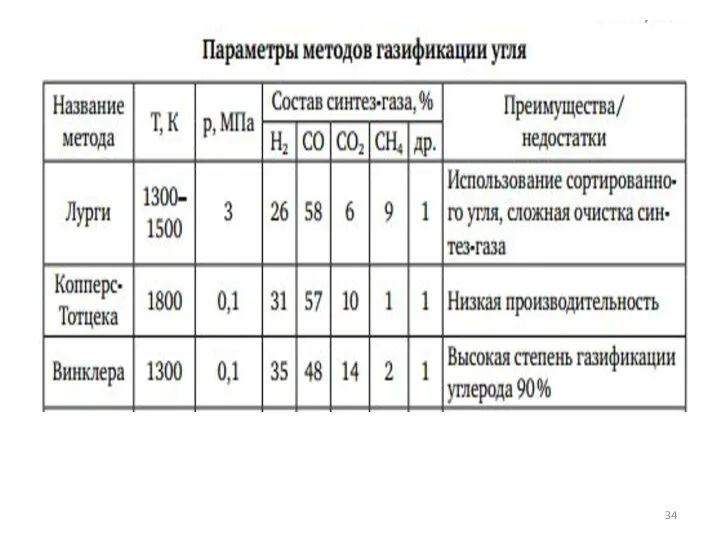
- 27. Наиболее современные газогенераторы Лурги Винклера Копперс-Тотцека Велман-Галуши
- 28. История создания газогенераторов: 1. Создание Фрицем Винклером (концерн BASF) в 1926 г. газогенератора с кипящим слоем.
- 29. Пылеугольный принцип газификации с жидким шлакоудалением реализован в промышленных аппаратах Destec, Shell, Prenflo, разработанных на основе
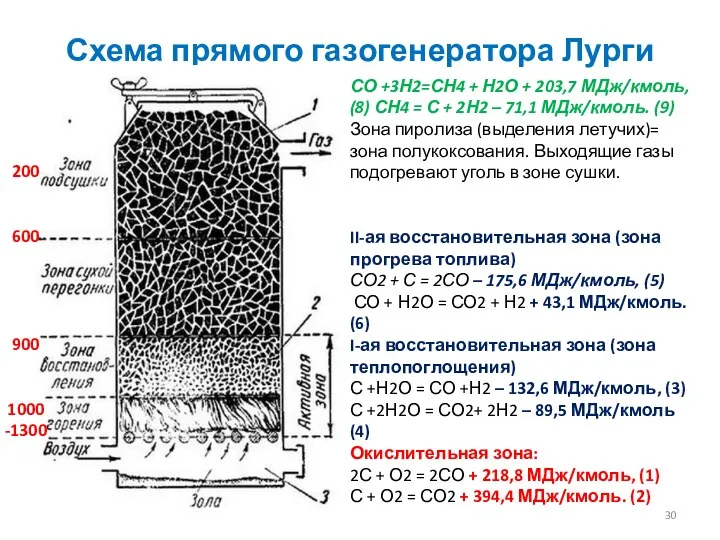
- 30. Схема прямого газогенератора Лурги СО +3Н2=СН4 + Н2О + 203,7 МДж/кмоль, (8) СН4 = С +
- 32. Минусы процесса
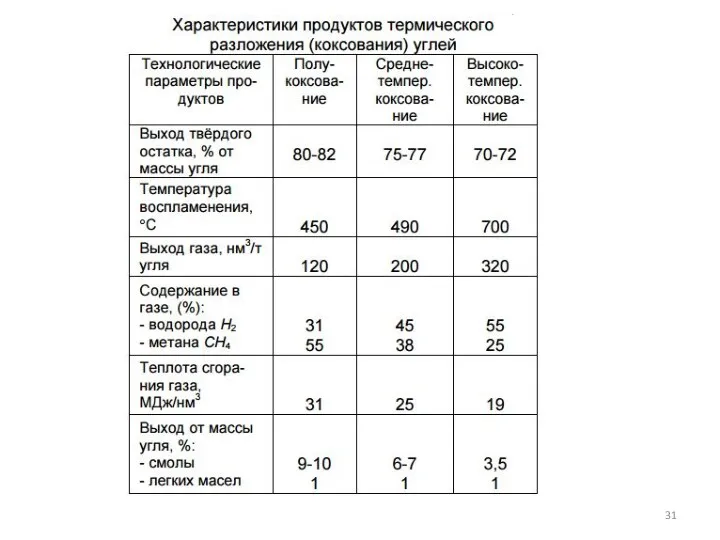
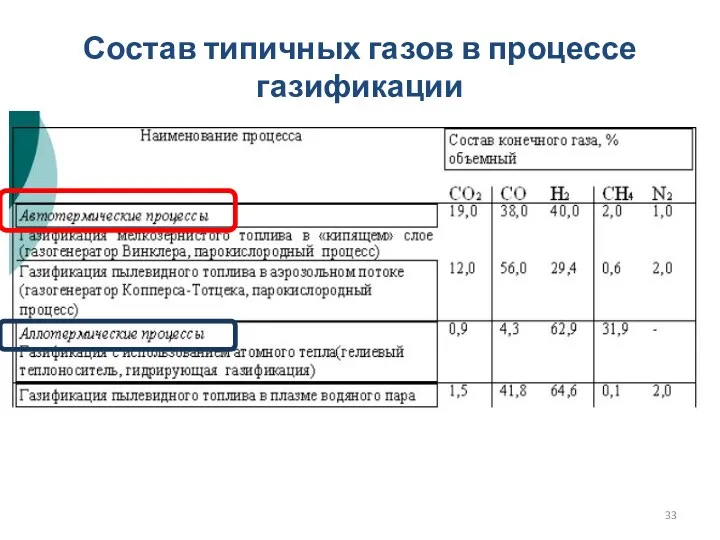
- 33. Состав типичных газов в процессе газификации
- 35. 1.2 Конверсия низших и высших УВ
- 36. В процессе конверсии метан окисляется по следующим основным реакциям: CH4+Н2О= СО + ЗН2- 206,4 кДж/моль (1)
- 37. Если требуется получить технически чистый Н2, проводят р-цию (1) или (3) с последующей конверсией СО по
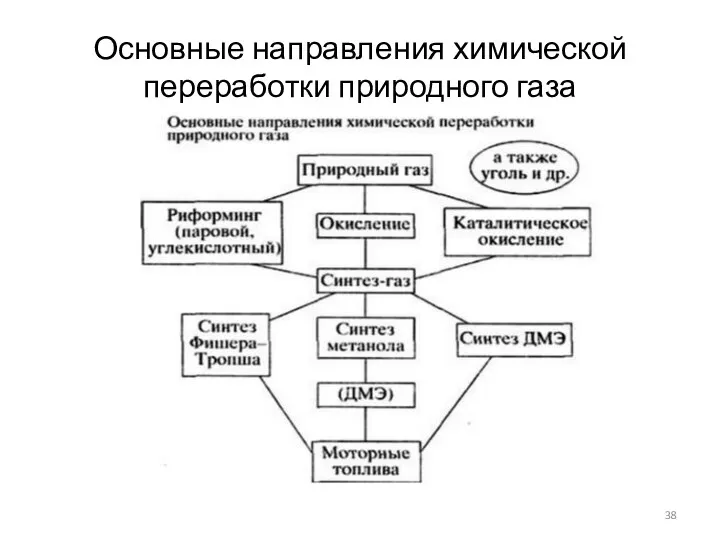
- 38. Основные направления химической переработки природного газа
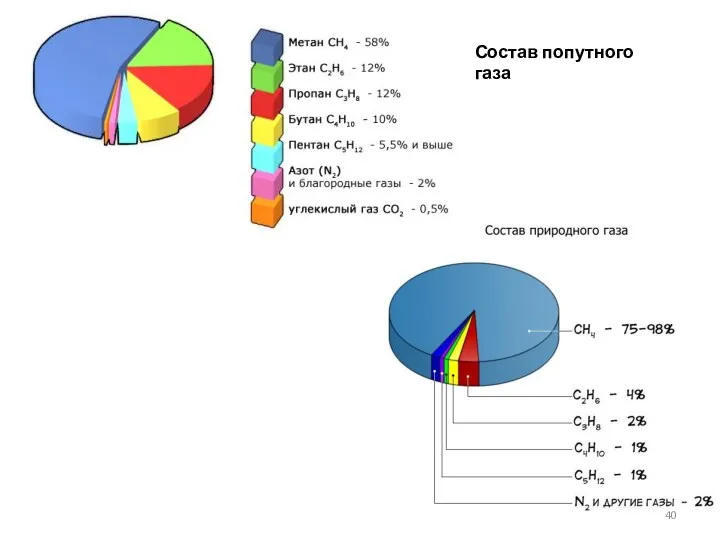
- 40. Состав попутного газа
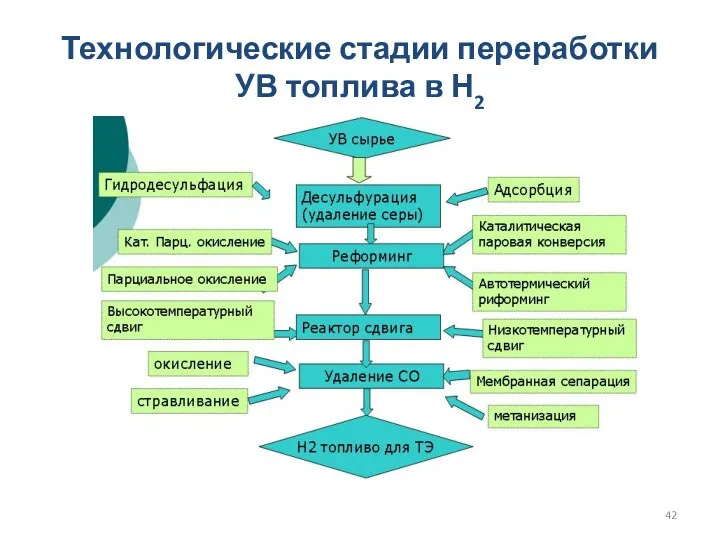
- 42. Технологические стадии переработки УВ топлива в Н2
- 43. Производство водорода
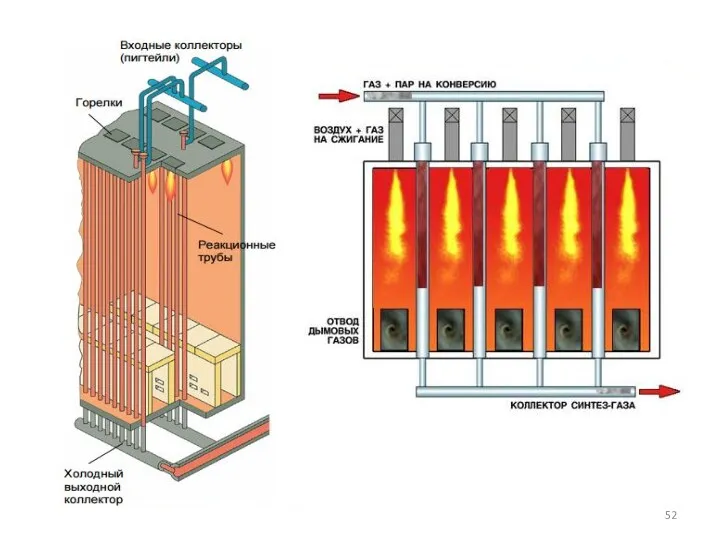
- 44. Паровая конверсия УВ (паровой риформинг) В качестве активаторов в них могут содержаться оксиды Са, Ti, Mg,
- 45. Проведение процесса при повышенных давлениях снижает расходы на компрессию полученного синтез-газа, затраты на изготовление аппаратуры, улучшает
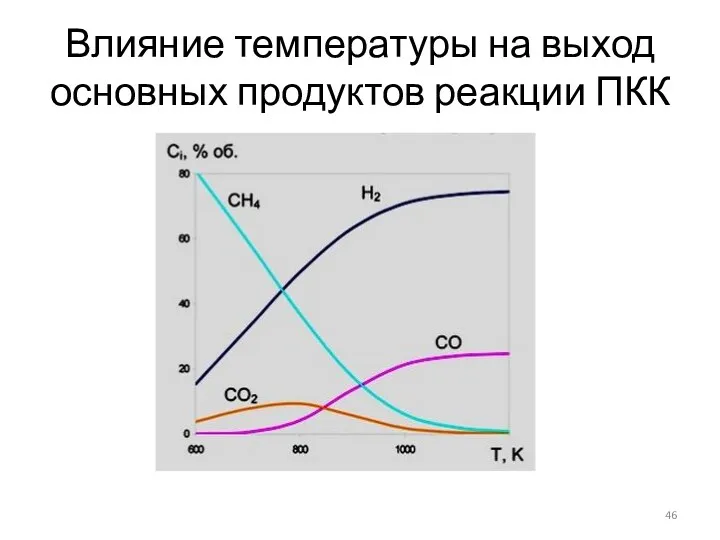
- 46. Влияние температуры на выход основных продуктов реакции ПКК
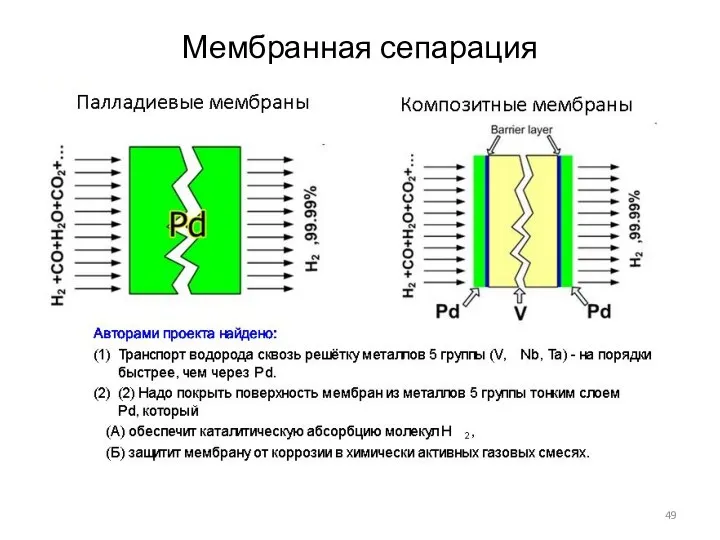
- 48. Мембранная сепарация водорода
- 49. Мембранная сепарация
- 50. Паровая конверсия метана энергия активации разложения газовых гидратов метана составляет 333 кДж/моль Однако наряду с этой
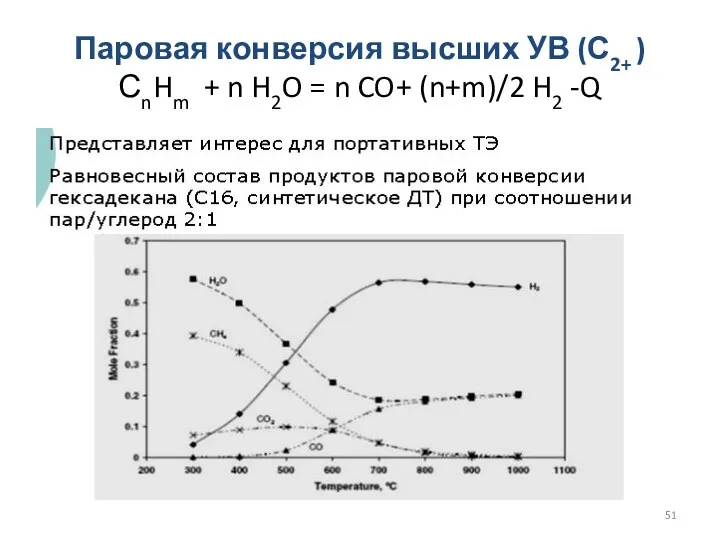
- 51. Паровая конверсия высших УВ (С2+ ) СnHm + n H2O = n CO+ (n+m)/2 H2 -Q
- 54. Особенности восстановления и работы катализатора В свежем катализаторе никель находится в виде оксидов. Катализатором же ускоряющим
- 55. Если Ni находится в виде соединении с Al2O3 (шпинели), то для его восстановления требуется более высокая
- 56. два существенных недостатка высокое содержание водорода в синтез-газе, что затрудняет его использование, например, в синтезе углеводородов
- 57. Высокотемпературная конверсия СН4/ Кислородная конверсия (парциальное окисление) СH4 + 0,5 О2 = CO+ 2 H2 +
- 58. два механизма парциального окисления метана: 1) последовательный механизм — глубокое окисление метана до СО2 и Н2О
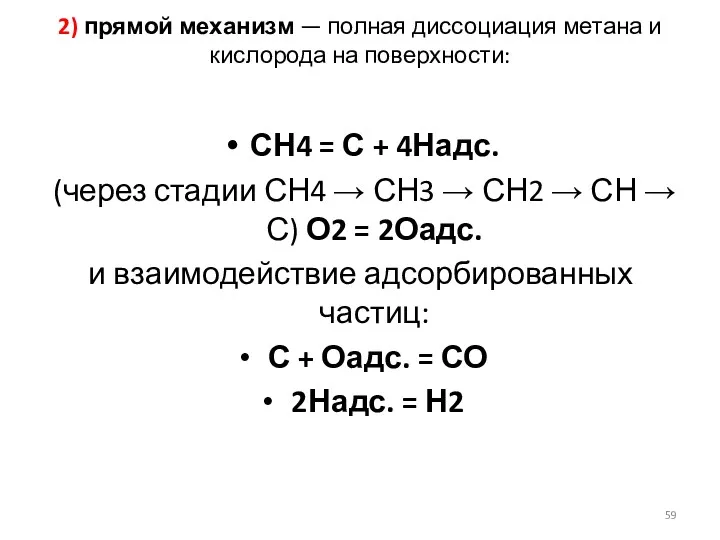
- 59. 2) прямой механизм — полная диссоциация метана и кислорода на поверхности: СН4 = С + 4Надс.
- 60. Парокислородная конверсия (автотермический риформинг) СH4 + 1,5 О2 = CO+ 2 H2О +519 кДж/моль СH4 +
- 61. Углекислотная конверсия Однако!! Катализатор чаще всего Ni/Al2O3 проявляет высокую активность в начальный период работы Снижение углеотложения
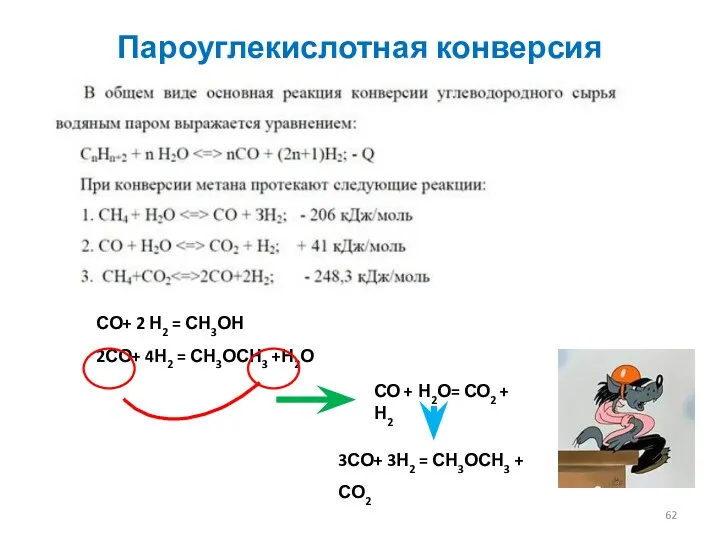
- 62. Пароуглекислотная конверсия СО+ 2 Н2 = СН3ОН 2СО+ 4Н2 = СН3ОСН3 +Н2О СО + Н2О= СО2
- 63. Задачи риформинга:
- 64. Реакция сдвига – паровая конверсия СО водяным паром
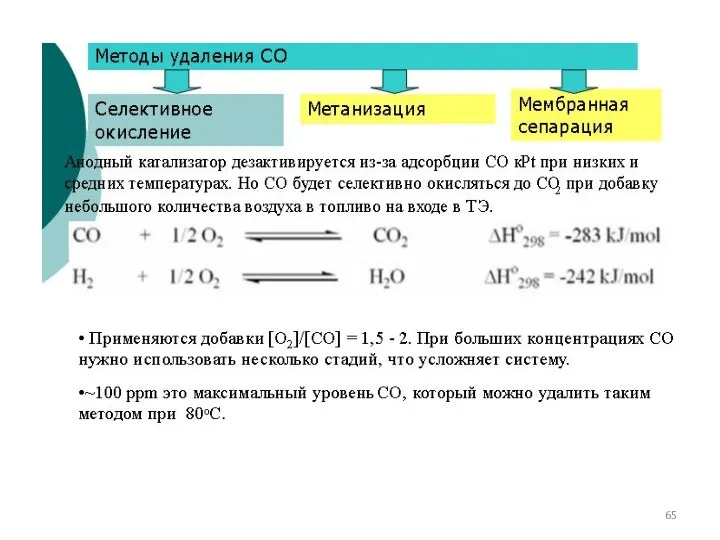
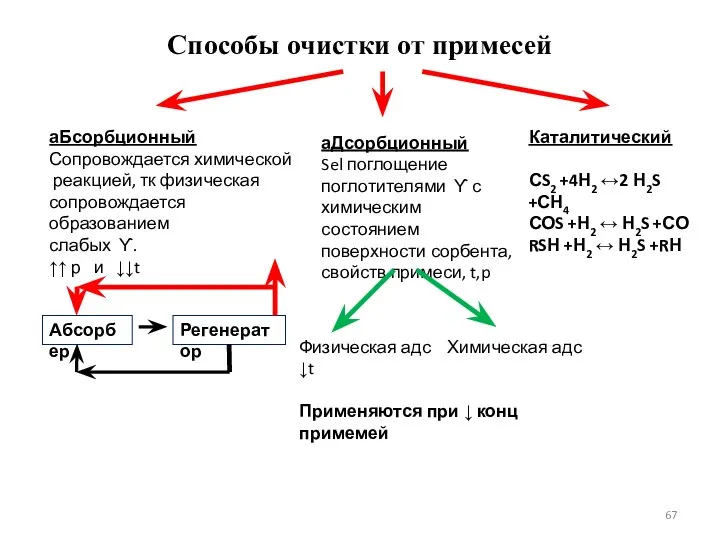
- 67. Способы очистки от примесей аБсорбционный Сопровождается химической реакцией, тк физическая сопровождается образованием слабых ϒ. ↑↑ р
- 68. Очистка природных газов от соединений серы. Углеводордные газы различных месторождений, кроме сероводорода Н2S, могут содержать сероуглерод
- 69. Очистка от сернистых соединений Серосодержащие соединения: H2S, COS, CS2 CnH2n-1SH тиофен С4Н4S сульфиды R-S-R дисульфиды R-SS-R
- 70. Cтепень превращения меркаптана в меркаптид не превышает 80-85% даже при применении 40%-ного водного раствора КОН и
- 71. Влияние амидов на степень извлечения меркаптановой серы
- 72. Каталитический способ нейтрализации
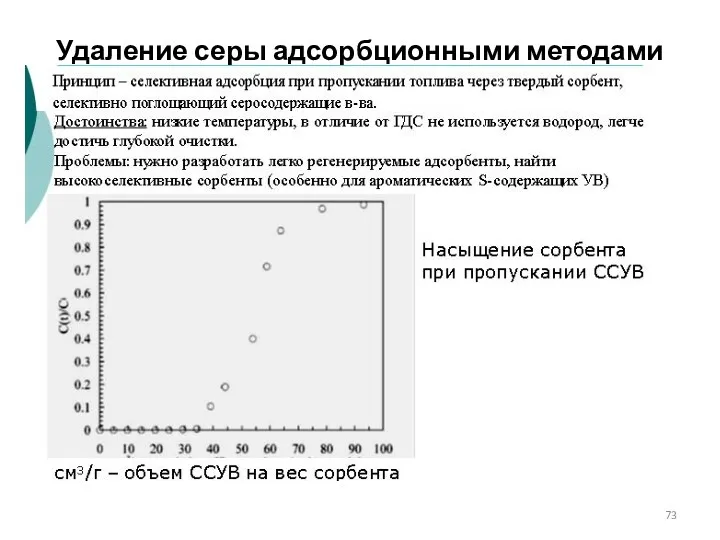
- 73. Удаление серы адсорбционными методами
- 74. Реакции серосодержащих соединений. Сероводород окисляется с образованием элементарной серы и сернистого ангидрида: Сера растворяется в очищаемом
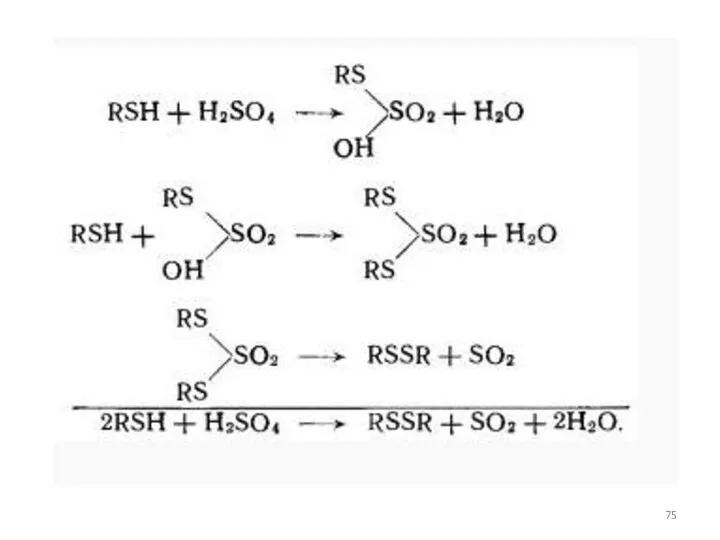
- 76. Помимо реакций образования меркаптидов в присутствии кислорода воздуха происходит окисление меркаптанов с получением дисульфидов: Широко распространен
- 78. Железопаровой способ получения Н2 Основная реакция метода: Т =650-800 С Водородный аэростат и газгольдеры СПб 1941-1945
- 79. Аналогичный метод получения 1941-1945 Si+2NaOH+H20=Na2SiO3+2H2. За час этим способом можно было получить до 400 кубических метров
- 80. Основная реакция метода: Т =650-800 С Образующая магнитная смесь восстанавливается г восстановителями:
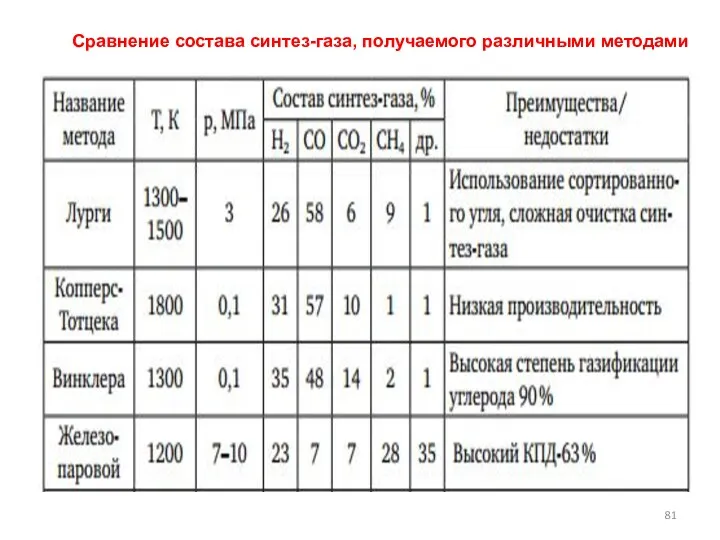
- 81. Сравнение состава синтез-газа, получаемого различными методами
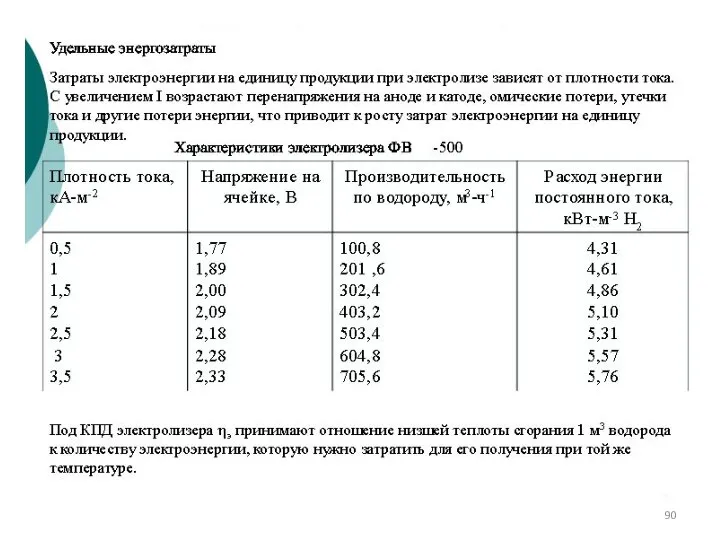
- 82. Электролиз имеет ряд преимуществ перед другими методами получения водорода: Высокая чистота продукта - до 99.9% Простота
- 83. Производство технического водорода электролизом воды, предназначенное для выпуска продукции марки “Б” по ГОСТ 3022-80, включает в
- 84. В процессе ЭХАВ происходят четыре основных процесса: 1) Электролитическое разложение воды (электролиз) за счет окислительно-восстановительных реакций
- 85. Чистая вода имеет удельную электрическую проводимость 0,055 микроОм при 25°С, дистиллированная вода — от 0,5 до
- 86. Физико-химические основы процесса
- 88. Таким образом:
- 89. Постановление Госгортехнадзора РФ от 06.06.2003 N 75 "Об утверждении Правил безопасности при производстве водорода методом электролиза
- 91. Основные электродные процессы при электролизе Выделение Н2 на катоде и О2 на аноде по суммарной реакции
- 92. В нейтральной и кислой среде на аноде происходит поляризация и разряд молекул воды с выделением О2
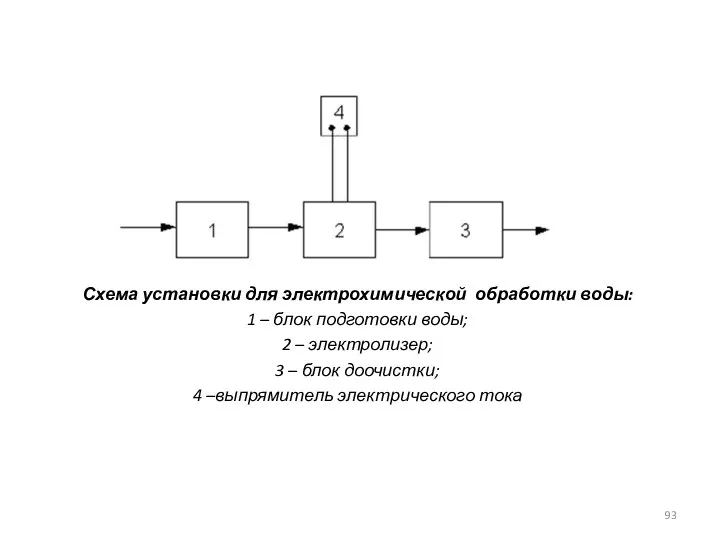
- 93. Схема установки для электрохимической обработки воды: 1 – блок подготовки воды; 2 – электролизер; 3 –
- 94. Количество вещества, прореагировавшего на электродах при пропускании постоянного электрического тока по закону Фарадея, прямо пропорционально силе
- 95. Потребляемая мощность, Вт, электролизера определяется по зависимости: Nпотр = ηэI Uэ где ηэ – коэффициент полезного
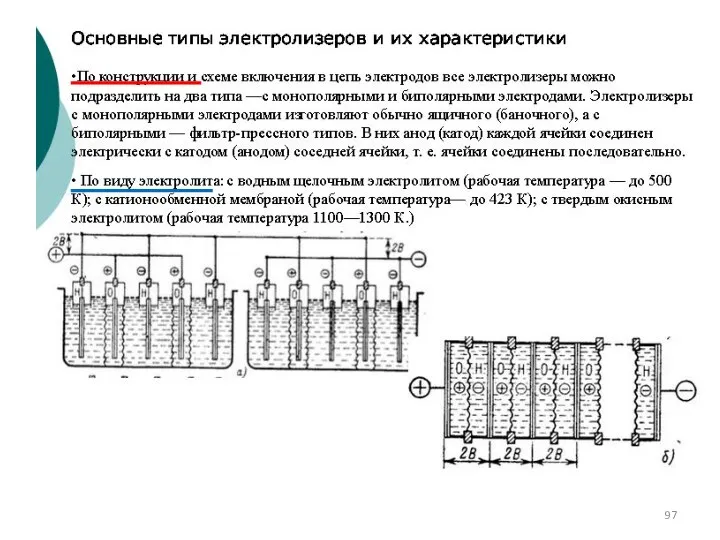
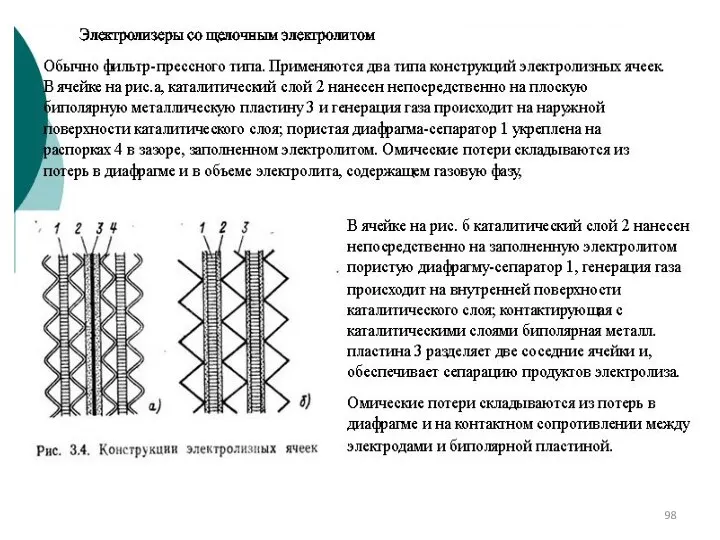
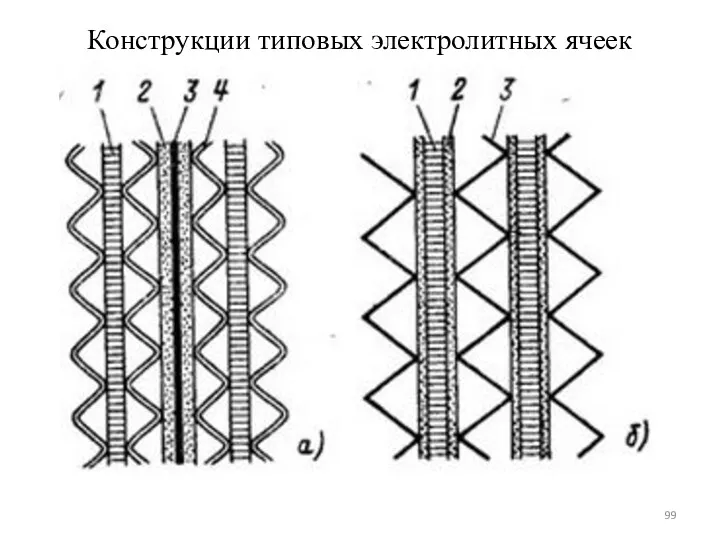
- 99. Конструкции типовых электролитных ячеек
- 102. Проблемы при использовании разного типа диафрагм
- 106. Металлогидриды
- 107. Интерметаллические соединения (ИМС)
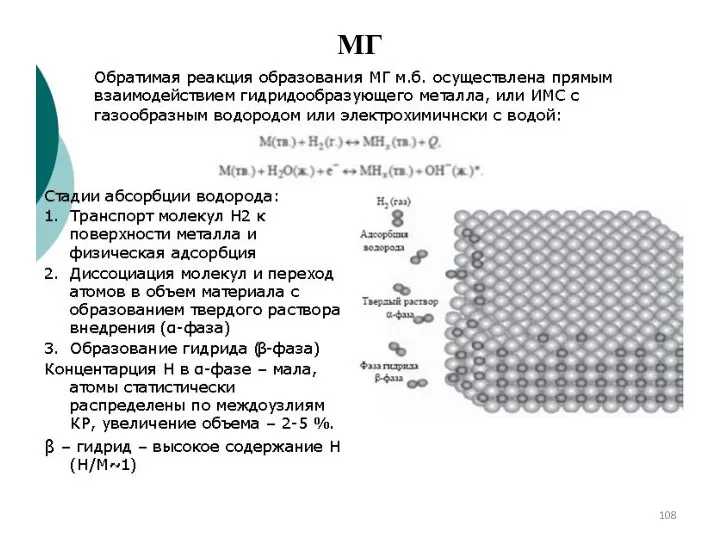
- 108. МГ
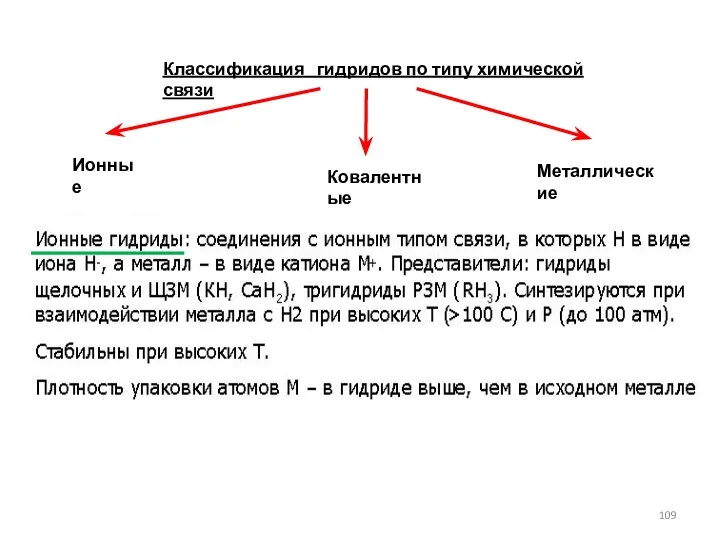
- 109. Классификация гидридов по типу химической связи Ионные Ковалентные Металлические
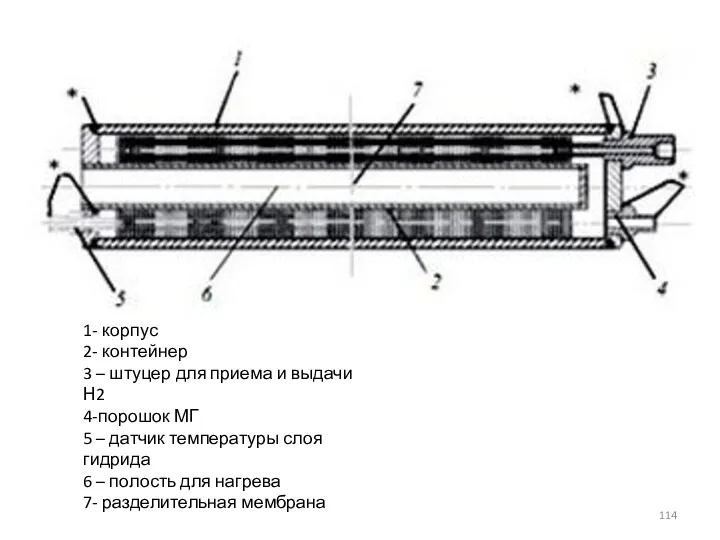
- 114. 1- корпус 2- контейнер 3 – штуцер для приема и выдачи Н2 4-порошок МГ 5 –
- 121. Скачать презентацию



















































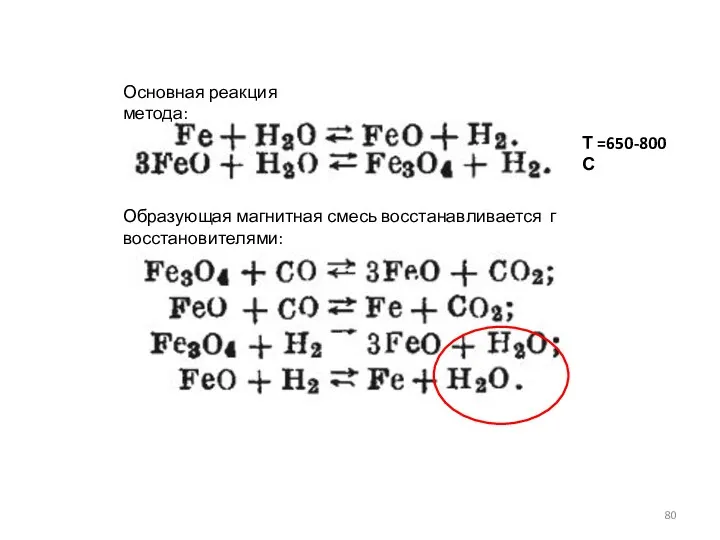





























 Титриметрический метод анализа
Титриметрический метод анализа Спирти. Загальні відомості про спирти
Спирти. Загальні відомості про спирти Периодическая система Д. И. Менделеева
Периодическая система Д. И. Менделеева Мектепте химия пәнінен олипиядалық есептерді шешуде иондар қасиеттерінің маңызы
Мектепте химия пәнінен олипиядалық есептерді шешуде иондар қасиеттерінің маңызы Общая схема радиолиза алифатических углеводородов. Радиолиз органических кислот. Радиолиз кетонов эфиров
Общая схема радиолиза алифатических углеводородов. Радиолиз органических кислот. Радиолиз кетонов эфиров Как и где используется соляная кислота
Как и где используется соляная кислота Теория строения органических соединений. Лекция 17
Теория строения органических соединений. Лекция 17 Силикаты (класс). Подкласс филлосиликаты (слоистые/листовые силикаты). Семейство слюды
Силикаты (класс). Подкласс филлосиликаты (слоистые/листовые силикаты). Семейство слюды Nuclear Energy, Controlled Fission and Fusion 2016
Nuclear Energy, Controlled Fission and Fusion 2016 Галогены. История открытия галогенов
Галогены. История открытия галогенов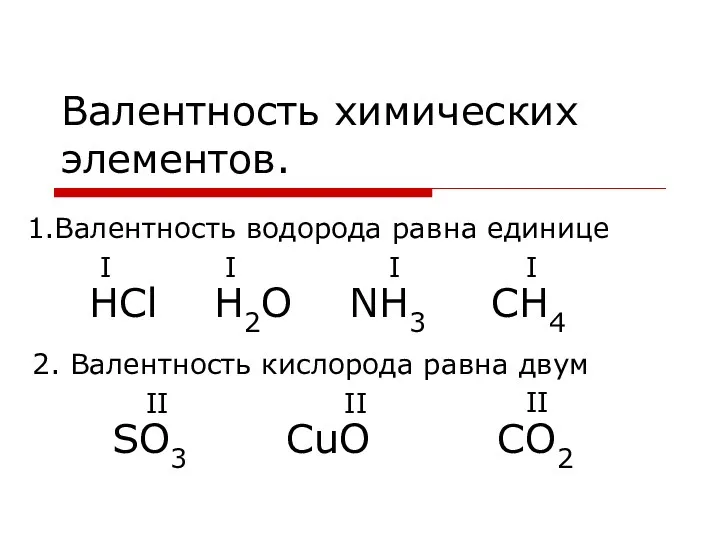 Валентность химических элементов
Валентность химических элементов Золото
Золото Перманганат калия
Перманганат калия Азот. Характеристика азота, фосфора (9класс)
Азот. Характеристика азота, фосфора (9класс) Катализ и катализаторы
Катализ и катализаторы Сполуки основних класів у будівництві і побуті
Сполуки основних класів у будівництві і побуті Метанол. Фізичні властивості
Метанол. Фізичні властивості Тепловой эффект химических реакций
Тепловой эффект химических реакций Получение и применение альдегидов
Получение и применение альдегидов Процесс электролиза
Процесс электролиза Бытовые химические товары. Особенности упаковки, маркировки товаров бытовой химии
Бытовые химические товары. Особенности упаковки, маркировки товаров бытовой химии Фуллерен С60 и его аналоги
Фуллерен С60 и его аналоги Формы залегания метаморфических пород
Формы залегания метаморфических пород Цікаві факти про хімію
Цікаві факти про хімію Задачи на избыток-недостаток
Задачи на избыток-недостаток Розчин та його компоненти
Розчин та його компоненти Кристалічний і аморфний стани твердих речовин
Кристалічний і аморфний стани твердих речовин Межлабораторные сравнительные испытания качественных параметров нефтепродуктов
Межлабораторные сравнительные испытания качественных параметров нефтепродуктов