Содержание
- 2. «ЗИМНЯЯ НОЧЬ» Б.ПАСТЕРНАК Мело, мело по всей земле Во все пределы. Свеча горела на столе, Свеча
- 3. ХИМИЧЕСКИЙ ЭКСПЕРИМЕНТ Zn + 2HCl = ZnCl2 + H2↑ + Q Признаками проводимой реакции будут выделение
- 4. Количество теплоты, которое выделяется или поглощается при химической реакции, называют тепловым эффектом реакции. Тепловой эффект обозначается
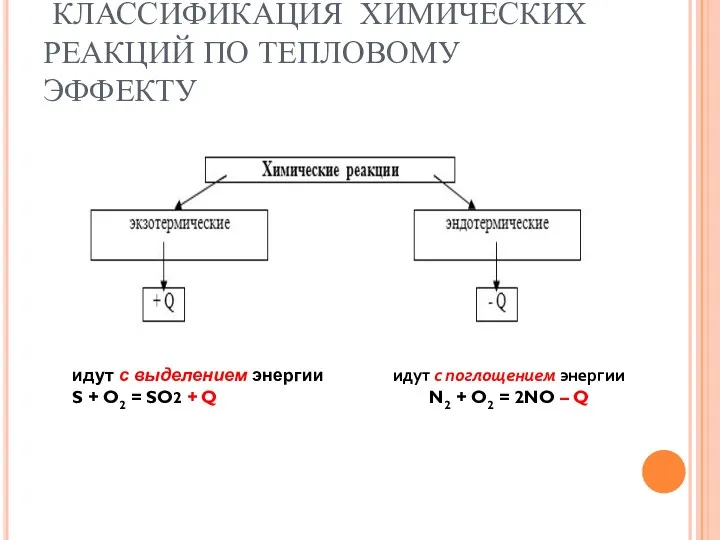
- 5. КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ ПО ТЕПЛОВОМУ ЭФФЕКТУ идут с выделением энергии S + O2 = SO2 +
- 6. ОТ ГРЕЧЕСКОГО «ЭНДО-» «ЭКЗО-» ВНУТРЬ НАРУЖУ
- 7. Химические уравнения, в которых указывается тепловой эффект, называют термохимическими. Например: 2HgO —> 2Hg + O2 –
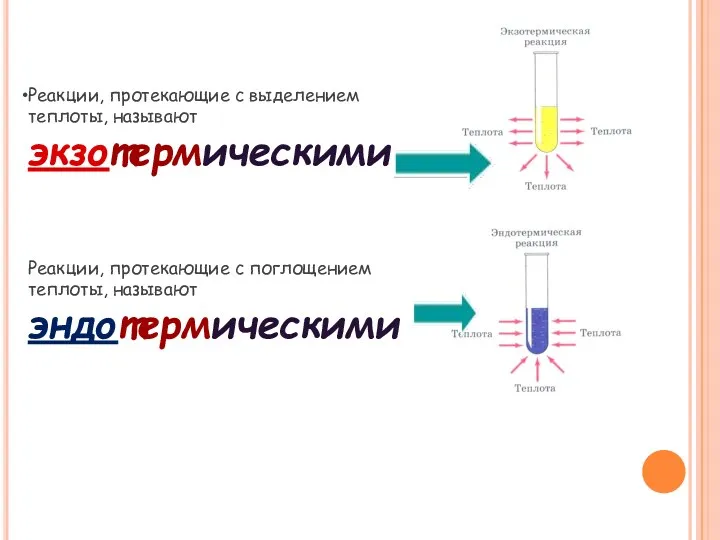
- 8. Реакции, протекающие с выделением теплоты, называют экзотермическими Реакции, протекающие с поглощением теплоты, называют эндотермическими
- 9. ГЕРМАН ИВАНОВИЧ ГЕСС -Российский академик -Основоположник термохимии Термохимия — раздел химии, в задачу которого входит определение
- 10. АЛГОРИТМ РЕШЕНИЯ ЗАДАЧ ПО ТЕРМОХИМИЧЕСКОМУ УРАВНЕНИЮ Кратко записать условия задачи (“дано”). Записать термохимическое уравнение реакции (ТХУ),
- 14. ЗАПОЛНИ ПРОПУСКИ 1. Реакции, протекающие с выделением теплоты и света называются реакциями ….. а) разложения; б)
- 15. 2. Какие схемы можно назвать термохимическими уравнениями реакций? а) 2 H2(г) + O2(г) = 2 H2О(ж)
- 16. 3. Какая запись, соответствует эндотермической реакции? а) С(тв) + O2(г) = СO2(г) + 394 кДж б)
- 17. 4. Приведены уравнения реакций: 1. С+О2 = СО2 + 402,24кДж 2. 2HgO = 2Hg + О2
- 19. Скачать презентацию













 Вода
Вода Строение атома
Строение атома Железо и его соединения
Железо и его соединения Особенности строения соединений органической химии. 10 класс
Особенности строения соединений органической химии. 10 класс Історія відкриття періодичної системи хімічних елементів
Історія відкриття періодичної системи хімічних елементів Основы химмотологии моторных топлив. Тема 3
Основы химмотологии моторных топлив. Тема 3 Prezentatciya
Prezentatciya Растворы. Основные понятия. Концентрация. Законы Рауля
Растворы. Основные понятия. Концентрация. Законы Рауля Кислородсодержащие соединения азота
Кислородсодержащие соединения азота Аналитическая химия стойких органических загрязнителей
Аналитическая химия стойких органических загрязнителей Получение каталитического слоя на основе углеродных нанотрубок с наночастицами платины для водородно–воздушных топливных элементов
Получение каталитического слоя на основе углеродных нанотрубок с наночастицами платины для водородно–воздушных топливных элементов Периодическая система химических элементов Д.И. Менделеева. Строение атома
Периодическая система химических элементов Д.И. Менделеева. Строение атома Окисно-відновні реакції, їхнє значення. Складання найпростіших окисно-відновних реакцій, добір коефіцієнтів
Окисно-відновні реакції, їхнє значення. Складання найпростіших окисно-відновних реакцій, добір коефіцієнтів Химический элемент. Изотопы. 11 класс
Химический элемент. Изотопы. 11 класс Непредельные углеводороды
Непредельные углеводороды Аминокислоты. Пептиды. Хроматографические методы исследования
Аминокислоты. Пептиды. Хроматографические методы исследования Воздух и его состав
Воздух и его состав Поверхностный мембранный потенциал. Равновесие Доннана
Поверхностный мембранный потенциал. Равновесие Доннана Трансмиссионные масла
Трансмиссионные масла Одноатомные спирты. Глицерин
Одноатомные спирты. Глицерин Неметаллические материалы
Неметаллические материалы Углеводы. Общая характеристика углеводов
Углеводы. Общая характеристика углеводов Полимеры органические и неорганические
Полимеры органические и неорганические Первоначальные представления об органических веществах
Первоначальные представления об органических веществах Металлы. Свойства металлов
Металлы. Свойства металлов Алканы. Получение, свойства и применение
Алканы. Получение, свойства и применение Общая характеристика металлов
Общая характеристика металлов Кислоты, их состав и названия
Кислоты, их состав и названия