Слайд 2
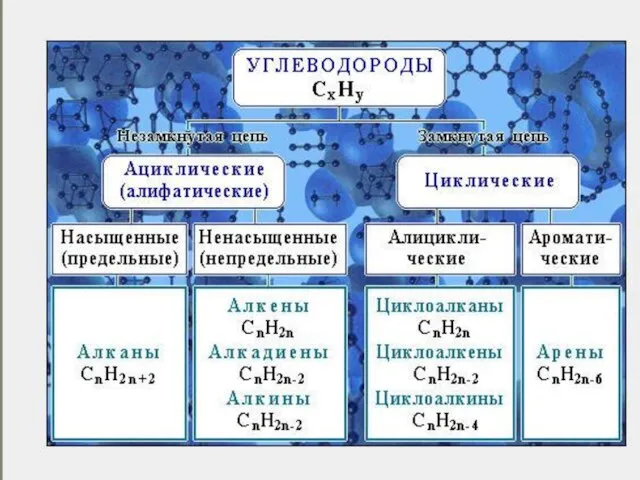
Слайд 3
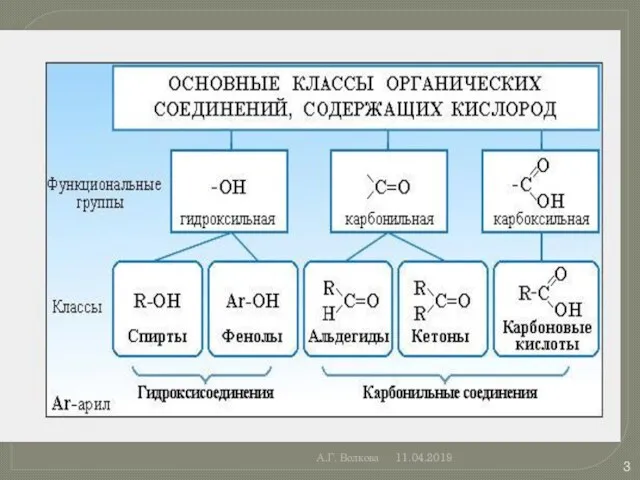
Слайд 4
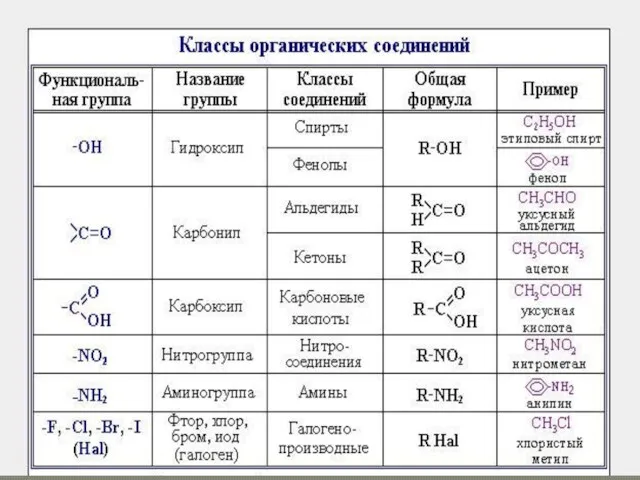
Слайд 5

А.Г. Волкова
11.04.2019
План урока
Классификация спиртов
Номенклатура спиртов
Изомерия спиртов
Отдельные представители
Метанол
Этанол
Этиленгликоль
Глицерин
Слайд 6

А.Г. Волкова
11.04.2019
Определение
Спирты́ (устаревшее алкого́ли) — органические соединения, содержащие одну или
несколько гидроксильных групп (гидроксил, OH),непосредственно связанных с атомом углерода в углеводородном радикале.
Общая формула спиртов СxHy(OH)n.
Слайд 7

А.Г. Волкова
11.04.2019
Классификация спиртов
Слайд 8

А.Г. Волкова
11.04.2019
Классификация спиртов
Слайд 9
А.Г. Волкова
11.04.2019
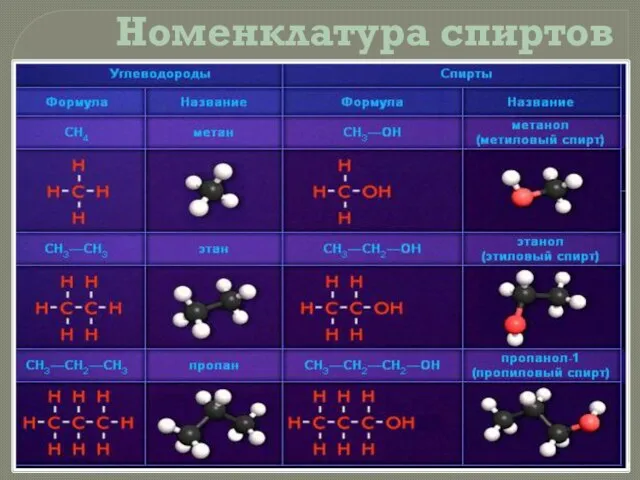
Номенклатура спиртов
Слайд 10

А.Г. Волкова
11.04.2019
Названия одноатомных спиртов образуются из названия углеводорода с самой длинной
углеродной цепью, содержащей гидроксильную группу, путём добавления суффикса -ол.
Для многоатомных спиртов перед суффиксом -ол по-гречески (-ди-, -три-, ...) указывается количество гидроксильных групп.
Например: CH3-CH2-OH этанол
Слайд 11
А.Г. Волкова
11.04.2019
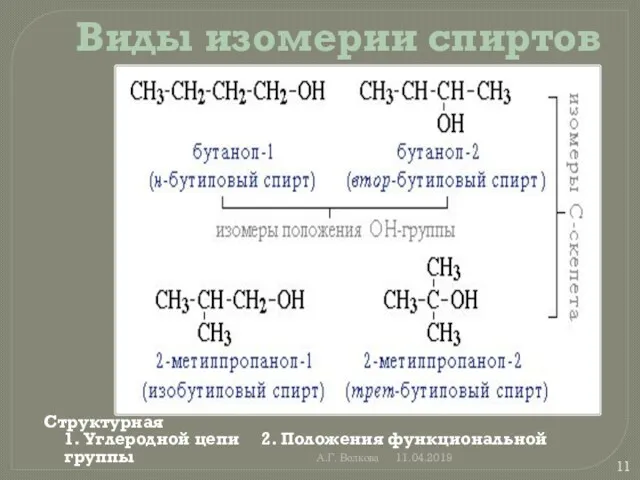
Виды изомерии спиртов
Структурная
1. Углеродной цепи 2. Положения функциональной группы
Слайд 12
А.Г. Волкова
11.04.2019
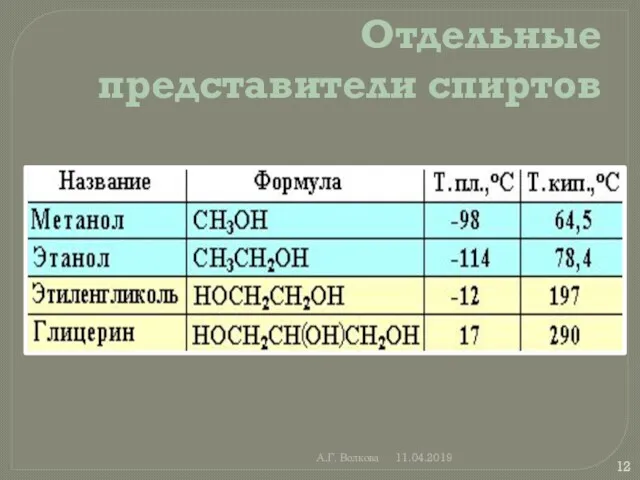
Отдельные представители спиртов
Слайд 13

А.Г. Волкова
11.04.2019
Одноатомный спирт - метанол
Жидкость без цвета с температурой кипения 64С,
характерным запахом Легче воды. Горит бесцветным пламенем.
Применяется в качестве растворителя и
топлива в двигателях внутреннего сгорания.
Слайд 14

А.Г. Волкова
11.04.2019
Метанол - яд
Ядовитое действие метанола основано на поражении нервной и
сосудистой системы. Приём внутрь 5—10 мл метанола приводит к тяжёлому отравлению, а 30 мл и более — к смерти.
Слайд 15

А.Г. Волкова
11.04.2019
Одноатомный спирт - этанол
Бесцветная жидкость с характерным запахом и жгучим
вкусом, температурой кипения78С. Легче воды. Смешивается с ней в любых отношениях.
Легко воспламеняется, горит слабо светящимся голубоватым пламенем.
Слайд 16

А.Г. Волкова
11.04.2019
Применение этанола
приготовлении различных
спиртных напитков.
приготовление экстрактов из лекарственных
растений
для дезинфекции.
растворитель
для духов и лосьонов.
Слайд 17

А.Г. Волкова
11.04.2019
Вредное воздействие этанола
В начале опьянения страдают структуры коры больших
полушарий; активность центров мозга, управляющих поведением, подавляется: утрачивается разумный контроль над поступками, снижается критическое отношение к себе. И. П. Павлов называл такое состояние «буйством подкорки».
При очень большом содержании алкоголя в крови угнетается активность двигательных центров мозга, главным образом страдает функция мозжечка - человек полностью теряет ориентацию.
Слайд 18

А.Г. Волкова
11.04.2019
Вредное воздействие этанола
Алкоголь крайне неблагоприятно влияет на сосуды головного мозга.
В начале опьянения они расширяются, кровоток в них замедляется, что приводит к застойным явлениям в головном мозге. Затем, когда в крови помимо алкоголя начинают накапливаться вредные продукты его неполного распада, наступает резкий спазм, сужение сосудов, развиваются такие опасные осложнения, как мозговые инсульты, приводящие к тяжелой инвалидности и даже смерти.
Слайд 19

А.Г. Волкова
11.04.2019
Многоатомный спирт -этиленгликоль
— представитель предельных двухатомных спиртов — гликолей.
Название
гликоли получили вследствие сладкого вкуса многих представителей ряда (греч. «гликос» — сладкий).
- это сиропообразная жидкость сладкого вкуса, без запаха, ядовит. Хорошо смешивается с водой и спиртом, гигроскопичен.
Слайд 20

А.Г. Волкова
11.04.2019
Применение этиленгликоля
применяется как компонент автомобильных антифризов и незамерзающих жидкостей.
применяется для
получения лавсана (ценного синтетического волокна).
Слайд 21

А.Г. Волкова
11.04.2019
Этиленгликоль - яд
Дозы вызывающие смертельное отравление этиленгликолем для человека
является 50-150 мл. Смертность при поражении этиленгликолем очень высока и составляет более 60% всех случаев отравления.
Слайд 22

А.Г. Волкова
11.04.2019
Многоатомный спирт - глицерин
– трехатомный предельный спирт.
Бесцветная, вязкая, гигроскопичная,
сладкая на вкус жидкость. Смешивается с водой в любых отношениях , хороший растворитель.
Реагирует с азотной кислотой с образованием нитроглицерина.
С карбоновыми кислотами образует жиры и масла.
Слайд 23

А.Г. Волкова
11.04.2019
Применение глицерина
в производстве взрывчатых веществ нитроглицерина.
при обработке кожи.
компонент некоторых
клеёв.
производсто пластмасс
производство кондитерских изделий и напитков (как пищевая добавка E422).
Слайд 24
А.Г. Волкова
11.04.2019
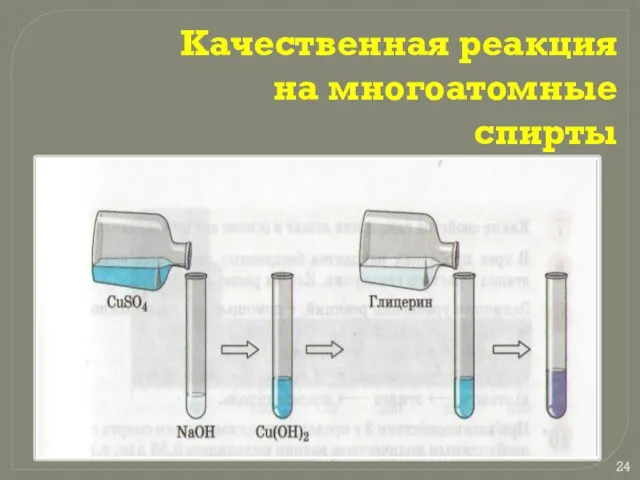
Качественная реакция на многоатомные спирты
Слайд 25

А.Г. Волкова
11.04.2019
Реакцией на многоатомные спирты является их взаимодействие со свежеполученным осадком
гидроксида меди (II), который растворяется с образованием яркого сине-фиолетового раствора.
Слайд 26

А.Г. Волкова
11.04.2019
Домашнее задание
П. 35
? 1, 3, 5б

























 Угарный газ
Угарный газ Коррозия и защита строительных материалов
Коррозия и защита строительных материалов Простые вещества. Игра Счастливый случай
Простые вещества. Игра Счастливый случай Химия в повседневной жизни человека
Химия в повседневной жизни человека Жидкокристаллические композиты ЖКК. Керамические композиционные материалы (ККМ). Углерод-углеродные композиционные (УУКМ)
Жидкокристаллические композиты ЖКК. Керамические композиционные материалы (ККМ). Углерод-углеродные композиционные (УУКМ) Простейшие представления о кинетике химических реакций
Простейшие представления о кинетике химических реакций Органическая химия
Органическая химия Кинетическое уравнение математическая запись закона действующих масс
Кинетическое уравнение математическая запись закона действующих масс Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Необоротні і оборотні хімічні процеси. Хімічна рівновага
Необоротні і оборотні хімічні процеси. Хімічна рівновага Химический элемент V группы: сурьма
Химический элемент V группы: сурьма Интоксикация ртутью
Интоксикация ртутью Качественные реакции на органические вещества
Качественные реакции на органические вещества Crystal Defects and Noncrystalline Structure–Imperfection
Crystal Defects and Noncrystalline Structure–Imperfection Аномальные свойства воды – основа жизни на Земле
Аномальные свойства воды – основа жизни на Земле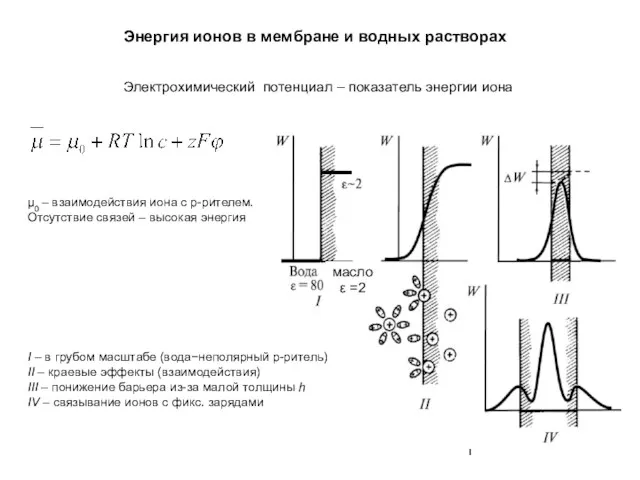 Энергия ионов в мембране и водных растворах
Энергия ионов в мембране и водных растворах Основные особенности композитов по сравнению с традиционными материалами
Основные особенности композитов по сравнению с традиционными материалами Карбонильные соединения
Карбонильные соединения Углерод. Физические и химические свойства
Углерод. Физические и химические свойства Химическая связь
Химическая связь Металлы II группы главной подгруппы
Металлы II группы главной подгруппы Паровые зоны в гидротермальных системах
Паровые зоны в гидротермальных системах Алкадиены. Диеновые углеводороды
Алкадиены. Диеновые углеводороды Состояние атмосферного воздуха в Ярославской области
Состояние атмосферного воздуха в Ярославской области Теплота горения
Теплота горения Ionic polymerization
Ionic polymerization Химия. Изучение жиров
Химия. Изучение жиров Сутектік көрсеткіш ph. Тұздар гидролизі
Сутектік көрсеткіш ph. Тұздар гидролизі