Содержание
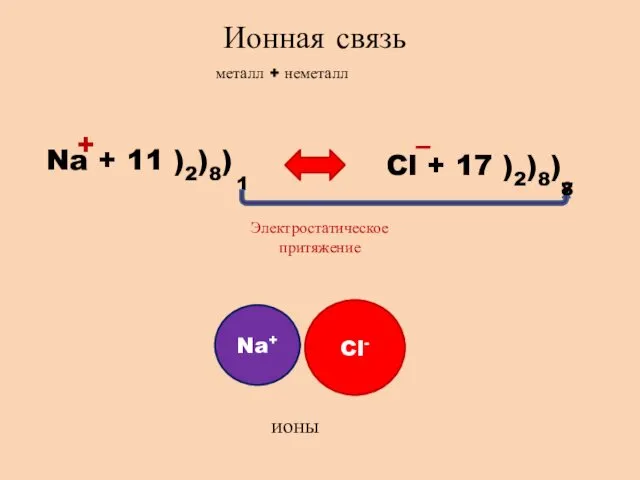
- 2. Ионная связь металл + неметалл Na + 11 )2)8) 1 Cl + 17 )2)8) 7 8
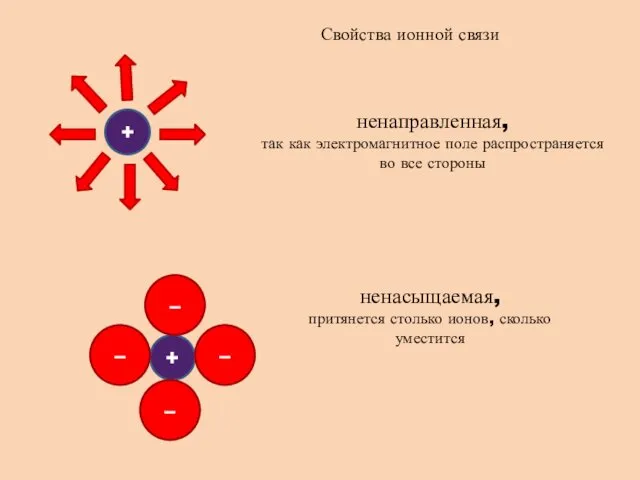
- 3. Свойства ионной связи ненаправленная, так как электромагнитное поле распространяется во все стороны ненасыщаемая, притянется столько ионов,
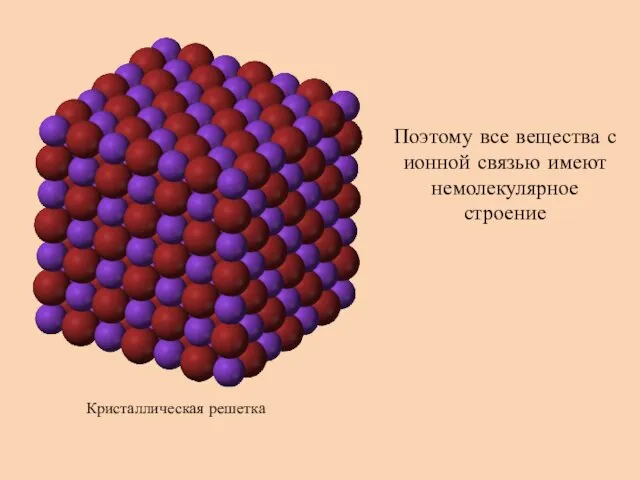
- 4. Поэтому все вещества с ионной связью имеют немолекулярное строение Кристаллическая решетка
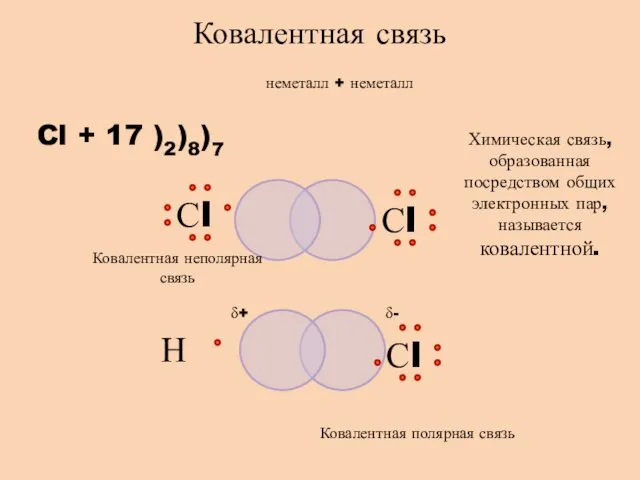
- 5. неметалл + неметалл Cl + 17 )2)8)7 Ковалентная связь Химическая связь, образованная посредством общих электронных пар,
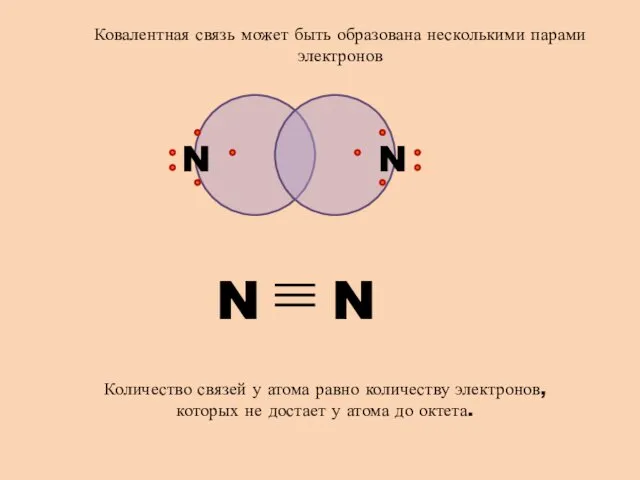
- 6. N N Ковалентная связь может быть образована несколькими парами электронов Количество связей у атома равно количеству
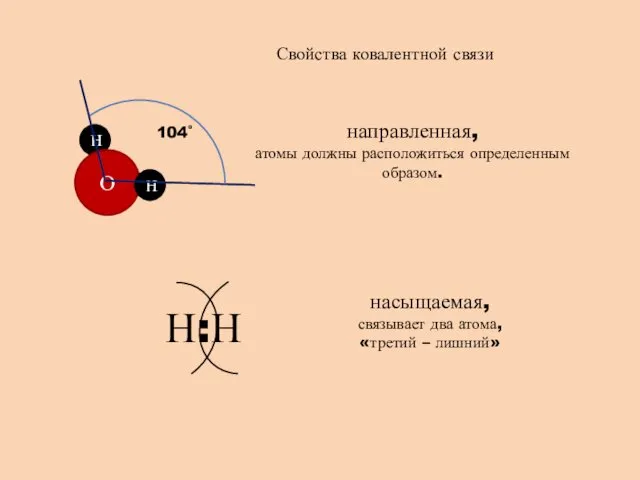
- 7. Свойства ковалентной связи направленная, атомы должны расположиться определенным образом. насыщаемая, связывает два атома, «третий – лишний»
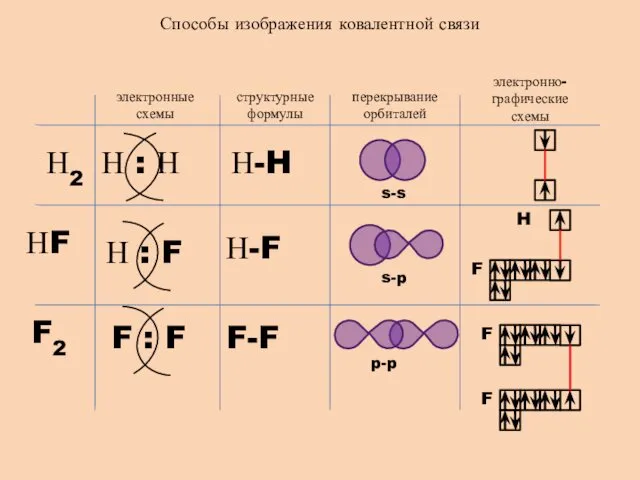
- 8. Способы изображения ковалентной связи электронные схемы структурные формулы перекрывание орбиталей электронно-графические схемы Н2 НF F2 Н-F
- 9. + + + + + + + + + + + + + + + +
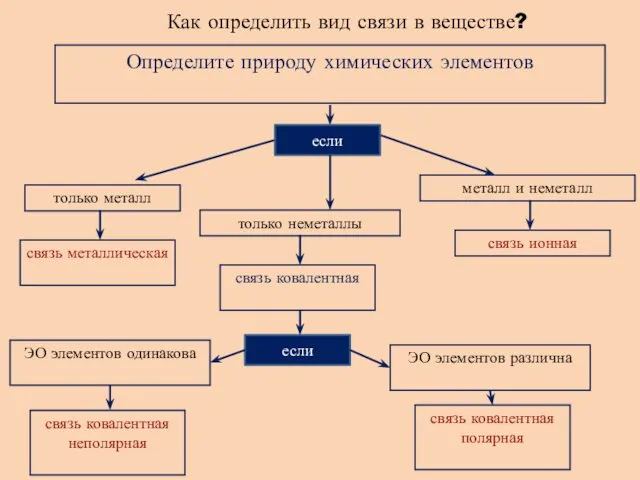
- 10. Как определить вид связи в веществе? Определите природу химических элементов если только металл только неметаллы металл
- 11. Определите вид связи в следующих веществах: Н2, Na, NaF, H2S, NH3, O2, Zn, CaS, Mg3N2, CH4,
- 13. Скачать презентацию

 Химический элемент радий
Химический элемент радий Основания. Классификация оснований
Основания. Классификация оснований Реакции электрофильного замещения в ароматическом ряду Se
Реакции электрофильного замещения в ароматическом ряду Se Главная подгруппа IV группы
Главная подгруппа IV группы Алкадиены (диеновые углеводороды)
Алкадиены (диеновые углеводороды) Свойства моторных топлив
Свойства моторных топлив Соли. Классификация. Физические и химические свойства. Получение и применение солей
Соли. Классификация. Физические и химические свойства. Получение и применение солей Химия и обмен углеводов. Функции углеводов
Химия и обмен углеводов. Функции углеводов Азотовмисні та елементоорганічні сполуки
Азотовмисні та елементоорганічні сполуки Физико-химия полимеров и их растворов
Физико-химия полимеров и их растворов Азотная кислота. К уроку химии для 9 класса
Азотная кислота. К уроку химии для 9 класса Тірі ағзада жүретін процесстер – физика-химиялық интерпретация
Тірі ағзада жүретін процесстер – физика-химиялық интерпретация Колоїдний захист
Колоїдний захист Алюминий и его соединения
Алюминий и его соединения Матеріальний баланс процесу горіння. Основні поняття матеріального балансу горіння
Матеріальний баланс процесу горіння. Основні поняття матеріального балансу горіння Содержание кислорода и углекислого газа в помещениях школы
Содержание кислорода и углекислого газа в помещениях школы Конструкционные функциональные волокнистые композиты. Углеродные волокна
Конструкционные функциональные волокнистые композиты. Углеродные волокна Основания. Состав, классификация, свойства, получение
Основания. Состав, классификация, свойства, получение Основные химические понятия
Основные химические понятия Интоксикации сельскохозяйственными ядохимикатами (пестицидами)
Интоксикации сельскохозяйственными ядохимикатами (пестицидами) Химическая кинетика
Химическая кинетика Классификация органических реакций
Классификация органических реакций Строение электронных оболочек атомов
Строение электронных оболочек атомов Алкены
Алкены Основные понятия и законы химии. Тема1
Основные понятия и законы химии. Тема1 Карбон қышқылдар, түрлері қасиеттері, түындылары. Лекция № 8. Гетерофункционалды қосылыстар. Лекция № 9
Карбон қышқылдар, түрлері қасиеттері, түындылары. Лекция № 8. Гетерофункционалды қосылыстар. Лекция № 9 Осадительное титрование. Меркуриметрия
Осадительное титрование. Меркуриметрия Общая характеристика неметаллов
Общая характеристика неметаллов