Содержание
- 2. Азотистая кислота Фосфорная кислота Кремниевая кислота Угольная кислота Гидроксид железа (III) Оксид азота (II)
- 3. Ответы −MgO, – SO2, – Al(OH)3, −HCl, −KOH, −H2SO4
- 4. В нашей лаборатории расцвёл цветок необычайной красоты – на его лепестках – формулы веществ. Расклассифицируйте вещества
- 5. Соли. Классификация. Физические и химические свойства. Получение и применение солей.
- 6. Цели урока: 1)Познакомить учащихся с понятием соли, изучить основные классификации солей; 2)Изучить основные химические свойства солей;
- 7. NaСI Са3(РО4)2 CaCO3
- 8. Что такое соли? Соли–это сложные вещества, образованные атомами металлов и кислотными остатками
- 9. Номенклатура солей Название Название Указание Кислотного + металла (в Р.п.) + валентности остатка (если она переменная)
- 10. Попробуйте сами дать названия следующим солям: KCI CaCI2 BaCO3
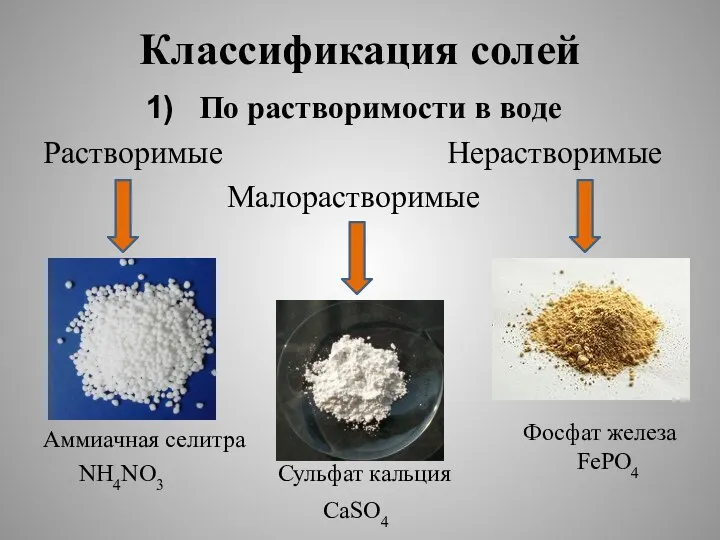
- 11. Классификация солей По растворимости в воде Растворимые Нерастворимые Малорастворимые Аммиачная селитра NH4NO3 Сульфат кальция Фосфат железа
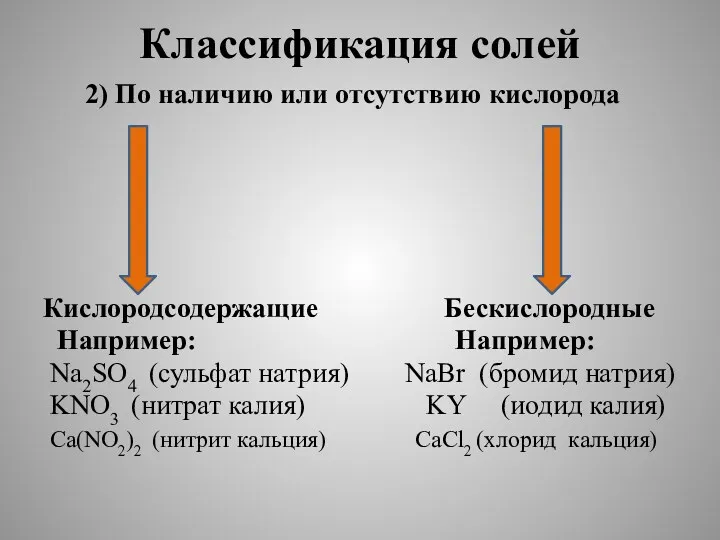
- 12. Классификация солей 2) По наличию или отсутствию кислорода Кислородсодержащие Бескислородные Например: Например: Na2SO4 (сульфат натрия) NaBr
- 13. Классификация солей Соли Средние (нормальные) Кислые Основные
- 14. Разновидности солей Соли бывают: Средние соли – это продукты полного замещения атомов водорода в кислоте на
- 15. Разновидности солей 2) Кислые соли – это продукты неполного замещения атомов водорода в кислоте на металл.
- 16. Разновидности солей 3) Основные соли – это продукты неполного замещения гидроксогрупп в основании на кислотный остаток.
- 17. Физические свойства: Все соли твердые кристаллические вещества. Соли имеют различную окраску, и разную растворимость в воде.
- 18. Написать названия солей 1. NaCl 2. CaCO3 3. Са3(РО4)2 4. МgBr2 5. KNO2 6. CuSO4
- 19. Написать формулы солей 7. Сульфит бария 8. Силикат магния 9. Иодид калия 10. Фосфат цинка 11.
- 20. Химические свойства Соль + кислота = другая соль + другая кислота Например: H2SO4 + BaCl2 =
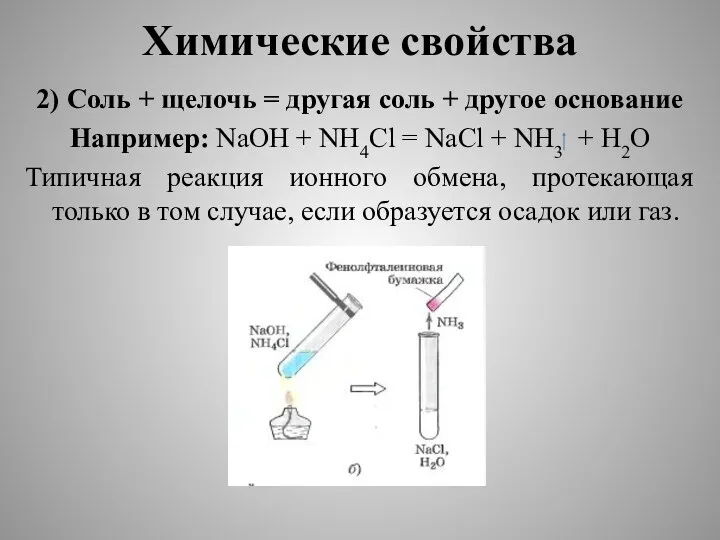
- 21. Химические свойства 2) Соль + щелочь = другая соль + другое основание Например: NaOH + NH4Cl
- 22. Химические свойства 3) Соль1 + соль2 = соль3 + соль4 Например: Na2SO4 + BaCl2 = BaSO4
- 23. Химические свойства 4) Соль + металл = другая соль + другой металл Например: CuSO4(p-p) + Fe
- 24. Получение солей: 1. Взаимодействие кислоты с Ме: Zn + 2HCI → ZnCI2 + H2 2. Взаимодействие
- 25. Применение солей - в стирке, с помощью порошка, с состав которого входит стиральная (кальцинированная) сода –
- 26. Мрамор, известняк, мел
- 27. ИЗДЕЛИЯ ИЗ МАЛАХИТА
- 28. Обобщение темы Тест «Как я запомнил тему»: 1) Выберите формулу соли: а) HCl б) Ca(OH)2 в)
- 29. . 4) К какому типу солей относится данная соль - AlOHCl2: а) средняя б) основная в)
- 30. Ответы: 1. в 2. г 3. б 4. б 5. в
- 31. Рефлексия
- 32. Домашнее задание: § 26 Упр. 6, 7 стр.115
- 34. Скачать презентацию

























 Карбоновые кислоты. Нахождение в природе
Карбоновые кислоты. Нахождение в природе Изомерия
Изомерия Гидролиз органических и неорганических веществ, солей
Гидролиз органических и неорганических веществ, солей Chemistry of Coordination Compounds
Chemistry of Coordination Compounds Тайна мыльного пузыря
Тайна мыльного пузыря Валентность и степень окисления химического элемента
Валентность и степень окисления химического элемента Растворы. (Лекция 7)
Растворы. (Лекция 7) Алкандар. Метан молекуласының құрылысы Метан және оның гомологтарының қасиеттері
Алкандар. Метан молекуласының құрылысы Метан және оның гомологтарының қасиеттері Диаграмма состояния Железо – Углерод. Материаловедение. Лекция 2
Диаграмма состояния Железо – Углерод. Материаловедение. Лекция 2 Теоретические основы количественного анализа
Теоретические основы количественного анализа Введение в минералогию. Генезис минералов
Введение в минералогию. Генезис минералов Подкласс Иносиликаты (цепочечные/ленточные силикаты)
Подкласс Иносиликаты (цепочечные/ленточные силикаты) Химическая связь
Химическая связь Теория электролитической диссоциации
Теория электролитической диссоциации Автомобильные бензины
Автомобильные бензины Ionic polymerization
Ionic polymerization Методы осаждения. Аналитическая химия
Методы осаждения. Аналитическая химия Степень окисления
Степень окисления Относительная молекулярная масса вещества. Задачи
Относительная молекулярная масса вещества. Задачи Спирты. Понятия о предельных одноатомных спиртах. Химические свойства этанола и его применение
Спирты. Понятия о предельных одноатомных спиртах. Химические свойства этанола и его применение Лекция Атомное строение твердых тел. 1-01
Лекция Атомное строение твердых тел. 1-01 Многоатомные спирты
Многоатомные спирты Химическая и электрическая работа систем с химическими реакциями. Устройства для проведения электрохимических реакций
Химическая и электрическая работа систем с химическими реакциями. Устройства для проведения электрохимических реакций Энергетический обмен
Энергетический обмен Химическое равновесие
Химическое равновесие Химия в продуктах питания
Химия в продуктах питания Твёрдое агрегатное состояние. Кристалические решетки. Урок 4
Твёрдое агрегатное состояние. Кристалические решетки. Урок 4 Расчеты по химическим уравнениям
Расчеты по химическим уравнениям