Спирты. Понятия о предельных одноатомных спиртах. Химические свойства этанола и его применение презентация
Содержание
- 2. План – конспект занятия Классификация спиртов Номенклатура спиртов Изомерия спиртов Отдельные представители Метанол Этанол Глицерин Свойства
- 3. Определение Спирты́ (устаревшее алкого́ли) — органические соединения, содержащие одну или несколько гидроксильных групп (гидроксил, OH),непосредственно связанных
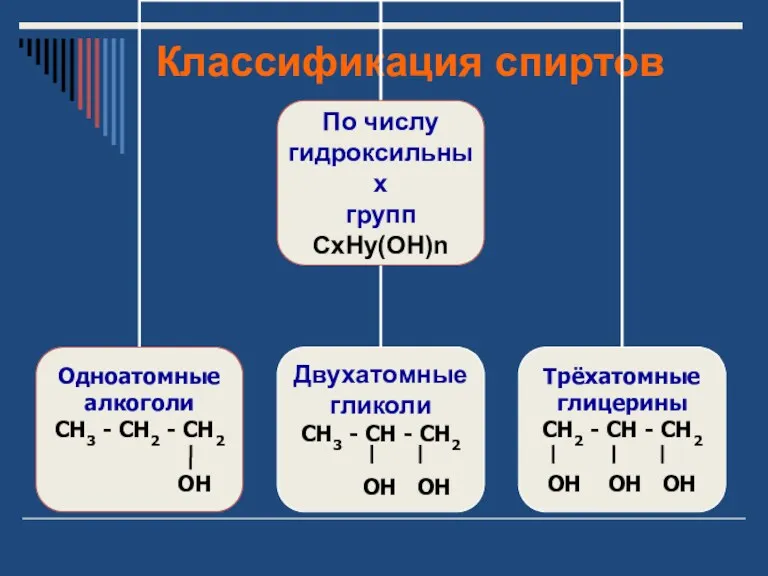
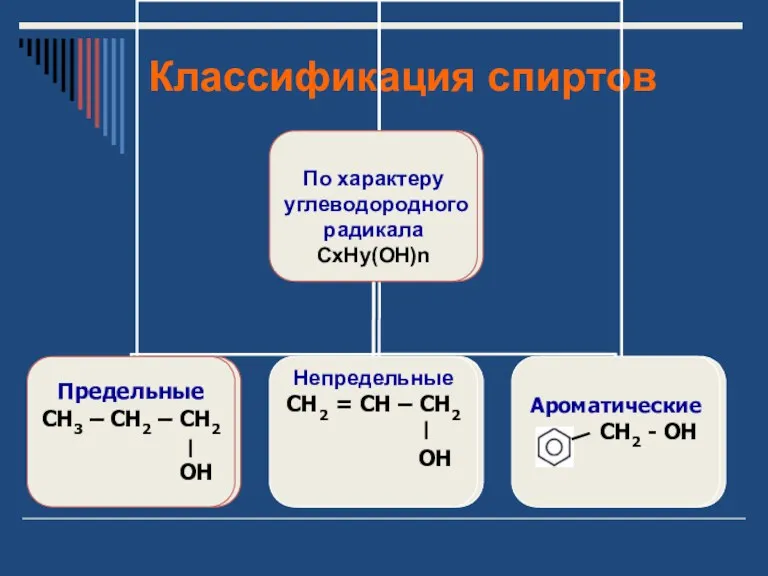
- 4. Классификация спиртов
- 5. Классификация спиртов
- 6. Классификация спиртов
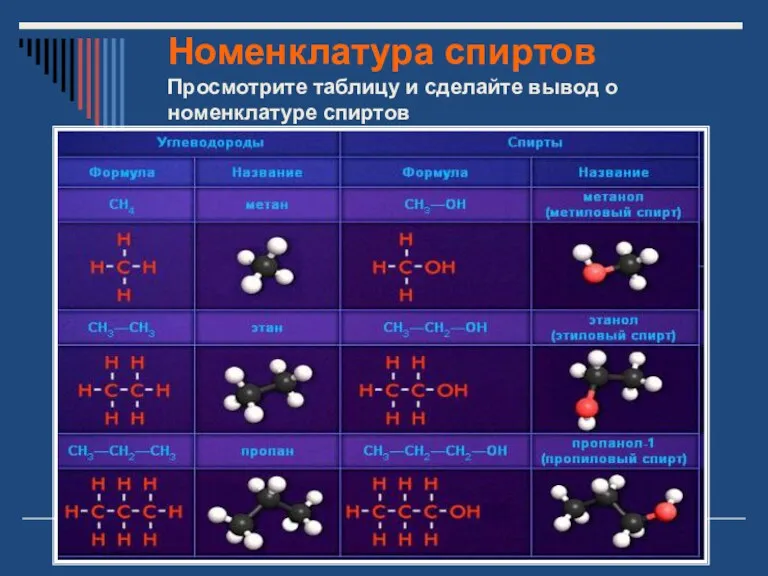
- 7. Номенклатура спиртов Просмотрите таблицу и сделайте вывод о номенклатуре спиртов
- 8. Вывод Названия одноатомных спиртов образуются из названия углеводорода с самой длинной углеродной цепью, содержащей гидроксильную группу,
- 9. Виды изомерии спиртов Структурная 1. Углеродной цепи 2. Положения функциональной группы
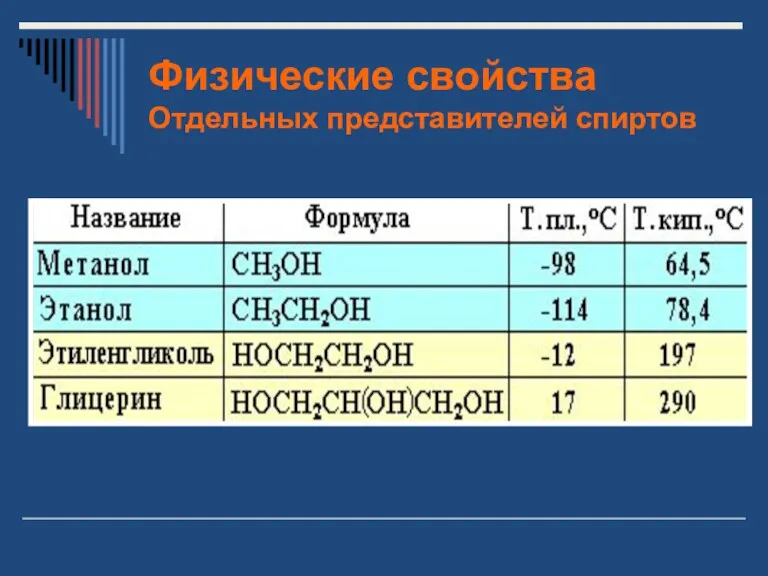
- 10. Физические свойства Отдельных представителей спиртов
- 11. Химические свойства: 1. Реакция замещения (Спирты проявляют кислотные свойства) а) Взаимодействие с натрием 2С2Н5ОН + 2Na
- 12. Химические свойства: 2. Дегидратации а) С2Н5ОН —> С2Н4 + Н2О этен б) С2Н5ОН + С2Н5ОН —>
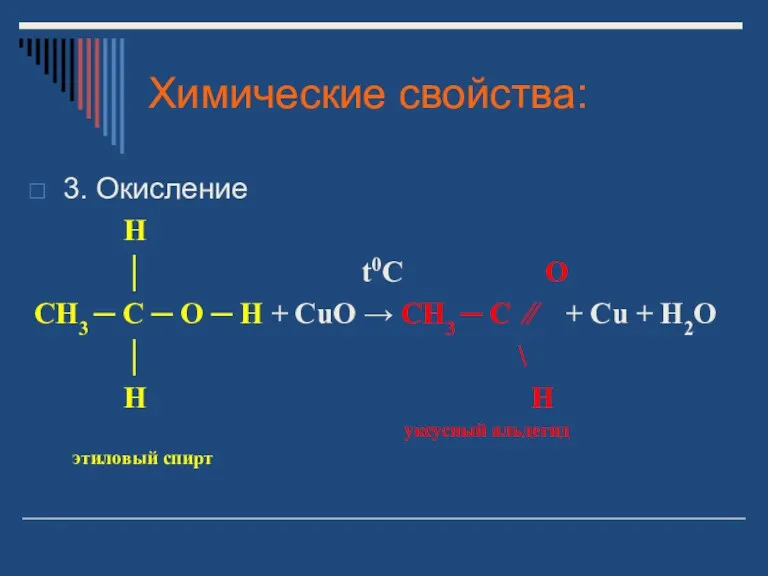
- 13. Химические свойства: 3. Окисление H │ t0C O CH3 ─ C ─ O ─ H +
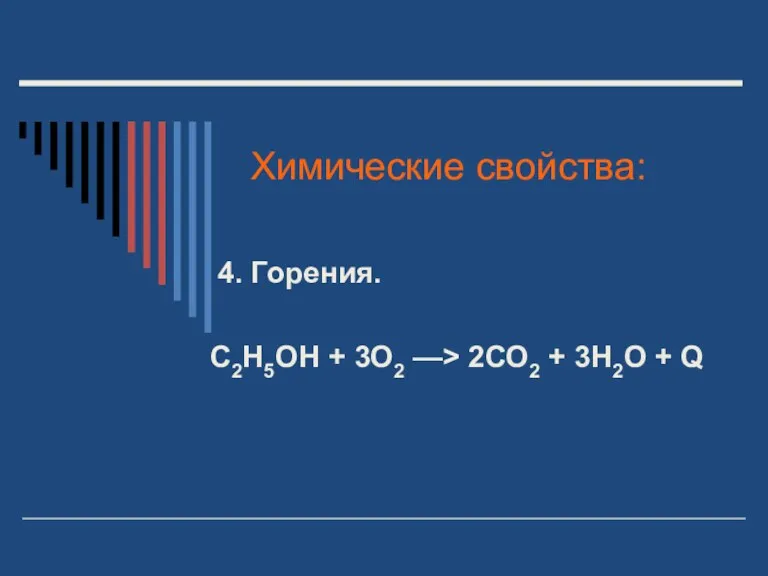
- 14. Химические свойства: 4. Горения. С2Н5ОН + 3О2 —> 2СО2 + 3Н2О + Q
- 15. Одноатомный спирт - метанол Жидкость без цвета с температурой кипения 64С, характерным запахом Легче воды. Горит
- 16. Метанол - яд Ядовитое действие метанола основано на поражении нервной и сосудистой системы. Приём внутрь 5—10
- 17. Одноатомный спирт - этанол Бесцветная жидкость с характерным запахом и жгучим вкусом, температурой кипения78С. Легче воды.
- 18. Применение этанола Этиловый спирт употребляется при приготовлении различных спиртных напитков. В медицине для приготовления экстрактов из
- 19. Многоатомный спирт - глицерин Глицерин – трехатомный предельный спирт. Бесцветная, вязкая, гигроскопичная, сладкая на вкус жидкость.
- 20. Многоатомный спирт - глицерин Простейший представитель многоатомных (трехатомных) спиртов - Глицерин По международной номенклатуре - Пропантриол-1,2,3
- 21. Химические свойства: 1. Глицерин является представителем трехатомных спиртов, для которых, как для гидроксилсодержащих соединений характерны те
- 22. Химические свойства 2.Нитрование тринитроглицерин
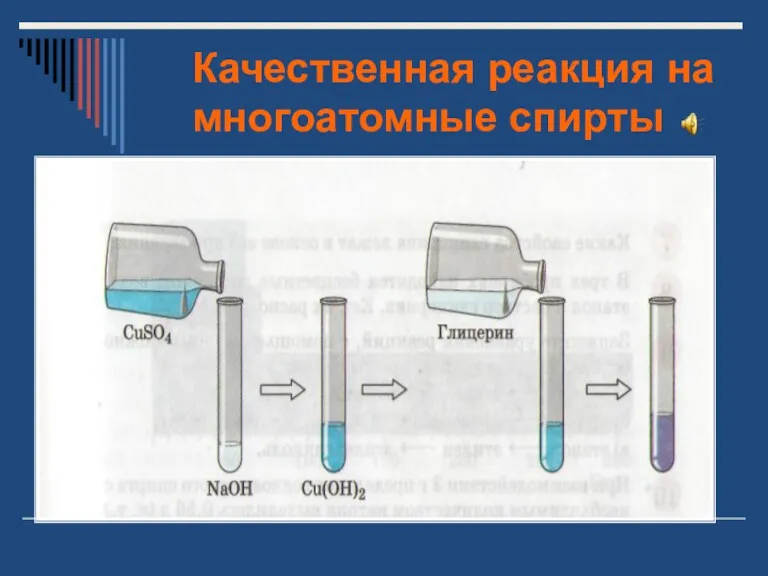
- 23. Качественная реакция на многоатомные спирты Глицерин имеет и специфические свойства, отличающие его от одноатомных спиртов: он
- 24. Качественная реакция на многоатомные спирты
- 25. Применение глицерина Применяется в производстве взрывчатых веществ нитроглицерина. При обработке кожи. Как компонент некоторых клеёв. При
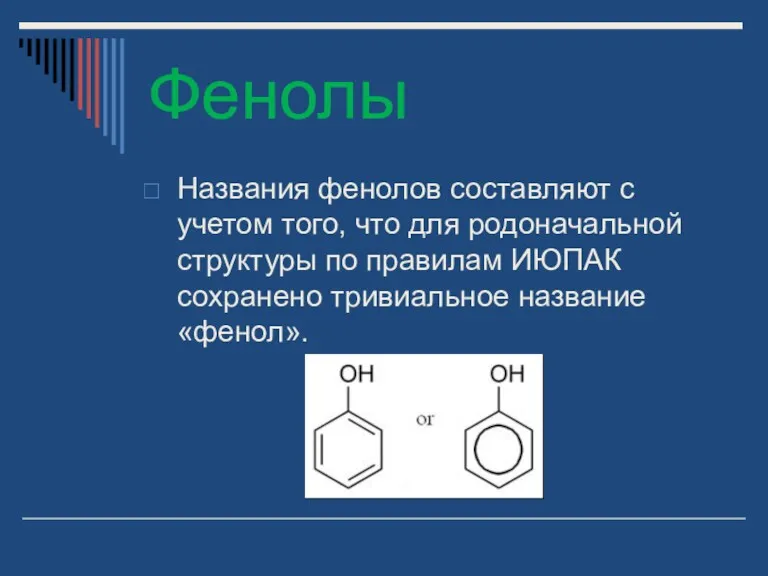
- 26. Фенолы Названия фенолов составляют с учетом того, что для родоначальной структуры по правилам ИЮПАК сохранено тривиальное
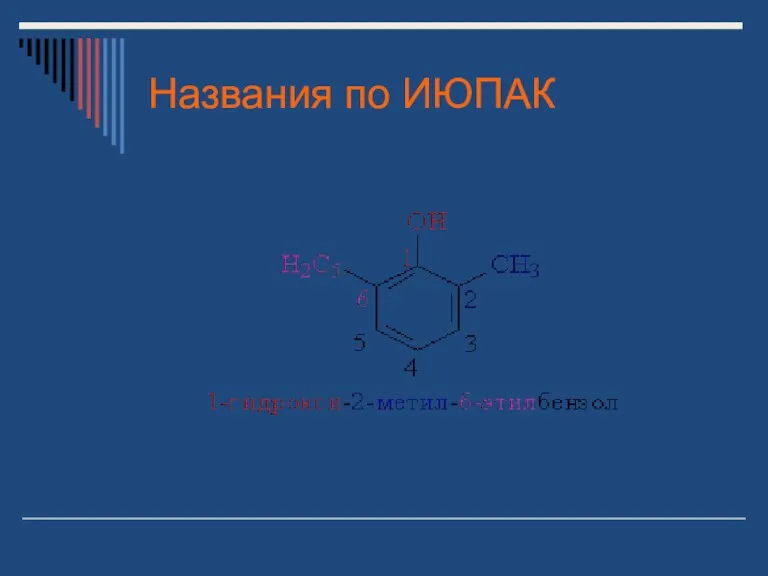
- 27. Номенклатура Нумерацию атомов углерода бензольного кольца начинают от атома, непосредственно связанного с гидроксильной группой (если она
- 28. Названия по ИЮПАК
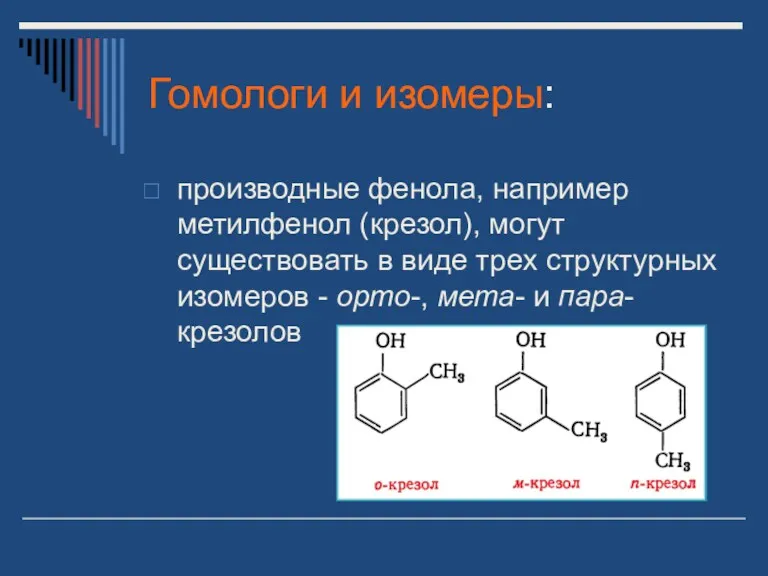
- 29. Гомологи и изомеры: производные фенола, например метилфенол (крезол), могут существовать в виде трех структурных изомеров -
- 30. Физические свойства. Фенолы в большинстве своем - кристаллические вещества (мета-крезол - жидкость) при комнатной температуре. Они
- 31. Химические свойства:
- 32. Химические свойства:
- 33. Химические свойства:
- 34. Химические свойства:
- 36. Задания Законспектировать занятие в рабочей тетради. Ответить на рабочую карту.
- 38. Скачать презентацию

























 Біріншілік алкилсульфаттар және алкилэтоксисульфаттарды алу
Біріншілік алкилсульфаттар және алкилэтоксисульфаттарды алу Синтетические топлива
Синтетические топлива Определение витамина “С” в продуктах питания с помощью иодометрии
Определение витамина “С” в продуктах питания с помощью иодометрии Геолого-промышленные типы месторождений полезных ископаемых
Геолого-промышленные типы месторождений полезных ископаемых Актиноиды. Физические и химические свойства
Актиноиды. Физические и химические свойства Этапы гравиметрического анализа. (Лекция 3)
Этапы гравиметрического анализа. (Лекция 3) Искусственная и синтетическая резина
Искусственная и синтетическая резина Элементный, фракционный и химический состав нефти. Классификация нефтей
Элементный, фракционный и химический состав нефти. Классификация нефтей Алкины. Ацетиленовые углеводороды
Алкины. Ацетиленовые углеводороды Подготовка к ГИА. А2. Периодический закон и Периодическая система химических элементов Д.И. Менделеева
Подготовка к ГИА. А2. Периодический закон и Периодическая система химических элементов Д.И. Менделеева Физико-химические методы в анализе ЛВ. Метод ионометрии в анализе ЛВ. Определение спирта в фармацевтических препаратах
Физико-химические методы в анализе ЛВ. Метод ионометрии в анализе ЛВ. Определение спирта в фармацевтических препаратах Галогены (солеобразующие)
Галогены (солеобразующие) Суды коагуляциялау әдісі. Судың сапасын жақсартудың арнайы әдістері
Суды коагуляциялау әдісі. Судың сапасын жақсартудың арнайы әдістері Чистые вещества и смеси. Химия. 8 кл
Чистые вещества и смеси. Химия. 8 кл Свойства воды. Оценка качества
Свойства воды. Оценка качества Теплота сгорания топлива
Теплота сгорания топлива Железо и его соединения
Железо и его соединения Коррозия металлов
Коррозия металлов Классы неорганических веществ. Соли
Классы неорганических веществ. Соли Растворы. Способы выражения концентрации растворенного вещества
Растворы. Способы выражения концентрации растворенного вещества Анионы. Группы анионов
Анионы. Группы анионов Электронное строение атома
Электронное строение атома Metal–metal multiple bonded intermediates in catalysis
Metal–metal multiple bonded intermediates in catalysis Магний (Mg)
Магний (Mg) Химические свойства солей в свете теории электролитической диссоциации
Химические свойства солей в свете теории электролитической диссоциации Удивительный мир камня
Удивительный мир камня Щелочные металлы
Щелочные металлы Характеристики химического процесса. Степень превращения, селективность, выход продукта. (Лекция 1.2)
Характеристики химического процесса. Степень превращения, селективность, выход продукта. (Лекция 1.2)