Характеристики химического процесса. Степень превращения, селективность, выход продукта. (Лекция 1.2) презентация
Содержание
- 2. Целью дисциплины является изучение теоретических основ химико-технологических процессов тонкого органического, основного и нефтехимического синтеза. - Механизмы
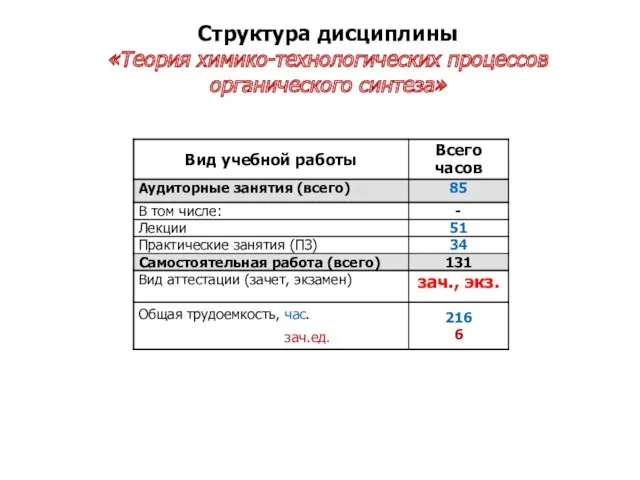
- 3. Структура дисциплины «Теория химико-технологических процессов органического синтеза»
- 4. Основная: Лебедев Н.Н., Манаков М.Н., Швец В.Ф. Теория химических процессов основного органического и нефтехимического синтеза. –
- 5. ЛИТЕРАТУРА Дополнительная: Лисицин В.Н. Химия и технология промежуточных продуктов. - М.: Химия, 1987. - 376с. Эфрос
- 6. Жоров Ю.М. Кинетика промышленных органических реакций. – М.: Химия, 1989. – 384 с. Бочкарев В.В. Теория
- 7. ХАРАКТЕРИСТИКИ ХИМИЧЕСКОГО ПРОЦЕССА: СТЕПЕНЬ ПРЕВРАЩЕНИЯ, СЕЛЕКТИВНОСТЬ, ВЫХОД ПРОДУКТА Первичной основой учения о химических превращениях является стехиометрия,
- 8. Мольные количества веществ ni удобны для характеристики периодических процессов. Для характеристики непрерывных процессов, когда вещества подают
- 9. СТЕХИОМЕТРИЯ РЕАКЦИЙ. МАТЕРИАЛЬНЫЕ РАСЧЕТЫ С точки зрения стехиометрии все химические реакции подразделяются на простые и сложные.
- 10. При этом стехиометрические коэффициенты (νi) расходуемых веществ берутся со знаком минус, а образующихся – со знаком
- 11. Пример. Пусть реакция диспропорционирования циклогексена с образованием циклогексана и бензола является простой, вычислить ni, если известно,
- 12. Из равенств К3 следует, что при простых реакциях мольное соотношение образующихся или расходуемых веществ постоянно и
- 13. Рис. Изменение мольного соотношения веществ при простых реакциях.
- 14. Сложные реакции состоят из нескольких простых реакций. К ним принадлежат: обратимые νAA + ... νBB +
- 15. При анализе известной системы сложных реакций прежде всего необходимо определить число стехиометрически независимых превращений, уравнения которых
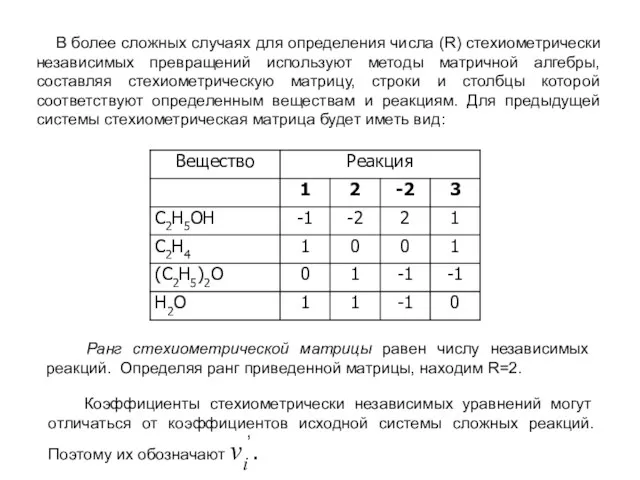
- 16. В более сложных случаях для определения числа (R) стехиометрически независимых превращений используют методы матричной алгебры, составляя
- 17. Одновременно с числом независимых реакций определяют равное ему число так называемых ключевых веществ, по которым можно
- 18. Тогда, имея в виду, что каждое из веществ может участвовать в нескольких реакциях (Δni=ΣΔnij), получим: ni
- 19. БЕЗРАЗМЕРНЫЕ ХАРАКТЕРИСТИКИ МАТЕРИАЛЬНОГО БАЛАНСА РЕАКЦИЙ В химии и технологии большое значение имеют безразмерные характеристики материального баланса:
- 20. В разных процессах химической технологии степень конверсии изменяется от 4 – 5 до почти 100 %.
- 21. где - абсолютное значение стехиометрического коэффициента при А.
- 22. Для сложных реакций, имеющих более одного ключевого вещества, степень конверсии показывает лишь долю превращенного реагента, но
- 23. Тогда получим выражение для селективности: К9 в котором двойной индекс при означает, что селективность определена для
- 24. Выражение соответствует количеству исходного реагента, израсходованному на образование данного вещества i. Очевидно, что сумма их для
- 25. Выход - это неоднозначное понятие. Иногда под ним понимают абсолютное количество полученного продукта (в г, кг,
- 26. Из формул К9 и К11 вытекает, что выход равен произведению селективности на степень конверсии: При этом
- 27. Из уравнения К11 мольные количества или потоки продуктов можно выразить через их выходы: К14 К15 Последние
- 28. Парциальные молярные балансы. На безразмерных характеристиках реакций основаны расчеты так называемых парциальных молярных балансов, составляемых на
- 29. Величина (ΔFAj / FA,0) есть степень полноты или частная степень конверсии основного реагента по данной суммарной
- 30. КОНЦЕНТРАЦИИ, ПАРЦИАЛЬНЫЕ ДАВЛЕНИЯ И МОЛЬНЫЕ ДОЛИ Кроме мольных количеств или потоков веществ и безразмерных характеристик баланса
- 31. Нередко объем или объемный поток остаются постоянными во время реакции. Это типично для жидкофазных процессов, а
- 32. Более сложные соотношения существуют для реакций, протекающих с изменением объема. При жидкофазных процессах это бывает при
- 33. Для газофазных процессов изменение объема обычно происходит из-за неравенства числа молей веществ во время реакции. Его
- 34. При подстановке Fi как функции FA,0 и XA оказывается, что Ci выражается через начальную концентрацию (CA,0=FA,0/W0).
- 36. Скачать презентацию































 Химические свойства металлов
Химические свойства металлов Золото. Что о нём мы можем рассказать?
Золото. Что о нём мы можем рассказать? d-элементы
d-элементы Подготовка к ВПР по химии. 11 класс
Подготовка к ВПР по химии. 11 класс Метаболизм кетоновых тел. Метаболизм холестерина
Метаболизм кетоновых тел. Метаболизм холестерина Химический потенциал. Фазовые равновесия
Химический потенциал. Фазовые равновесия Кислотные дожди
Кислотные дожди The Molecules of Life
The Molecules of Life Цинк и его соединения
Цинк и его соединения Фосфор и его соединения
Фосфор и его соединения Химия воды
Химия воды Закономірності протікання хімічних реакцій
Закономірності протікання хімічних реакцій Классификация химических элементов
Классификация химических элементов Способы выражения состава раствора. Задача 7
Способы выражения состава раствора. Задача 7 НЮ 2.1.1. Металлы - общая характеристика
НЮ 2.1.1. Металлы - общая характеристика Гониометрическое исследование кристаллов
Гониометрическое исследование кристаллов Сплавы железа с углеродом: стали и чугуны
Сплавы железа с углеродом: стали и чугуны Багатоатомні насичені спирти. Фізичні та хімічні властивості. Добування і застосування
Багатоатомні насичені спирти. Фізичні та хімічні властивості. Добування і застосування Мінерали та гірські породи
Мінерали та гірські породи Серная кислота
Серная кислота Electrolysis
Electrolysis Вещества
Вещества Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы
Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы Аминокислоты 2
Аминокислоты 2 Метаболизм углеводов
Метаболизм углеводов Спектральные методы: атомная спектроскопия
Спектральные методы: атомная спектроскопия Валентность и степень окисления. Химическая связь
Валентность и степень окисления. Химическая связь Альдегіди. Карбонові кислоти. Одержання. Фізичні та хімічні властивості
Альдегіди. Карбонові кислоти. Одержання. Фізичні та хімічні властивості