Содержание
- 2. Для аланина: рКа (-ОН) = 2,35 рКа (бетаина) = 9,7 Анионная форма Разделение и анализ аминокислот
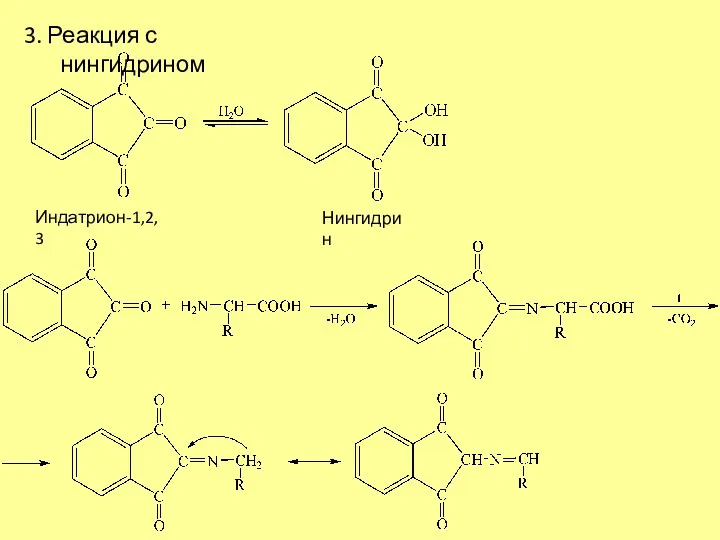
- 3. 3. Реакция с нингидрином Индатрион-1,2,3 Нингидрин
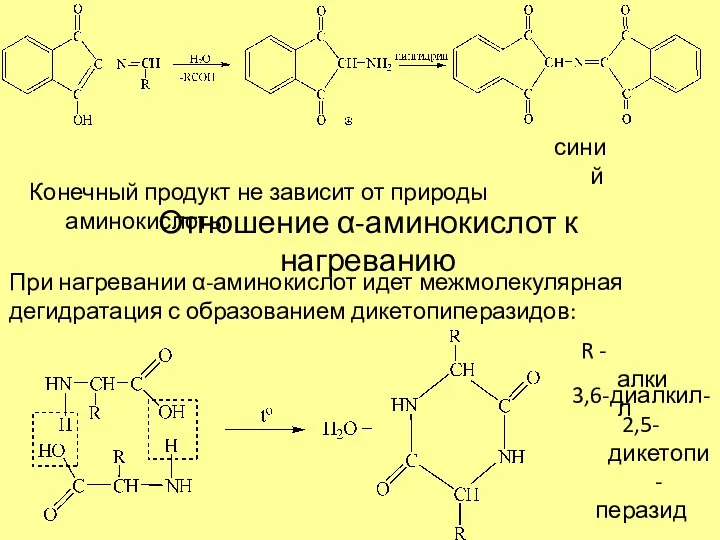
- 4. синий Конечный продукт не зависит от природы аминокислоты. Отношение α-аминокислот к нагреванию При нагревании α-аминокислот идет
- 5. N - ацилирование N-ацетилаланин Аланин Глицин Бензоилхлорид N-Бензоилглицин Реакция ацилирования применяется для защиты аминогруппы
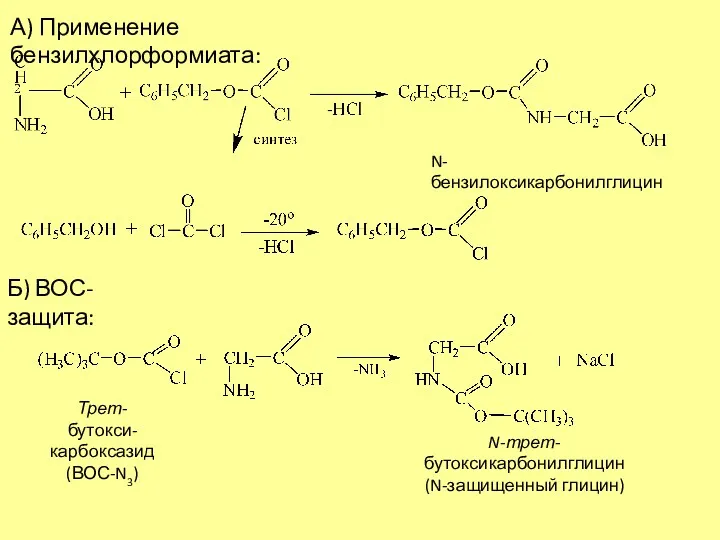
- 6. А) Применение бензилхлорформиата: N-бензилоксикарбонилглицин Б) ВОС-защита: Трет-бутокси- карбоксазид (ВОС-N3) N-трет-бутоксикарбонилглицин (N-защищенный глицин)
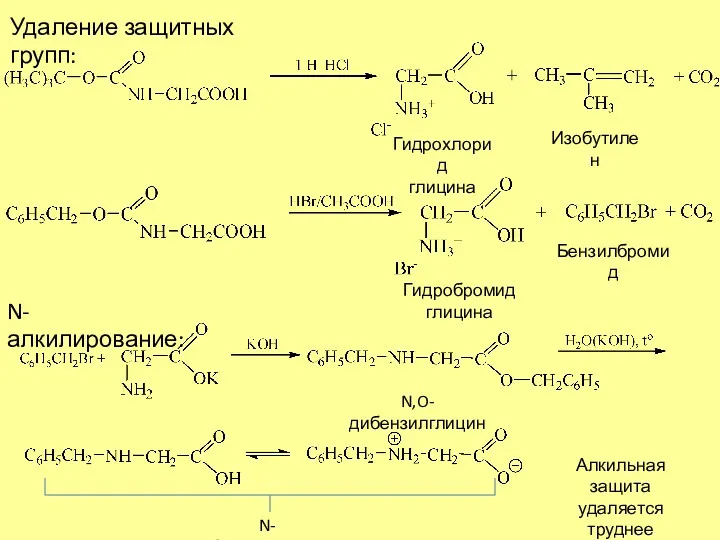
- 7. Удаление защитных групп: Гидрохлорид глицина Изобутилен Гидробромид глицина Бензилбромид N-алкилирование: N-бензилглицин Алкильная защита удаляется труднее ацильной
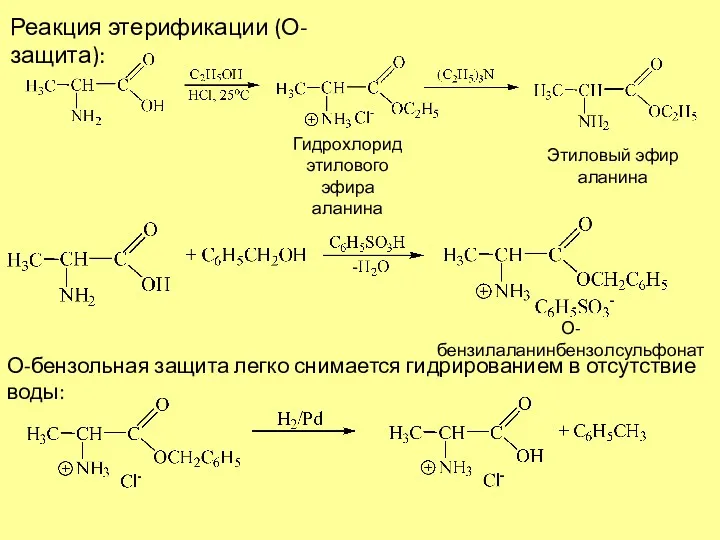
- 8. Реакция этерификации (О-защита): Гидрохлорид этилового эфира аланина Этиловый эфир аланина О-бензилаланинбензолсульфонат О-бензольная защита легко снимается гидрированием
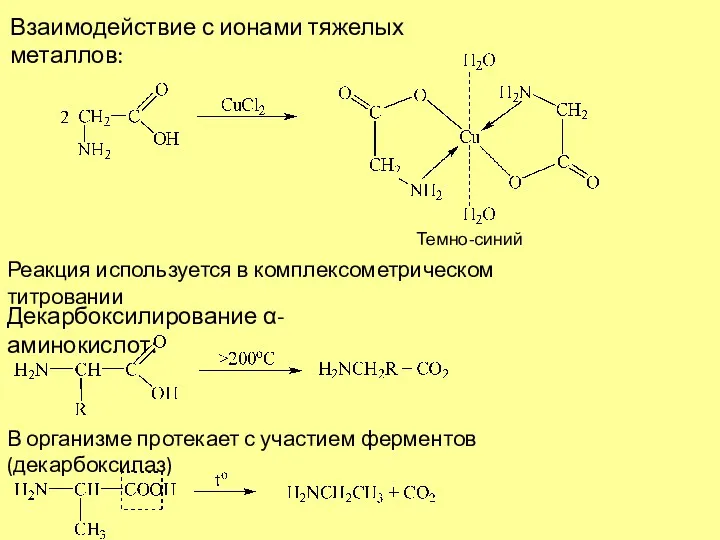
- 9. Взаимодействие с ионами тяжелых металлов: Темно-синий Реакция используется в комплексометрическом титровании Декарбоксилирование α-аминокислот: В организме протекает
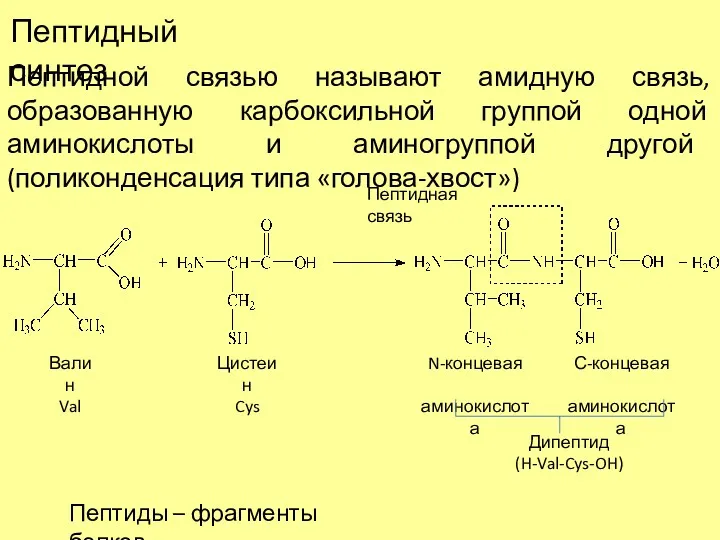
- 10. Пептидный синтез Пептидной связью называют амидную связь, образованную карбоксильной группой одной аминокислоты и аминогруппой другой (поликонденсация
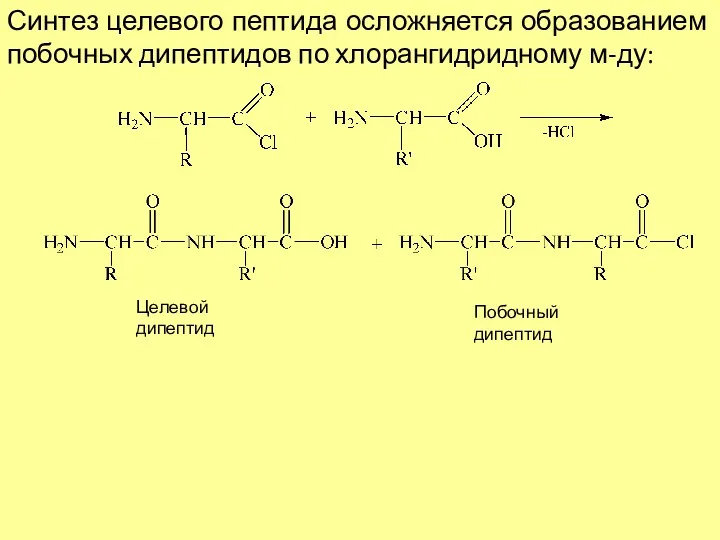
- 11. Синтез целевого пептида осложняется образованием побочных дипептидов по хлорангидридному м-ду: Целевой дипептид Побочный дипептид
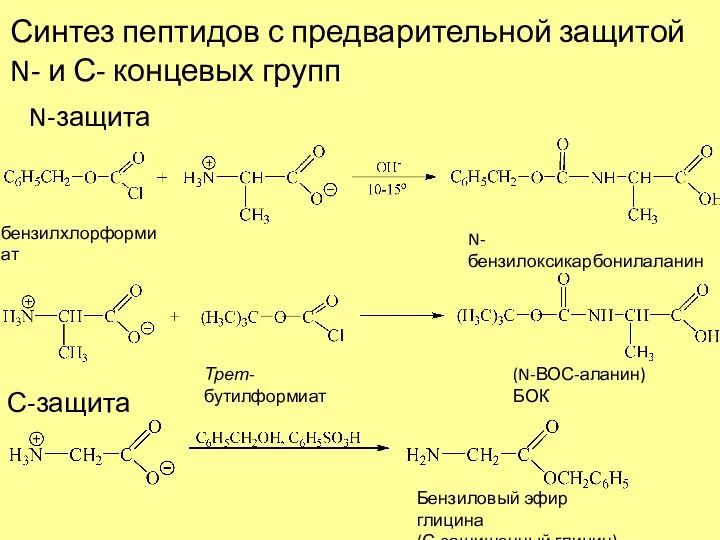
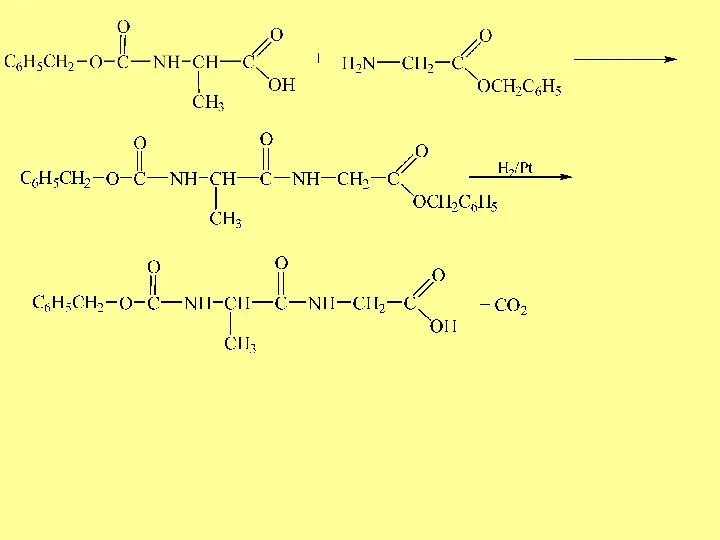
- 12. Синтез пептидов с предварительной защитой N- и С- концевых групп N-защита бензилхлорформиат N-бензилоксикарбонилаланин (N-ВОС-аланин) БОК Трет-бутилформиат
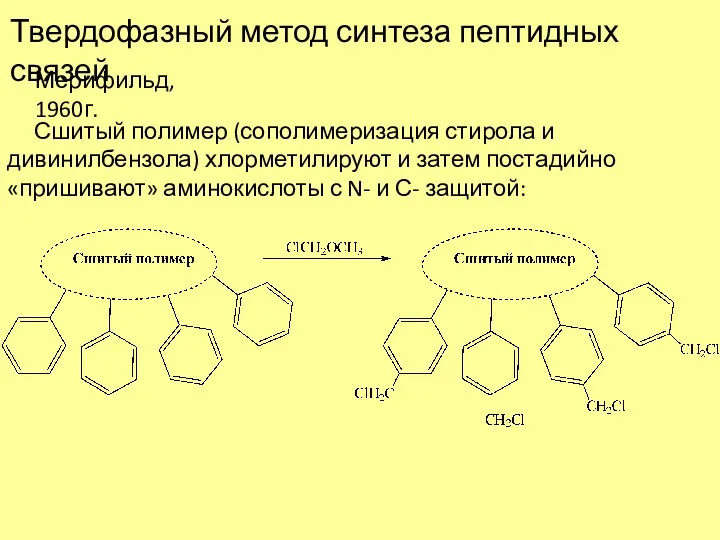
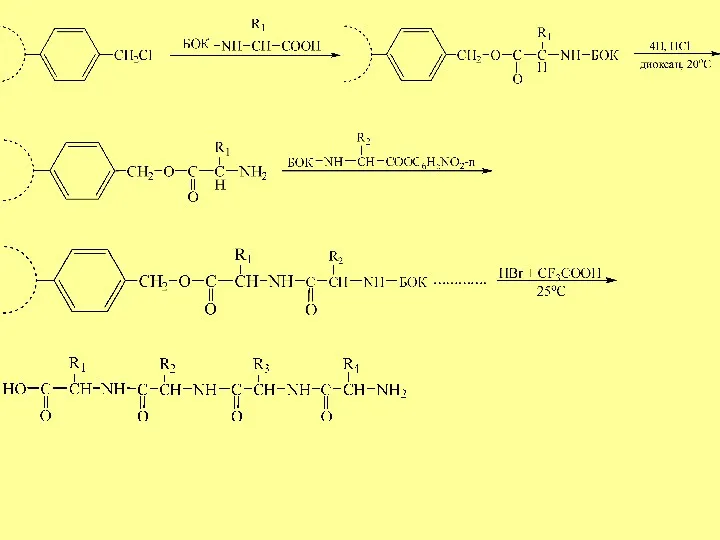
- 14. Твердофазный метод синтеза пептидных связей Мерифильд, 1960г. Сшитый полимер (сополимеризация стирола и дивинилбензола) хлорметилируют и затем
- 17. Скачать презентацию


 Простые вещества металлы
Простые вещества металлы Биотыңайтқыштар
Биотыңайтқыштар Цинк
Цинк Тканые армирующие наполнители
Тканые армирующие наполнители Углеводы. Урок по химии для 9 класса
Углеводы. Урок по химии для 9 класса Оксиди нітрогену
Оксиди нітрогену Классы неорганических веществ (лекция № 4/5)
Классы неорганических веществ (лекция № 4/5) Роль хімії у розв`язанні екологічної проблеми
Роль хімії у розв`язанні екологічної проблеми Молекулярна маса речовини
Молекулярна маса речовини Расчеты по химическим уравнениям
Расчеты по химическим уравнениям Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Запалювання нагрітим тілом та електричним розрядом
Запалювання нагрітим тілом та електричним розрядом Интересные факты о химических веществах
Интересные факты о химических веществах Аналитическая химия. Предмет и задачи
Аналитическая химия. Предмет и задачи General, specific properties are common to all matters
General, specific properties are common to all matters Биологически важные 5-ти и 6-ти членные гетероциклические соединения. (Лекция 25)
Биологически важные 5-ти и 6-ти членные гетероциклические соединения. (Лекция 25) Фосфор и его соединения. Урок по химии для 9 класса
Фосфор и его соединения. Урок по химии для 9 класса Химические реакторы
Химические реакторы Физические методы стабилизации масел
Физические методы стабилизации масел Экспериментальным исследованием установить тип данной химической реакции
Экспериментальным исследованием установить тип данной химической реакции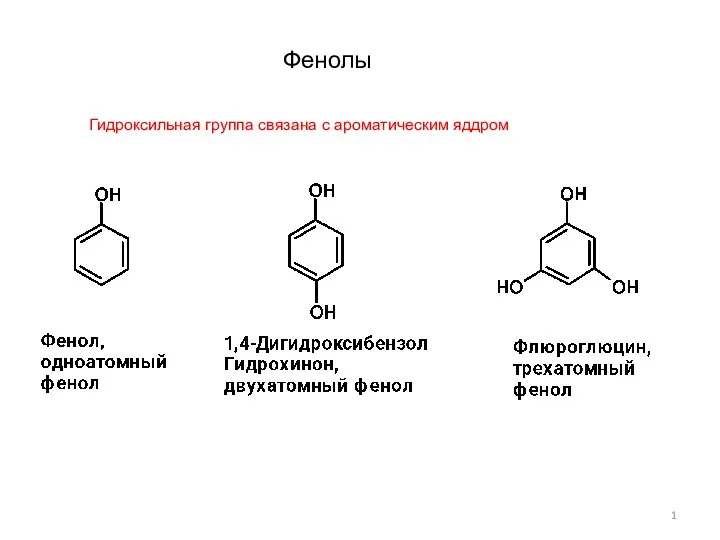 Фенолы-1
Фенолы-1 Химический факультет
Химический факультет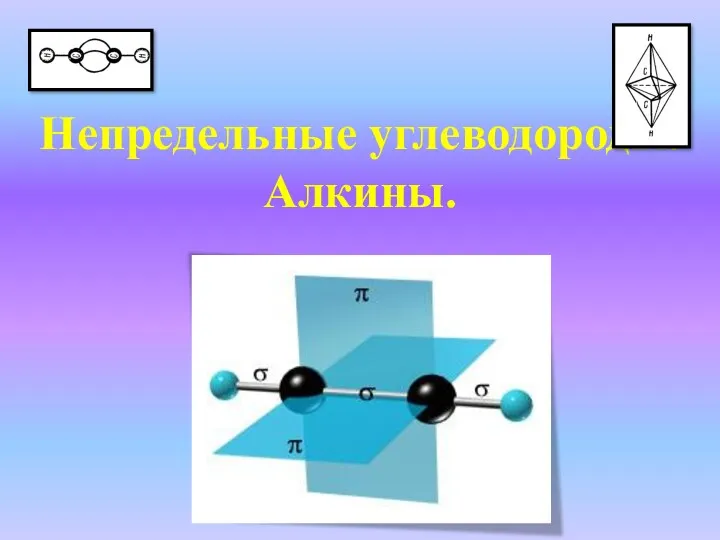 Непредельные углеводороды. Алкины
Непредельные углеводороды. Алкины Катиониты. Классификация катионитов
Катиониты. Классификация катионитов Азотная кислота
Азотная кислота Классификация химических реакций
Классификация химических реакций Озон. Применение
Озон. Применение Дисперсные системы
Дисперсные системы