Содержание
- 2. Определите химическую связь для веществ Н2 НСl NаСl Са ионная ковалентная неполярная ковалентная полярная металлическая
- 3. Степень окисления. Степень окисления - это условный заряд атомов, вычисленный из предположения, что вещество состоит только
- 4. порядок выставления с. о. в химических формулах: вверху над символом элемента, причем вначале пишется заряд («+»
- 5. * 1. На первом месте находится элемент с положительной степенью окисления. 2. На последнем месте находится
- 6. Степень окисления Правила для определения степени окисления. Положительная (положительное значение с.о. имеют элементы с меньшим значением
- 7. Постоянная степень окисления. У металлов степень окисления всегда положительна и равна номеру группы (для металлов главных
- 8. Постоянная степень окисления Степень окисления фтора (F) всегда равна -1
- 9. Переменная степень окисления Все остальные металлы (кроме перечисленных) Почти все неметаллы
- 10. Переменная степень окисления. У атома кислорода (О) степень окисления равна -2, кроме соединений со фтором (+2)
- 11. Переменная степень окисления. У атома водорода степень окисления равна +1 +1 -2 Н2О, Кроме соединений с
- 12. Нулевая степень окисления. Степень окисления простых веществ и свободных атомов всегда равна нулю (0): 0 О2
- 13. Суммарная степень окисления в молекуле всегда равна 0 +1 -2 Na2O +3 -1 AlCl3 +2 -1
- 14. Для того, чтобы рассчитать с.о. данного элемента в соединении, надо знать с.о. другого элемента
- 15. Задание 1: Определить степень окисления в соединениях K2О, AlH3, CaF2 +1 -2 K2O +3 -1 AlH3
- 16. Бинарные соединения. Бинарные соединения – это соединения, состоящие из двух химических элементов.
- 17. Бинарные соединения. На первом месте всегда записывается элемент с положительной степенью окисления, а на втором -
- 18. Названия бинарных соединений. На первом месте в названии бинарного соединения записывается латинское название элемента с отрицательной
- 19. Названия бинарных соединений. Названия элементов с отрицательной степенью окисления: Cl - хлорид О - оксид Н
- 20. Задание 2: назвать бинарные соединения, формулы которых даны. +1 -1 NaCl - +2 -1 SCl2 -
- 21. Составление формул бинарных соединений по названию. оксид углерода (IV). 1) Записать символы химических элементов образующих соединение:
- 22. Составление формул бинарных соединений по названию. 2) Над атомами химических элементов в соединении проставить их степени
- 23. Составление формул бинарных соединений по названию. 3) Найти наименьшее общее кратное между значениями степеней окисления: +4
- 24. Составление формул бинарных соединений по названию. Определить индексы, разделив НОК на значения степеней окисления каждого элемента.
- 25. Задание 3: Составить формулы веществ по названиям. Сульфид лития - Оксид серы (IV) - Оксид азота
- 26. Домашнее задание: § 17 Назвать вещества: NO, N2O, N2O3, PCl3, PCl5, CuCl2. Составить формулы веществ по
- 28. Скачать презентацию
 Токсикология и анализ спиртов
Токсикология и анализ спиртов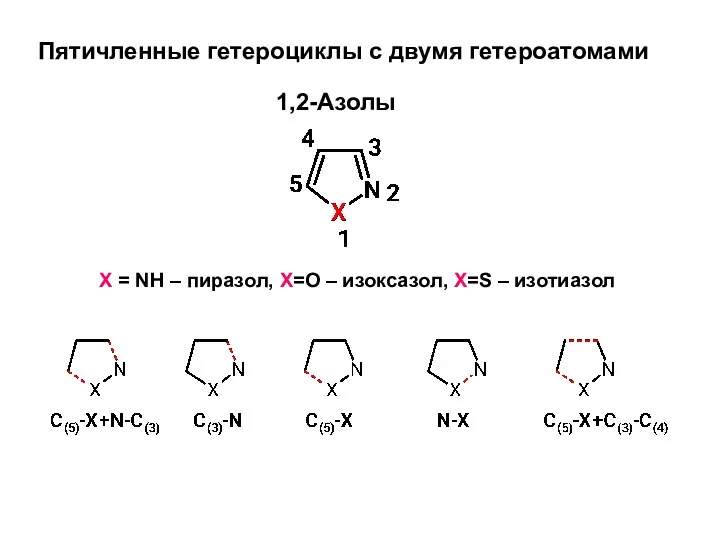 Пятичленные гетероциклы с двумя гетероатомами
Пятичленные гетероциклы с двумя гетероатомами Химические свойства металлов
Химические свойства металлов Water vapor. Nitrous oxide. Aerosols
Water vapor. Nitrous oxide. Aerosols Цинк и его соединения
Цинк и его соединения Химическая связь. Валентность элементов в ковалентных соединениях. Степень окисления элементов
Химическая связь. Валентность элементов в ковалентных соединениях. Степень окисления элементов Соли аммония
Соли аммония Оксиды и гидроксиды
Оксиды и гидроксиды Бытовая химия
Бытовая химия Целлюлоза
Целлюлоза Реакційна здатність насичених вуглеводнів. Реакційна здатність ненасичених вуглеводнів (алкени, алкадієни, алкіни)
Реакційна здатність насичених вуглеводнів. Реакційна здатність ненасичених вуглеводнів (алкени, алкадієни, алкіни) Строение атома. Периодический закон и система элементов Д.И. Менделеева. Химическая связь. Гибридизация
Строение атома. Периодический закон и система элементов Д.И. Менделеева. Химическая связь. Гибридизация Кислотно-основное титрование в неводных средах
Кислотно-основное титрование в неводных средах Валентность и степень окисления 8 класс
Валентность и степень окисления 8 класс Химические элементы и организм человека
Химические элементы и организм человека Кристаллография, кристаллохимия, минералогия
Кристаллография, кристаллохимия, минералогия Аварийно-химически-опасные вещества (АХОВ). Описание. Методы оказания первой помощи
Аварийно-химически-опасные вещества (АХОВ). Описание. Методы оказания первой помощи Химические элементы в организме человека
Химические элементы в организме человека Тотығутотықсыздану титрлеу әдістері. Дәріс № 7
Тотығутотықсыздану титрлеу әдістері. Дәріс № 7 Химические реакции. Классификация. Повторение
Химические реакции. Классификация. Повторение Теории кислот и оснований. Буферные системы крови
Теории кислот и оснований. Буферные системы крови Коллигативные свойства растворов
Коллигативные свойства растворов Карбоновые кислоты – союз двух групп (урок-исследование химических свойств карбоновых кислот)
Карбоновые кислоты – союз двух групп (урок-исследование химических свойств карбоновых кислот) Борьба с биологической коррозией
Борьба с биологической коррозией Элементы IV А - группы
Элементы IV А - группы Соединения химических элементов. 8 класс
Соединения химических элементов. 8 класс Электрохимические процессы
Электрохимические процессы Спирты. Классификация спиртов
Спирты. Классификация спиртов