Слайд 2
2
2 2
2
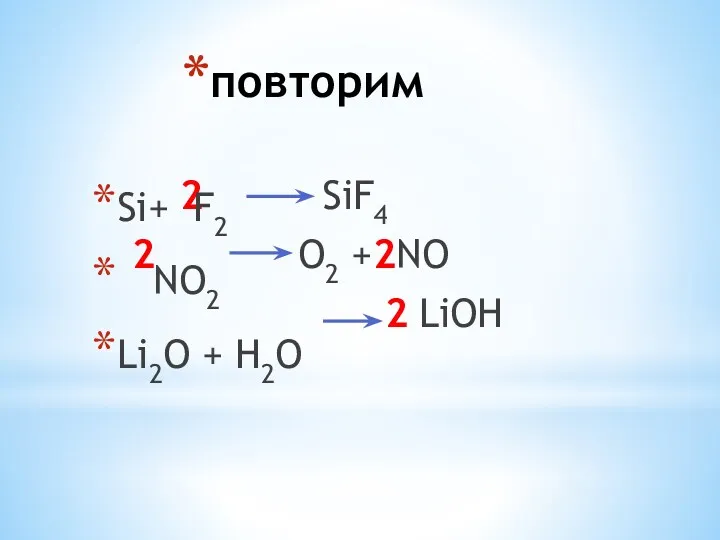
повторим
Si+ F2
NO2
Li2O + H2O
SiF4
O2
+ NO
LiOH
Слайд 3

Химические реакции. Классификация.
Тема урока:
Слайд 4

Что такое химическая реакция?
Химические реакции или химические явления – это процессы,
в результате которых одни вещества превращаются в другие;
Слайд 5

По каким признакам можно определить химические реакции?
Выделение газа;
Образование осадка;
Выделение (поглощение) тепла
и света;
Появление или изменение запаха или вкуса;
Изменение цвета;
Слайд 6

Тип химической реакции?
Расставьте коэффициенты в уравнениях
химических реакций:
Ca + O2
=
Li + O2 =
S + O2 =
A + B = AB
Слайд 7

РЕАКЦИИ
СОЕДИНЕНИЯ
Как одним словом мы можем назвать процесс, который протекает?
Слайд 8
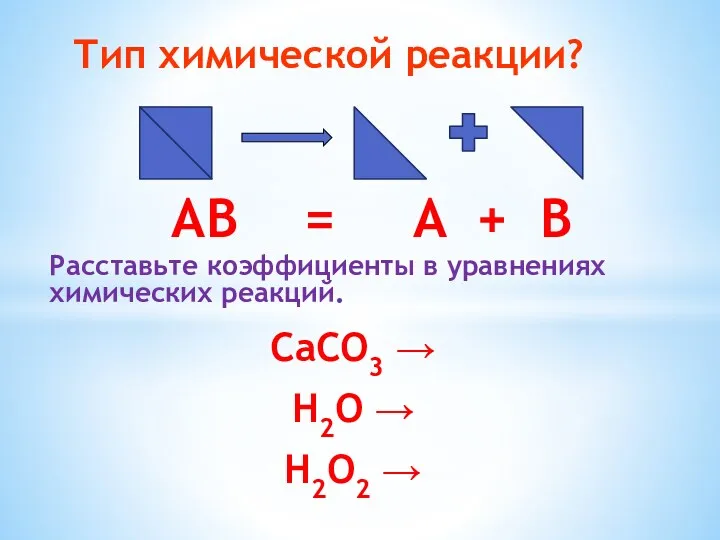
Тип химической реакции?
Расставьте коэффициенты в уравнениях химических реакций.
CaCO3 →
H2O
Слайд 9

РЕАКЦИИ
РАЗЛОЖЕНИЯ
Как одним словом мы можем назвать процесс, который протекает?
Слайд 10

С
Д
ДОМ
СОМ
Тип химической реакции?
Слайд 11

РЕАКЦИИ
ЗАМЕЩЕНИЯ
Как одним словом мы можем назвать процесс, который протекает?
Слайд 12
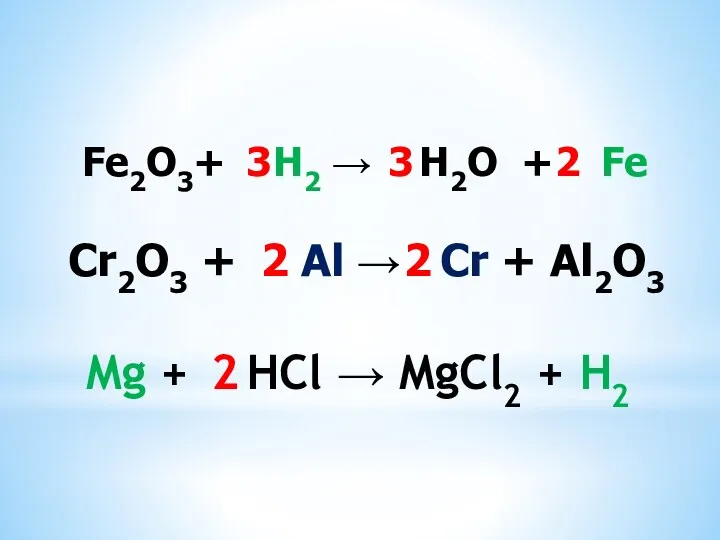
H2
Cr2O3 + Al → Cr + Al2O3
3 3 2
Fe2O3+ H2 → H2O + Fe
Слайд 13

РЕАКЦИИ
ОБМЕНА
Как одним словом мы можем назвать процесс, который протекает?
Слайд 14
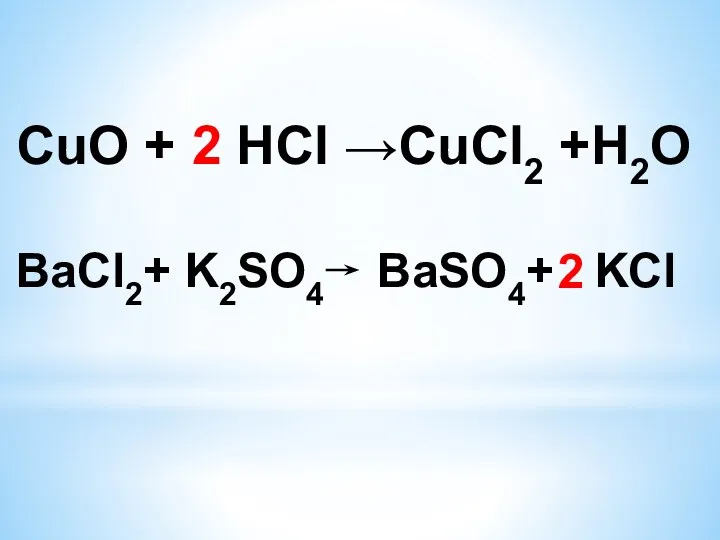
CuO + HCl →СuСl2 +H2О
2
BaCl2+ K2SO4 BaSO4+ KCl
2
Слайд 15
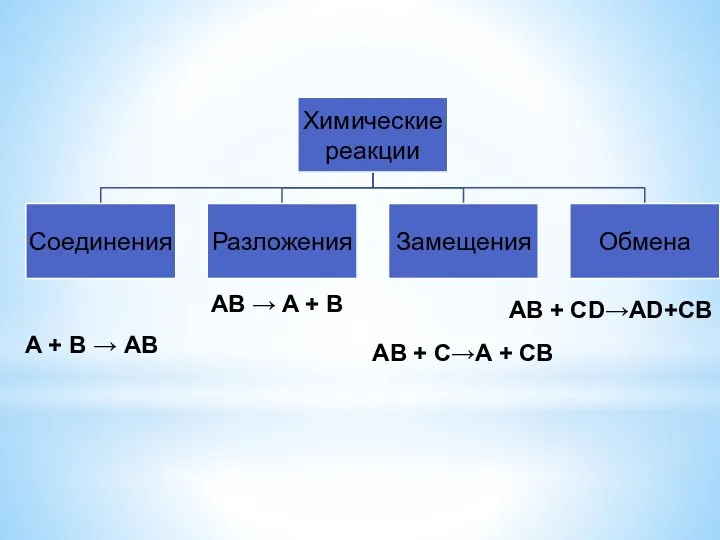
A + B → AB
AB → A + B
AB + C→A
Слайд 16

Инструкции по проведению лабораторной работы №3 «Типы химических реакций»
Ход работы:
Опыты №1, №2 демонстрирует учитель.
Опыты №3№4 ученики проводят самостоятельно.
При выполнении работы соблюдаем правила ТБ.
Работаем аккуратно и внимательно.
Желаю успехов.
Слайд 17

§20 , в. 3 (п) , конспект
Домашнее задание:
Слайд 18

Итоги урока:
1) по какому принципу мы разделили химические реакции на четыре
типа?
(по исходным веществам и продуктам реакции).
2) с какими именно типами реакций мы ознакомились сегодня?
( соединения, разложения , замещения , обмена . )
Слайд 19

Спасибо за урок! До новых встреч!










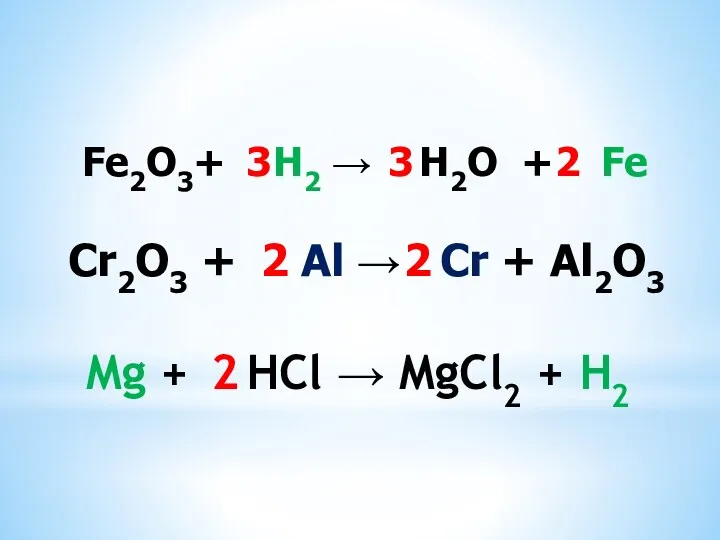







 Хімічні формули речовин
Хімічні формули речовин Водород
Водород Химиялық қауіптілер. Нитраттар
Химиялық қауіптілер. Нитраттар Кислоты в свете теории электролитической диссоциации (ТЭД)
Кислоты в свете теории электролитической диссоциации (ТЭД) Кристаллическое строение и свойства металлов
Кристаллическое строение и свойства металлов Материаловедение промышленного производства. Особенности строения твердых тел
Материаловедение промышленного производства. Особенности строения твердых тел Неметаллы: общая характеристика. 9 класс
Неметаллы: общая характеристика. 9 класс Понятия про синтетические лекарственные средства
Понятия про синтетические лекарственные средства Основи. Властивості, застосування гідроксидів Натрію і Калію
Основи. Властивості, застосування гідроксидів Натрію і Калію Акцепторы катионов и анионов. Краун-эфиры и близкие структурные аналоги: поданды, лариатэфиры. Супрамолекулярная фотоника
Акцепторы катионов и анионов. Краун-эфиры и близкие структурные аналоги: поданды, лариатэфиры. Супрамолекулярная фотоника Химия в Великую Отечественную войну
Химия в Великую Отечественную войну Массовая доля вещества в растворе
Массовая доля вещества в растворе Строение атома. Периодический закон и периодическая система элементов
Строение атома. Периодический закон и периодическая система элементов Современные химические технологии
Современные химические технологии Каталитический риформинг
Каталитический риформинг Получение, собирание, распознавание газов. (Практическая работа 2)
Получение, собирание, распознавание газов. (Практическая работа 2) Углеводороды. Предельные нециклические (ациклические) углеводороды. Алканы
Углеводороды. Предельные нециклические (ациклические) углеводороды. Алканы Простые вещества
Простые вещества Незвичайна вода
Незвичайна вода Фазовое равновесие
Фазовое равновесие Химия в повседневной жизни человека
Химия в повседневной жизни человека Химическая очистка сточных вод. Окисление и восстановление
Химическая очистка сточных вод. Окисление и восстановление Растворы: состав и их коллигативные свойства
Растворы: состав и их коллигативные свойства Щелочные и щелочноземельные металлы
Щелочные и щелочноземельные металлы Относительная молекулярная масса вещества. Задачи
Относительная молекулярная масса вещества. Задачи Химические свойства карбокатионов
Химические свойства карбокатионов Тіршілік процесіне қатысатын гетерофункционалды қосылыстар
Тіршілік процесіне қатысатын гетерофункционалды қосылыстар Скорость химических реакций
Скорость химических реакций