Тест по теме “Водород. Химический элемент и простое вещество”
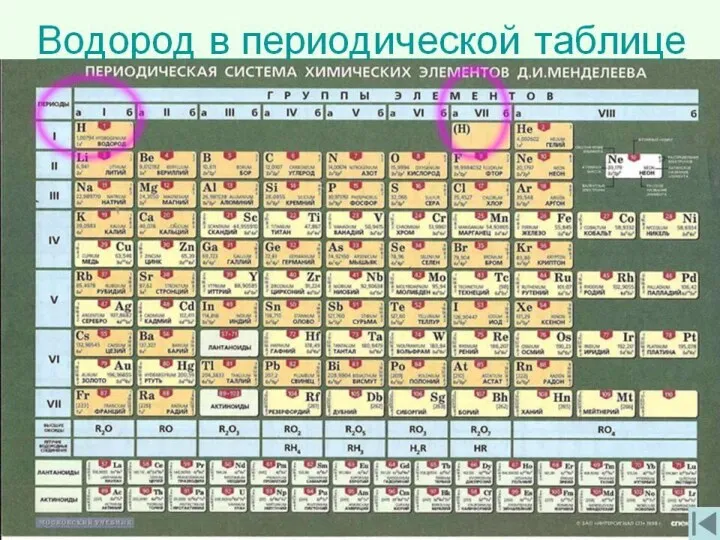
1. Водород в ПС
находится:
1) во 2 А группе
2) в 7 А группе
3) в 6 А группе
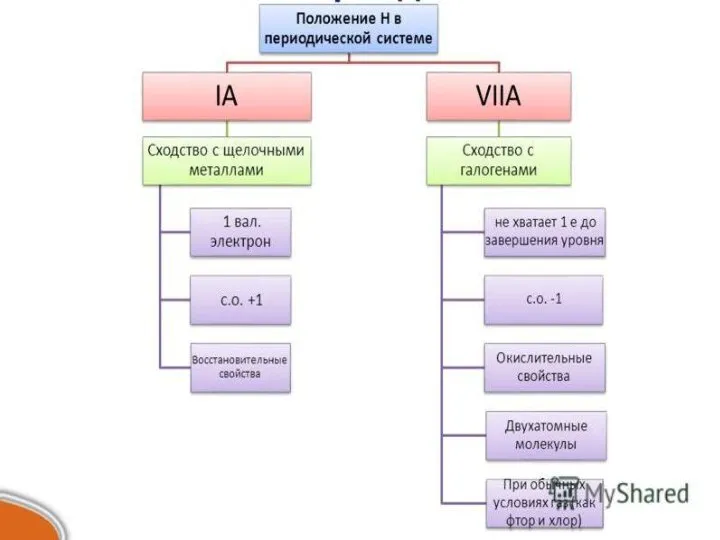
2.Водород проявляет степень окисления в соединениях:
1) +1 и - 1
2) +2 и -2
3) 0 и + 1
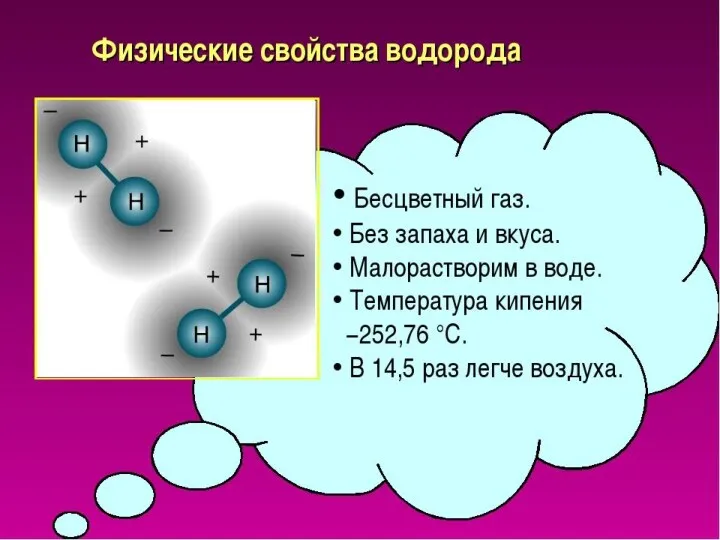
3. Водород это газ:
1) без цвета, вкуса, запаха, тяжелее воздуха
2) без цвета, запаха, вкуса, легче воздуха
3) без цвета, вкуса, с запахом, легче воздуха
4. Водород – как химический элемент во Вселенной занимает:
1) Второе место
2) Третье место
3) Первое место
5.Водород является продуктом взаимодействия:
1) Cu + HCl;
2) Zn + HCl;
3) Cu + H2O;
6. Водород в химической реакции с металлами является:
1) восстановителем
2) окислителем
















 Азотная кислота и её соли
Азотная кислота и её соли Химический состав красителей и препаратов для завивки. Лекция 8. Индустрия красоты
Химический состав красителей и препаратов для завивки. Лекция 8. Индустрия красоты Фосфор. Гипофосфатемия и гиперфосфатемия
Фосфор. Гипофосфатемия и гиперфосфатемия Химия и здоровье
Химия и здоровье Классификация химических реакций по различным основаниям. 9 класс
Классификация химических реакций по различным основаниям. 9 класс Галогены. 9 класс
Галогены. 9 класс Кислородсодержащие органические соединения. Спирты
Кислородсодержащие органические соединения. Спирты Алкины. Химические и физические свойства алкинов. Строение алкинов
Алкины. Химические и физические свойства алкинов. Строение алкинов Теория электролитической диссоциации
Теория электролитической диссоциации Явище ізомерії. Структурна ізомерія, номенклатура насичених вуглеводнів
Явище ізомерії. Структурна ізомерія, номенклатура насичених вуглеводнів Основные классы неорганических соединений
Основные классы неорганических соединений Кислородсодержащие соединения азота
Кислородсодержащие соединения азота Apparatus of installations with circulating ball catalyst
Apparatus of installations with circulating ball catalyst Посуда, ее виды и использование
Посуда, ее виды и использование Газохимия. Абсорбционно-газофракционирующая установка. (Лекция 5.2)
Газохимия. Абсорбционно-газофракционирующая установка. (Лекция 5.2) Азот
Азот Штучні та природні речовини
Штучні та природні речовини Многоатомные спирты (10 класс)
Многоатомные спирты (10 класс) Новые требования к оценке опасности, паспортам безопасности и маркировке химической продукции
Новые требования к оценке опасности, паспортам безопасности и маркировке химической продукции Механические свойства минералов
Механические свойства минералов Альдегиды и кетоны
Альдегиды и кетоны Геохимические классификации элементов
Геохимические классификации элементов Виды присадок к моторным топливам. Присадки к дизельному топливу
Виды присадок к моторным топливам. Присадки к дизельному топливу Дробный метод анализа металлических ядов в минерализате (деструктате) (Продолжение)
Дробный метод анализа металлических ядов в минерализате (деструктате) (Продолжение) Неметаллы: общая характеристика. 9 класс
Неметаллы: общая характеристика. 9 класс Пироксены. Группа пироксенов
Пироксены. Группа пироксенов Электролит және бейэлектролит ерітінділердің коллигативті қасие
Электролит және бейэлектролит ерітінділердің коллигативті қасие Вода - розчинник. Урок 41
Вода - розчинник. Урок 41