Содержание
- 2. Познакомиться с азотной кислотами, её солями- нитратами, их физическими и химическими свойствами ; Экспериментально изучить свойства
- 3. Когда - то селитрами звали нитраты, а "духом" была кислота
- 4. Бесцветная жидкость «Дымится» на воздухе Едкая Плотность в 1,4 раза больше плотности воды На свету желтеет
- 5. Разложение 4HNO3=4NO2+2H2O+O2
- 7. +5 +4 N +1e=N +5 +2 N +3е= N +5 -3 N +8e =N
- 8. Взаимодействие с металлами 3Cu+8HNO3=3Cu(NO3)2+2NO +4H 2O 0 +2 Cu -2e=Cu +5 +2 N + 3e =N
- 9. Ag+2HNO 3=AgNO 3+NO 2 +H 2O 0 + Ag -1e=Ag +5 +4 N +1e=N
- 10. 4Zn+10HNO 3=4Zn(NO 3) 2+NH 4NO3 +3H 2O 0 +2 Zn -2e=Zn +5 -3 N +8e=N
- 11. 2KNO 3=2KNO 2+O 2 2Cu(NO 3) 2=2CuO+4NO 2 +O 2 2AgNO3=2Ag+2NO 2 + O 2 Нитраты.Разложение
- 12. NH 4NO3 =2H 2 O+N 2O NH 4NO 2=2H 2O+N2
- 13. Применение азотной кислоты и нитратов
- 14. Красители
- 15. Удобрения
- 16. Взрывчатка
- 17. Лекарства
- 18. Пластмассы
- 19. Искусственные волокна
- 20. 20 Проверь сам себя
- 21. Параграф №26,стр.119 – 12 рабочая тетрадь,стр.№ Домашнее задание
- 22. Спасибо за урок
- 24. Скачать презентацию










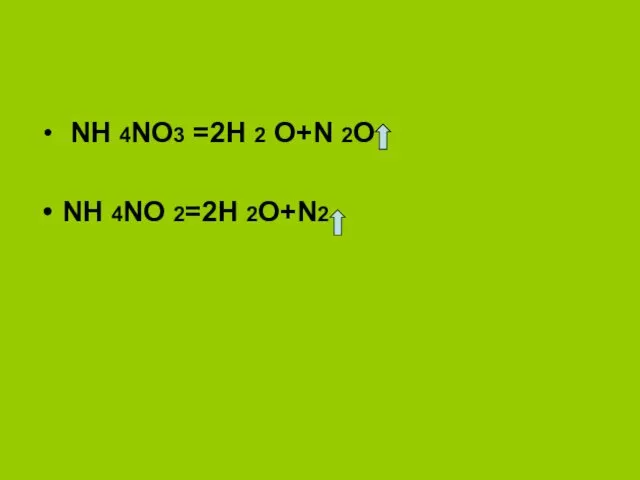









 Углеводородное топливо, его виды и назначения
Углеводородное топливо, его виды и назначения Соединения химических элементов. Урок-игра. 8 класс
Соединения химических элементов. Урок-игра. 8 класс Основи. Властивості, застосування гідроксидів Натрію і Калію
Основи. Властивості, застосування гідроксидів Натрію і Калію Фенолы. Классификация и номенклатура фенолов
Фенолы. Классификация и номенклатура фенолов Общая характеристика элементов VA -группы. Азот, распространение, физические и химические свойства. Круговорот в природе
Общая характеристика элементов VA -группы. Азот, распространение, физические и химические свойства. Круговорот в природе Гетерофункциональные соединения
Гетерофункциональные соединения Циклоалканы
Циклоалканы Mineralogy. Chemical composition and properties of minerals
Mineralogy. Chemical composition and properties of minerals Введение в геологию и минералогию
Введение в геологию и минералогию Электрохимические системы
Электрохимические системы Окислительно-восстановительные реакции. Основные закономерности окисления различных классов органических веществ
Окислительно-восстановительные реакции. Основные закономерности окисления различных классов органических веществ Нефть
Нефть Классификация химических реакций
Классификация химических реакций Гибридизация электронных орбиталей и геометрия молекул
Гибридизация электронных орбиталей и геометрия молекул Важнейшие классы бинарных соединений – оксиды и летучие соединения
Важнейшие классы бинарных соединений – оксиды и летучие соединения Карбоновые кислоты и их функциональные производные
Карбоновые кислоты и их функциональные производные Атмосфера. Химия стратосферы
Атмосфера. Химия стратосферы Обмен индивидуальных аминокислот
Обмен индивидуальных аминокислот Вещества в твоей жизни
Вещества в твоей жизни Біохімія вуглеводів
Біохімія вуглеводів Оксиды. 9 класс
Оксиды. 9 класс Вуглеводи
Вуглеводи Нефть как природный источник углеводородов
Нефть как природный источник углеводородов Признаки химических реакций
Признаки химических реакций Металдардың химиялық белсенділігі
Металдардың химиялық белсенділігі Химический элемент водород
Химический элемент водород Характеристика химического элемента по его положению в периодической системе химических элементов Д.И. Менделеева
Характеристика химического элемента по его положению в периодической системе химических элементов Д.И. Менделеева Химико-лесной комплекс
Химико-лесной комплекс