Слайд 2
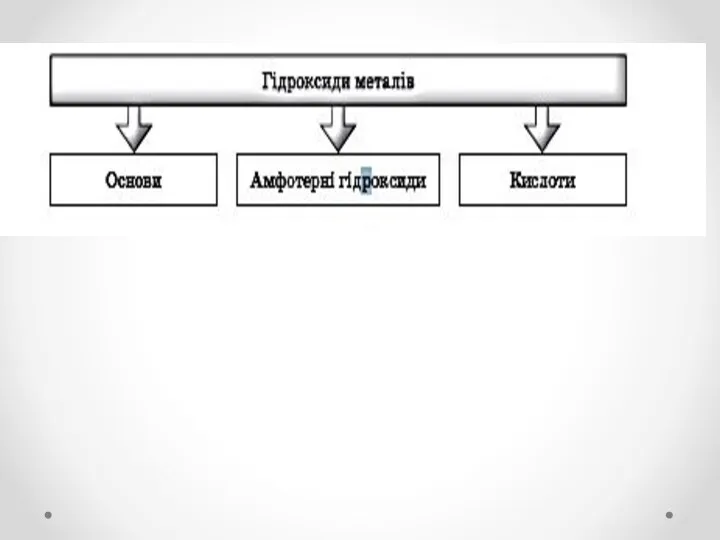
Слайд 3

Основи
Складні речовини із загальною формулою.
Основи поділяють на розчинні (луги) і
нерозчинні у воді
Слайд 4

ФІЗИЧНІ ВЛАСТИВОСТІ НАТРІЙ ГІДРОКСИДУ І КАЛЬЦІЙ ГІДРОКСИДУ
Натрій гідроксид NaOH — біла
непрозора тверда речовина, гігроскопічна, добре розчиняється у воді (за 20 °С у 100 г води розчиняється 100 г натрій гідроксиду), розчинення супроводжується виділенням теплоти. Розчини милкі на дотик.
Фізичні властивості кальцій гідроксиду схожі з властивостями натрій гідроксиду.
Хоча він має порівняно малу розчинність (за 20 °С у 100 г води розчиняється 0,16 г кальцій гідроксиду).
Слайд 5

ЗАБАРВЛЕННЯ ІНДИКАТОРІВ
У розчині лугів лакмус набуває синього кольору, метиловий оранжевий —
жовтого, фенолфталеїн — малинового.
Універсальний індикатор у розбавленому розчині лугу має зелене забарвлення, у концентрованому — синє та синьо-фіолетове.
ПРАВИЛА ТБ!!!!!!!!
Слайд 6

Хімічні властивості лугів
Запишіть відповідні рівняння хімічних реакцій
Слайд 7

ХІМІЧНІ ВЛАСТИВОСТІ НАТРІЙ ГІДРОКСИДУ І КАЛЬЦІЙ ГІДРОКСИДУ
Лугам також властива взаємодія з
металами, оксиди та гідроксиди яких мають амфотерні властивості, і деякими органічними речовинами.
1. Взаємодія натрій гідроксиду при сплавлянні з металами, оксиди та гідроксиди яких мають амфотерні властивості.
2NaOH + Zn = H2 + Na2ZnO2 натрій цинкат
2KOH + 2Al + 2H2O = 3H2 + 2KAlO2 калій метаалюмінат
2. Взаємодія натрій гідроксиду з деякими органічними речовинами (пригадайте з 10 класу взаємодію лугів з фенолом, омилення жирів).
Слайд 8

Слайд 9
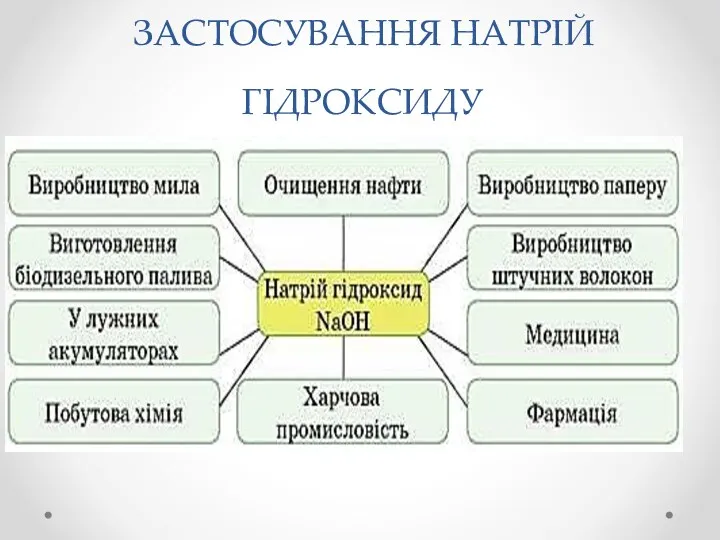
ЗАСТОСУВАННЯ НАТРІЙ ГІДРОКСИДУ
Слайд 10

ЗАСТОСУВАННЯ КАЛЬЦІЙ ГІДРОКСИДУ (ГАШЕНОГО ВАПНА)
СаО + Н2О = Са(ОН)2 реакція екзотермічна
Використовують у будівництві (вапняний розчин)
Зв'язувальні властивості гашеного вапна Са(ОН)2, ґрунтуються на тому, що ця речовина поступово реагує з вуглекислим газом повітря і перетворюється на кальцій карбонат:
Са(ОН)2 + СО2 → СаСО3 + Н2О.
Унаслідок цього вапняний розчин твердне і міцно скріплює будівельні матеріали.
Кальцій гідроксид входить до складу бордоської рідини, якою обробляють сади від шкідників.
На кислотних ґрунтах його вносять для зниження їх кислотності.
У харчовій промисловості гідроксид кальцію використовується як харчова добавка Е 526 (загущувач, регулятор кислотності, затверджувач, емульгатор).









 топ през
топ през Благородные металлы
Благородные металлы Полимеры, бумага
Полимеры, бумага Анализ раствора кальция хлорида 5%-200 мл
Анализ раствора кальция хлорида 5%-200 мл Скорость химических реакций. Химическое равновесие
Скорость химических реакций. Химическое равновесие Магний и кальций
Магний и кальций Вода. 8 класс
Вода. 8 класс Гидролиз солей. Лекция №9
Гидролиз солей. Лекция №9 Кислородные соединения серы. 2 часть
Кислородные соединения серы. 2 часть Переходные элементы
Переходные элементы Деструктивные процессы переработки нефти
Деструктивные процессы переработки нефти Складання рівнянь окисно-відновних реакцій. Метод електронного балансу
Складання рівнянь окисно-відновних реакцій. Метод електронного балансу Законы химии
Законы химии Plastic is one of the challenges of the 21st century
Plastic is one of the challenges of the 21st century Методы определения механических свойств полимерных композиционных материалов
Методы определения механических свойств полимерных композиционных материалов Оксиды. Классификация, номенклатура, свойства оксидов, получение, применение
Оксиды. Классификация, номенклатура, свойства оксидов, получение, применение Энергетика химических процессов. Термодинамика. (Лекция 4)
Энергетика химических процессов. Термодинамика. (Лекция 4) Циклоалканы. 10 класс
Циклоалканы. 10 класс Сулы ерітінділер. Тірі ағза сұйықтықтарындағы тепе-теңдік
Сулы ерітінділер. Тірі ағза сұйықтықтарындағы тепе-теңдік Сера и ее соединения
Сера и ее соединения Термохимия. Расчет тепловых эффектов химических реакций
Термохимия. Расчет тепловых эффектов химических реакций Реакции SR в ряду алканов
Реакции SR в ряду алканов Классификация химических реакций. 8 класс
Классификация химических реакций. 8 класс Спирты, фенолы, тиолы
Спирты, фенолы, тиолы Оксиды. 8 класс
Оксиды. 8 класс Чистые вещества и смеси (продолжение)
Чистые вещества и смеси (продолжение) Природный и попутный нефтяной газы
Природный и попутный нефтяной газы Предмет и задачи химии. Вещества и их свойства (продолжение)
Предмет и задачи химии. Вещества и их свойства (продолжение)