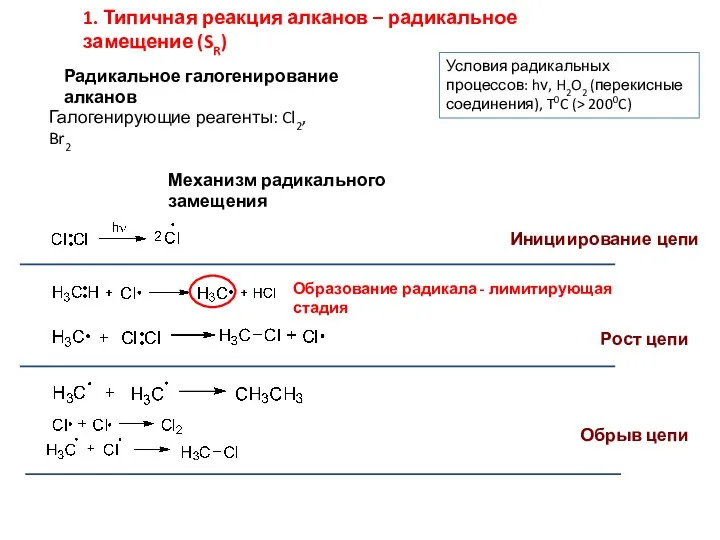
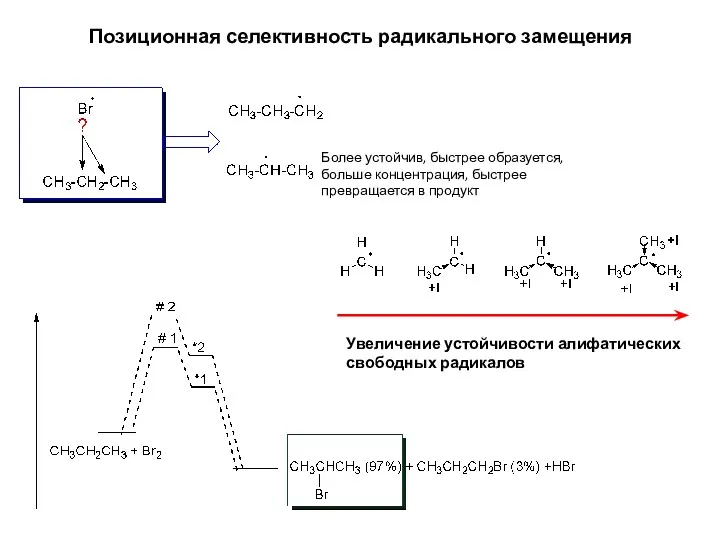
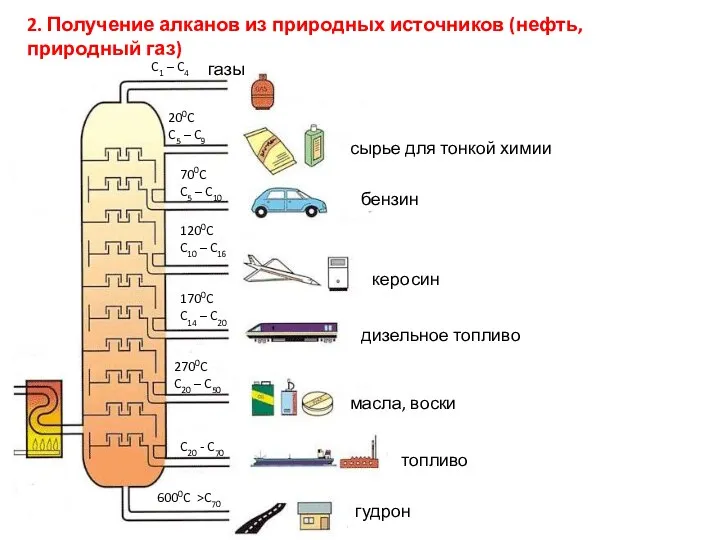
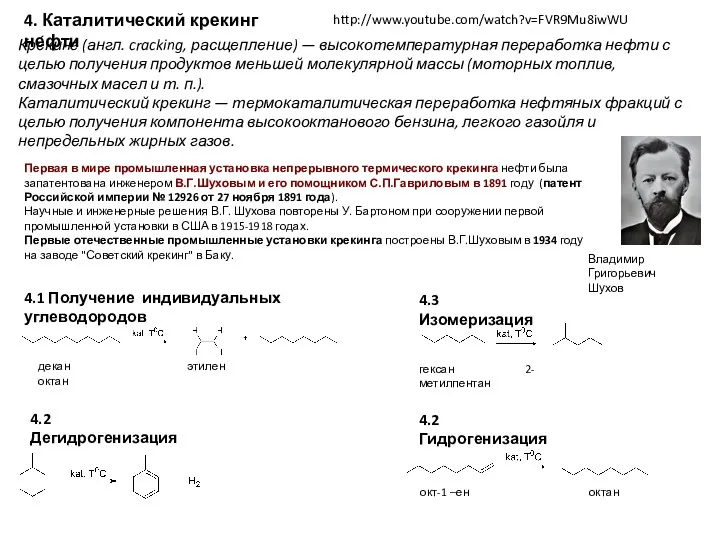
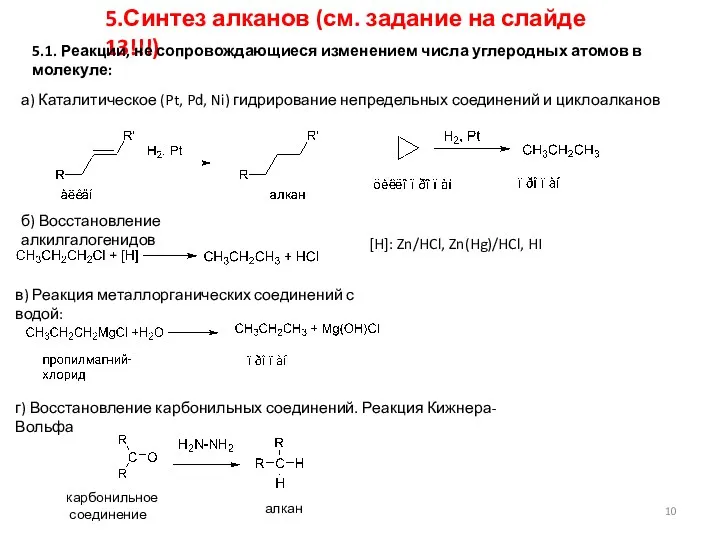
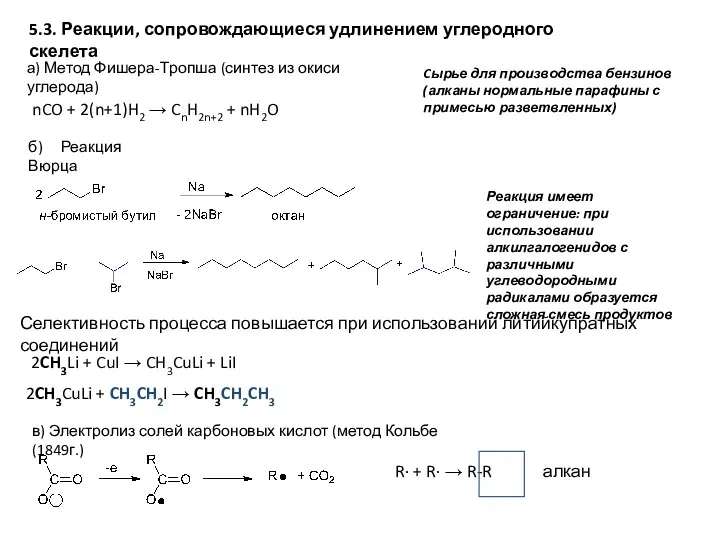
4. Каталитический крекинг нефти
Кре́кинг (англ. cracking, расщепление) — высокотемпературная переработка
нефти с целью получения продуктов меньшей молекулярной массы (моторных топлив, смазочных масел и т. п.).
Каталитический крекинг — термокаталитическая переработка нефтяных фракций с целью получения компонента высокооктанового бензина, легкого газойля и непредельных жирных газов.
Владимир Григорьевич
Шухов
Первая в мире промышленная установка непрерывного термического крекинга нефти была запатентована инженером В.Г.Шуховым и его помощником С.П.Гавриловым в 1891 году (патент Российской империи № 12926 от 27 ноября 1891 года).
Научные и инженерные решения В.Г. Шухова повторены У. Бартоном при сооружении первой промышленной установки в США в 1915-1918 годах.
Первые отечественные промышленные установки крекинга построены В.Г.Шуховым в 1934 году на заводе "Советский крекинг" в Баку.
http://www.youtube.com/watch?v=FVR9Mu8iwWU
4.2 Дегидрогенизация
4.2 Гидрогенизация
окт-1 –ен октан
4.3 Изомеризация
гексан 2-метилпентан
4.1 Получение индивидуальных углеводородов
декан этилен октан





 Sulfur and its compounds. Contact method for producing sulfuric acid
Sulfur and its compounds. Contact method for producing sulfuric acid Материаловедение и технологии конструкционных материалов
Материаловедение и технологии конструкционных материалов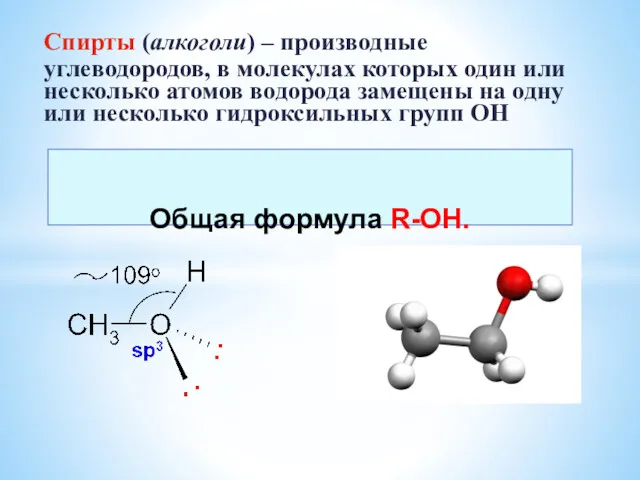 Спирты. Многоатомные спирты
Спирты. Многоатомные спирты Соли. Определение солей
Соли. Определение солей The role of chemistry in the solution of the food problem
The role of chemistry in the solution of the food problem Адсорбция. Физическая и химическая адсорбция
Адсорбция. Физическая и химическая адсорбция Актиноиды. Физические и химические свойства
Актиноиды. Физические и химические свойства Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Стекловолокно. Что такое стекловолокно?
Стекловолокно. Что такое стекловолокно? Три правила взаимодействия элементов симметрии
Три правила взаимодействия элементов симметрии Простые и сложные полиэфиры. Пентапласт
Простые и сложные полиэфиры. Пентапласт Вольфрам — химический элемент
Вольфрам — химический элемент Виды присадок к моторным топливам. Присадки к дизельному топливу
Виды присадок к моторным топливам. Присадки к дизельному топливу Совйства спиртов. 10 класс
Совйства спиртов. 10 класс Чистые вещества и смеси (продолжение)
Чистые вещества и смеси (продолжение) Растворы. Процесс растворения
Растворы. Процесс растворения Сульфиды. Лекция 6
Сульфиды. Лекция 6 Термопластичные полимеры
Термопластичные полимеры Состав, свойства и роль молока в жизни человека
Состав, свойства и роль молока в жизни человека Фенолы. Классификация фенолов
Фенолы. Классификация фенолов Биологически важные окислительно-восстановительные реакции органических соединений
Биологически важные окислительно-восстановительные реакции органических соединений Непредельные углеводороды. Алкены. Номенклатура алкенов
Непредельные углеводороды. Алкены. Номенклатура алкенов Сложные эфиры. Жиры. Мыла
Сложные эфиры. Жиры. Мыла Карбоновые кислоты. 10 класс
Карбоновые кислоты. 10 класс Явища природи. Фізичні явища, їх різноманітність. Хімічні явища, їх ознаки. Горіння. Гниття
Явища природи. Фізичні явища, їх різноманітність. Хімічні явища, їх ознаки. Горіння. Гниття Азотные удобрения
Азотные удобрения Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю
Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю Количество вещества. Единица измерения вещества моль
Количество вещества. Единица измерения вещества моль