Содержание
- 2. Строение карбоновых кислот. Классификация. Номенклатура. Основные представители карбоновых кислот и их применение. Свойства карбоновых кислот. Оглавление
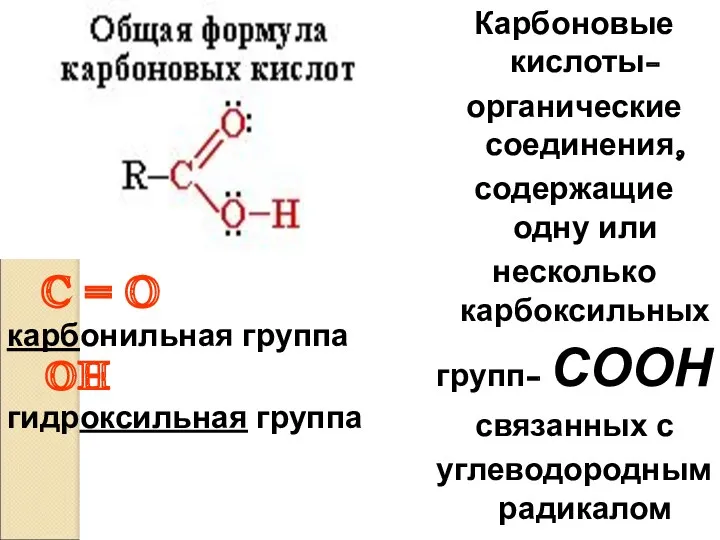
- 3. Карбоновые кислоты- органические соединения, содержащие одну или несколько карбоксильных групп- СООН связанных с углеводородным радикалом C
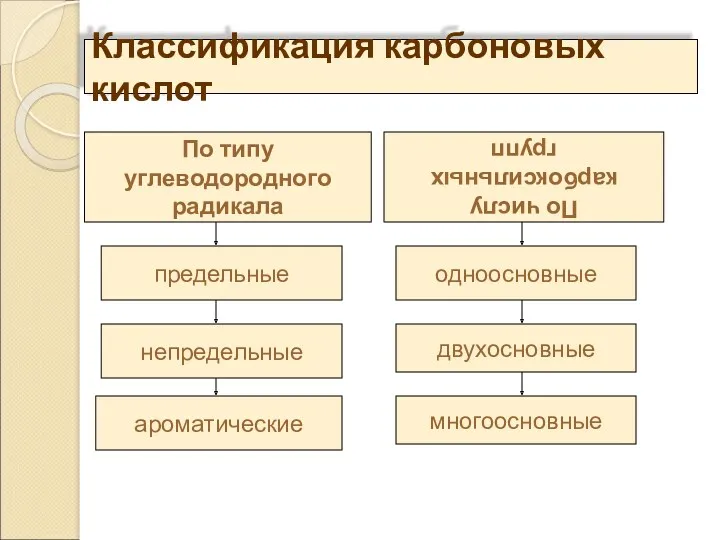
- 4. Классификация карбоновых кислот По числу карбоксильных групп непредельные ароматические одноосновные двухосновные многоосновные предельные По типу углеводородного
- 5. Общая формула одноосновных кислот предельного ряда СnH2n+1COOН где n может быть равно нулю.
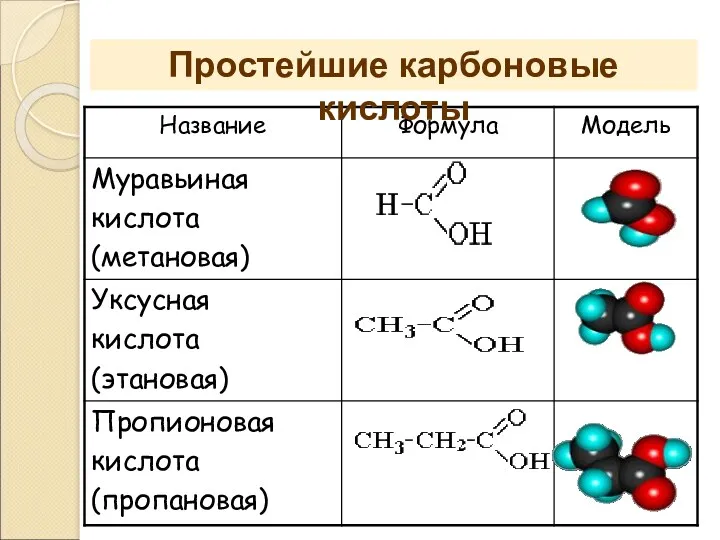
- 6. Простейшие карбоновые кислоты
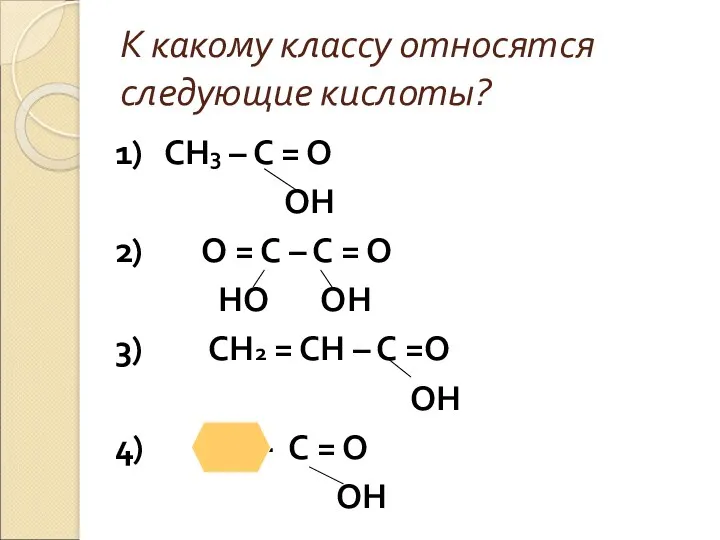
- 7. К какому классу относятся следующие кислоты? 1) СН3 – С = О ОН 2) О =
- 8. Алгоритм названий карбоновых кислот Главную цепь необходимо начинать нумеровать с карбоксильной группы. Указывают положение и название
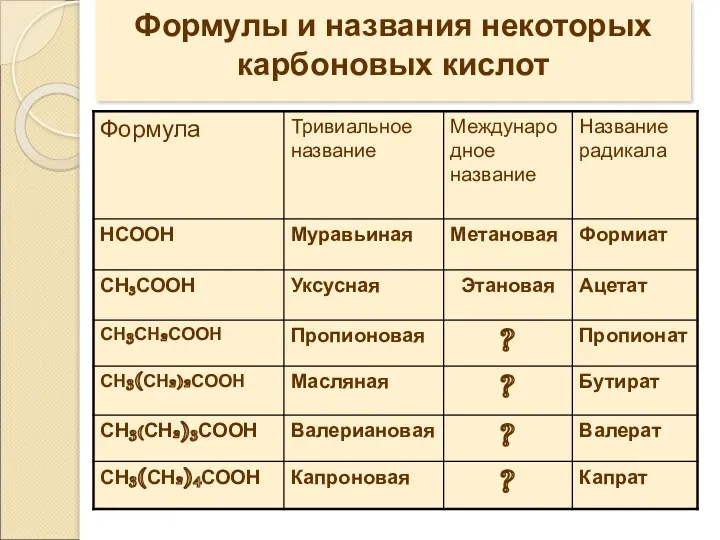
- 9. Формулы и названия некоторых карбоновых кислот
- 10. Алгоритм записи формул карбоновых кислот Выделить корень слова на основании, которого записать углеродный скелет в состав,
- 11. Составьте формулы: 2 метилбутановой кислоты; 2,2 диметилпропановой кислоты; 3,3 дихлоргексановой кислоты.
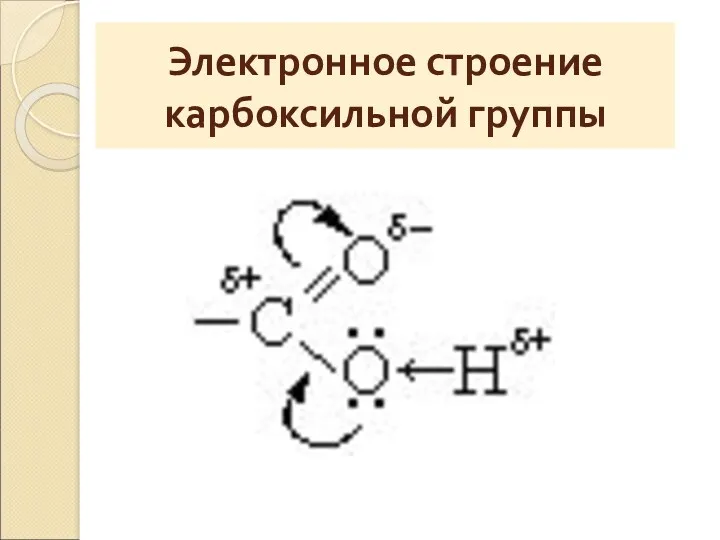
- 12. Электронное строение карбоксильной группы
- 13. Физические свойства предельных одноосновных карбоновых кислот в значительной степени обусловлены наличием между молекулами прочных водородных связей
- 14. Муравьиная кислота Содержится в ядовитых железах муравьев, в крапиве, в еловой хвое. В 10 раз сильнее
- 15. Свойства муравьиной кислоты Бесцветная жидкость с резким запахом, хорошо растворимая в воде. Может проявлять свойства характерные
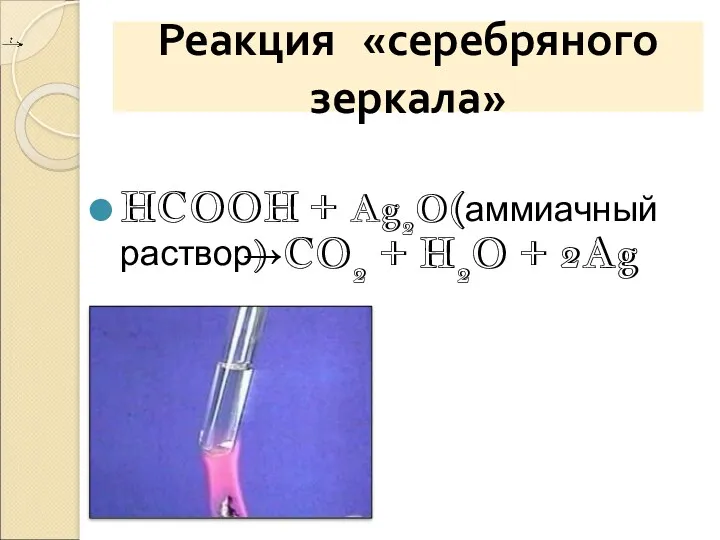
- 16. Реакция «серебряного зеркала» HCOOH + Ag2O(аммиачный раствор) →CO2 + H2O + 2Ag
- 17. Уксусная кислота Известна с незапамятных времен. В чистом виде выделена в 1700 г В 1845 г.
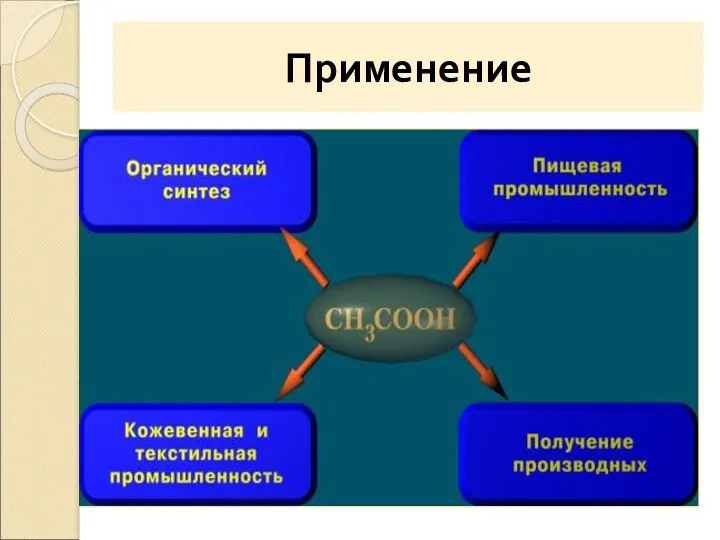
- 18. Применение
- 19. Химические свойства уксусной кислоты Опыт: «Действие на индикаторы». Опыт: «Взаимодействие с металлами».
- 20. С какими из перечисленных соединений будет реагировать уксусная кислота? Этан, этанол, пропан, гидроксид натрия, соляная кислота,
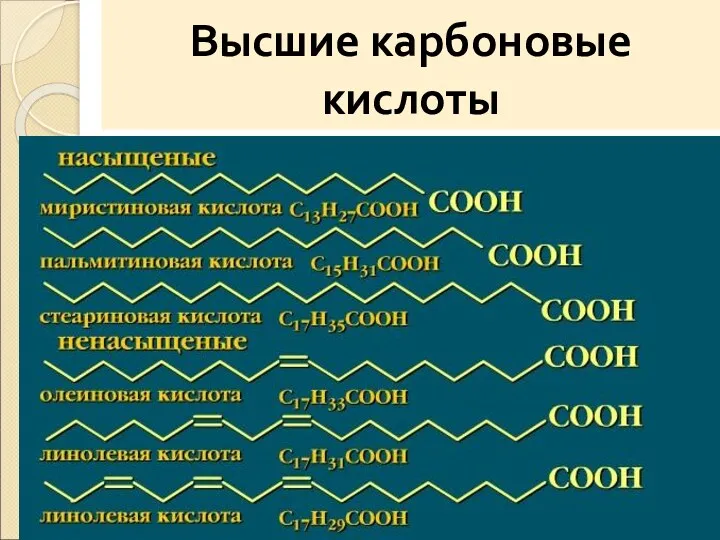
- 21. Высшие карбоновые кислоты
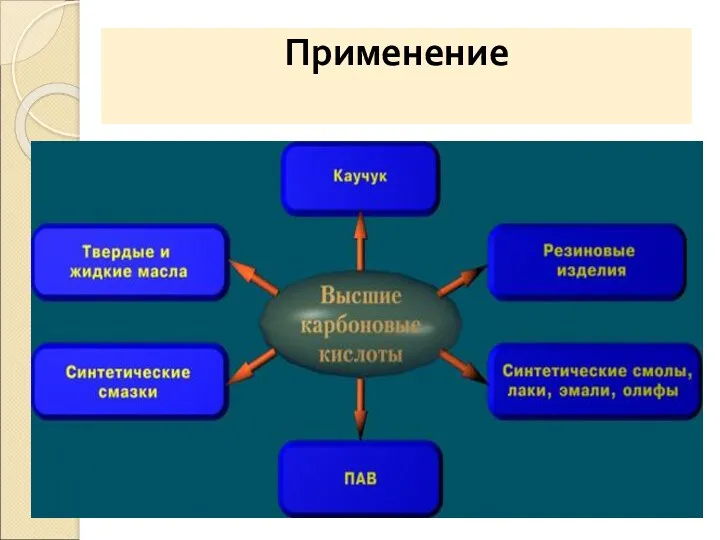
- 22. Применение
- 23. Получение карбоновых кислот Окисление альдегидов. В промышленности: 2RCHO + O2 →2RCOOH Лабораторные окислители: Ag2O, Cu(OH)2, KMnO4
- 24. Какой информацией я владею после урока: Знаю состав органических кислот. Знаю состав и классификацию органических кислот.
- 25. Домашнее задание: Задачи Какая масса гидроксида калия потребуется для полной нейтрализации 360 г 35% раствора уксусной
- 27. Скачать презентацию














 Химические формулы
Химические формулы Удивительные свойства воды
Удивительные свойства воды Графен. Свойства и получение. Функционализация и применение композитов на его основе
Графен. Свойства и получение. Функционализация и применение композитов на его основе Значення хімії у повсякденному житті
Значення хімії у повсякденному житті Конструкционные функциональные волокнистые композиты. Стеклопластики
Конструкционные функциональные волокнистые композиты. Стеклопластики Характеристика элементов VI группы .Кислород. Озон
Характеристика элементов VI группы .Кислород. Озон Химический состав водоотталкивающих средств
Химический состав водоотталкивающих средств Процессы нитрозирования и основные реакции диазосоединений
Процессы нитрозирования и основные реакции диазосоединений Благородные газы
Благородные газы Алюминий и его свойства
Алюминий и его свойства Химические реакторы. Лекция №10
Химические реакторы. Лекция №10 Классификация химических реакций
Классификация химических реакций Жесткость воды и способы её устранения
Жесткость воды и способы её устранения Галогени. Хімічні властивості
Галогени. Хімічні властивості Вода
Вода Классификация химических реакций (11 класс)
Классификация химических реакций (11 класс) Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Iron Oxide
Iron Oxide Electrochemistry
Electrochemistry Теория электролитической диссоциации
Теория электролитической диссоциации Газовые смеси
Газовые смеси Оксид меди
Оксид меди Кислоты. Определение и классификация
Кислоты. Определение и классификация Решение задачи №4. Старость - на радость. Команда Карбораны
Решение задачи №4. Старость - на радость. Команда Карбораны Элементы IV группы главной подгруппы. Углерод
Элементы IV группы главной подгруппы. Углерод Альтернативная елочка из кристаллов
Альтернативная елочка из кристаллов Созвездие талантов. Игра-зачет по теме Основные классы неорганической химии 8 класс
Созвездие талантов. Игра-зачет по теме Основные классы неорганической химии 8 класс Кислые породы повышенной щелочности и щелочные
Кислые породы повышенной щелочности и щелочные