Слайд 2

Химическая реакция - это процесс превращения исходных веществ (реагентов) в продукты
реакции
Классификация - распределение на группы по сходным признакам
Слайд 3

2.1. по числу и составу реагирующих и образующихся веществ:
а) соединения
б) разложения
в)
замещения
г) обмена
Слайд 4
Реакции соединения:
А + В => АВ
из двух или нескольких веществ получается
одно, более сложное вещество
Слайд 5
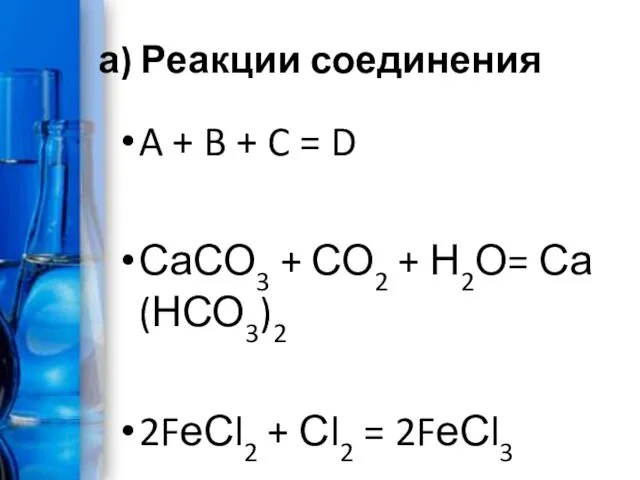
а) Реакции соединения
A + B + C = D
СаСО3 + СО2 + Н2О=
Са(НСО3)2
2FеСl2 + Сl2 = 2FеСl3
Слайд 6
Реакции разложения:
АВ => А + В
из одного сложного вещества
образуются два или несколько простых или менее сложных веществ
Слайд 7
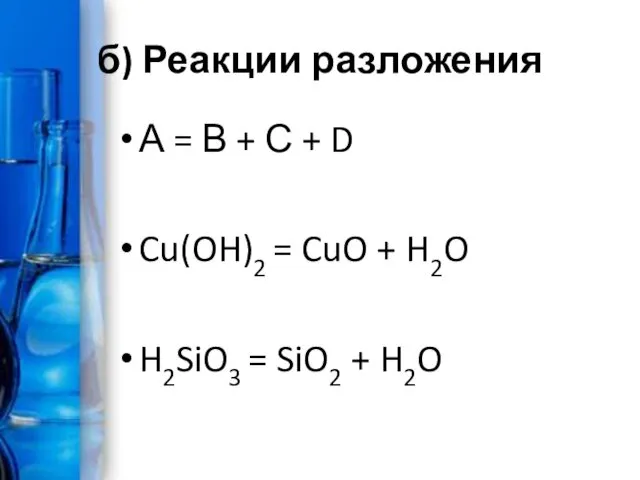
б) Реакции разложения
А = В + С + D
Cu(OH)2 = CuO
+ H2O
H2SiO3 = SiO2 + H2O
Слайд 8
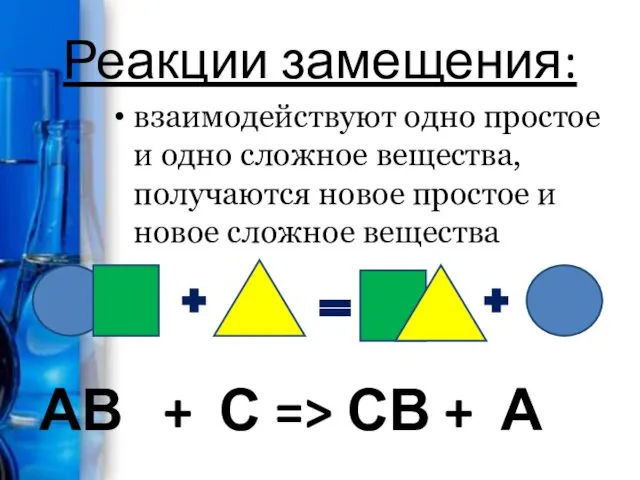
Реакции замещения:
АВ + С => СВ + А
взаимодействуют одно простое и одно
сложное вещества, получаются новое простое и новое сложное вещества
Слайд 9

в) Реакции замещения
А + ВС = АВ + С
2Аl + Fe2O3 =
2Fе + Аl2О3
Zn + 2НСl = ZnСl2 + Н2
Слайд 10
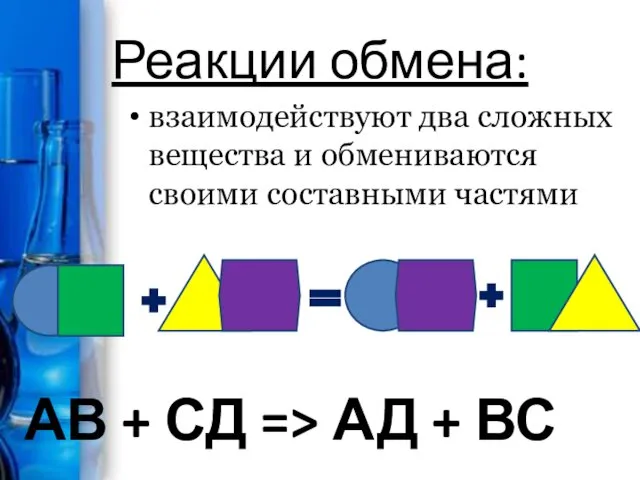
Реакции обмена:
АВ + СД => АД + ВС
взаимодействуют два сложных вещества
и обмениваются своими составными частями
Слайд 11
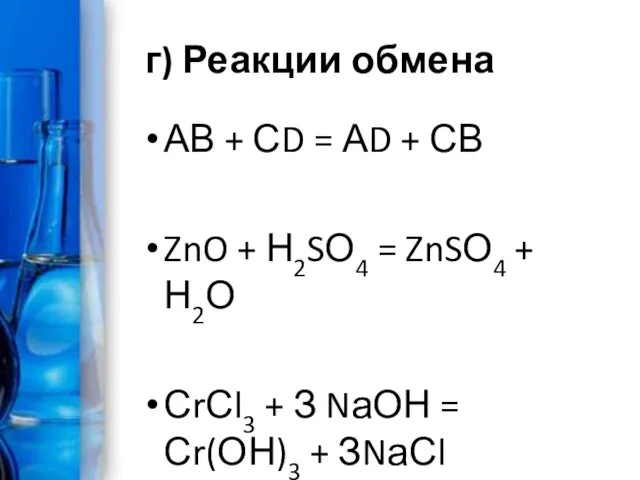
г) Реакции обмена
АВ + СD = АD + СВ
ZnO + Н2SО4 =
ZnSО4 + Н2О
СrСl3 + З NаОН = Сr(ОН)3 + ЗNаСl










 Кислоты. Состав кислот
Кислоты. Состав кислот Реакції йонного обміну. Йонно-молекулярні рівняння
Реакції йонного обміну. Йонно-молекулярні рівняння Амфотерные соединения
Амфотерные соединения Гетероциклические соединения
Гетероциклические соединения Фенолы. Химические свойства и способы получения
Фенолы. Химические свойства и способы получения Chemical Formulas and Nomenclature of compounds
Chemical Formulas and Nomenclature of compounds Товары бытовой химии
Товары бытовой химии Кристаллофизика_часть_1
Кристаллофизика_часть_1 Тяжелые металлы. Опасность токсичных металлов для организма
Тяжелые металлы. Опасность токсичных металлов для организма Домашнее задание по теме Химические свойства альдегидов, их получение
Домашнее задание по теме Химические свойства альдегидов, их получение Электронные конфигурации атомов химических элементов. Графическое изображение электронных конфигураций атомов
Электронные конфигурации атомов химических элементов. Графическое изображение электронных конфигураций атомов Переработка газа. Первичная переработка нефти. Лекция 9
Переработка газа. Первичная переработка нефти. Лекция 9 Химические соединения в организме человека
Химические соединения в организме человека Способы и степень дробления
Способы и степень дробления Оксиды. Классификация оксидов
Оксиды. Классификация оксидов Осадочные и метаморфические горные породы
Осадочные и метаморфические горные породы Химическая термодинамика
Химическая термодинамика Свойства воды. Оценка качества
Свойства воды. Оценка качества Состав и свойства сжиженного газа. Вопрос №1
Состав и свойства сжиженного газа. Вопрос №1 Химический элемент фосфор
Химический элемент фосфор Углерод и его соединения
Углерод и его соединения Характеристика металу Ферум
Характеристика металу Ферум Separation amp confirmation
Separation amp confirmation Оксиды. Физические свойства
Оксиды. Физические свойства Галогены. Нахождение в природе
Галогены. Нахождение в природе Химия и проблемы экологии. Кислотные дожди
Химия и проблемы экологии. Кислотные дожди Алкины. Гомологический ряд, получение, свойства и применение
Алкины. Гомологический ряд, получение, свойства и применение Биоорганическая химия
Биоорганическая химия