Содержание
- 2. Строение молекулы ацетилена С2Н2
- 4. Гомологический ряд ацетиленовых CnH2n+2 - алканы CnH2n-2 – Алкины CH4 - метан CH3 – CH3 –
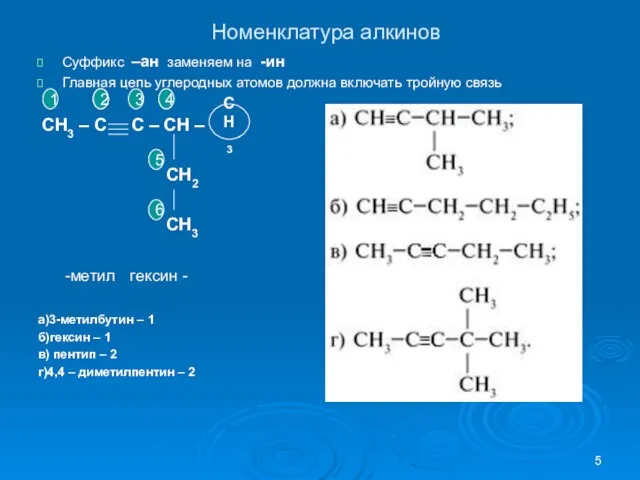
- 5. Номенклатура алкинов Суффикс –ан заменяем на -ин Главная цепь углеродных атомов должна включать тройную связь СН3
- 6. Изомерия алкинов Изомерия положения двойной связи Изомерия цепи Межклассовая изомерия С4Н6 (2 изомера) НС = С
- 7. Физические свойства Плохо растворимы в воде С2 по С4 – газы С5 по С15 – жидкости
- 8. Химические свойства реакции присоединения Гидрирование осуществляется при нагревании с теми же металлическими катализаторами (Ni, Pd или
- 9. Правило В.В.Марковникова: водород присоединяется к наиболее гидрогенизированному атому углерода при двойной связи, то есть к атому
- 10. Гидратация (реакция Кучерова). Присоединение воды осуществляется в присутствии сульфата ртути. Эту реакцию открыл и исследовал в
- 11. Горение - Полное окисление 2СН≡ СН + 4O2 →CO2 + 2H2 O + 3C↓ Так как
- 12. Полимеризация. Алкины ввиду наличия тройной связи склонны к реакциям полимеризации, которые могут протекать в нескольких направлениях:
- 13. Особое свойство ацетилена – реакция замещения HC≡CH + Ag2O = AgC≡CAg + H2O аммиачный р-р ацетилинид
- 14. Получение алкинов Получение алкинов. 1.Высокотемпературный крекинг метана. 2.Гидролиз карбида кальция
- 16. Скачать презентацию












 Особенности строения соединений органической химии. 10 класс
Особенности строения соединений органической химии. 10 класс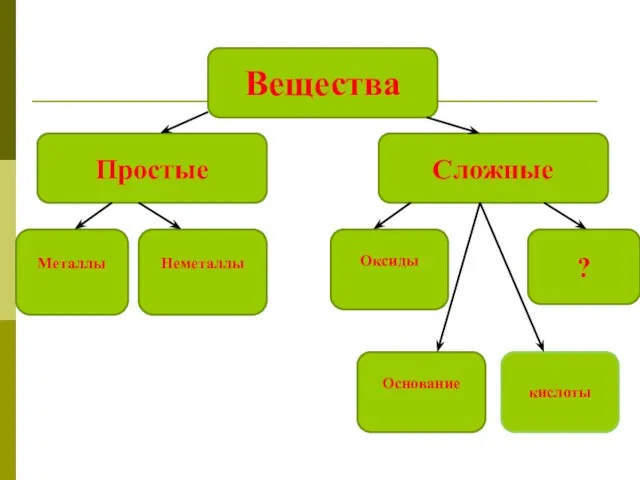 Соли, как производные кислот и оснований
Соли, как производные кислот и оснований Гидролиз органических и неорганических веществ
Гидролиз органических и неорганических веществ Периодический закон и периодическая система Д.И. Менделеева
Периодический закон и периодическая система Д.И. Менделеева 20231110_zakon_avogadro
20231110_zakon_avogadro Спирты. Понятия о предельных одноатомных спиртах. Химические свойства этанола и его применение
Спирты. Понятия о предельных одноатомных спиртах. Химические свойства этанола и его применение Химический элемент кремний
Химический элемент кремний Степень окисления. Бинарные соединения
Степень окисления. Бинарные соединения Основные классы неорганических соединений
Основные классы неорганических соединений Алкины
Алкины Классы органических соединений
Классы органических соединений Периодический закон Д.И. Менделеева
Периодический закон Д.И. Менделеева Непредельные углеводороды
Непредельные углеводороды Нитросоединения
Нитросоединения Металлы. Общие свойства и получение
Металлы. Общие свойства и получение Закон действующих масс и его применение в аналитической химии
Закон действующих масс и его применение в аналитической химии Гидролиз солей
Гидролиз солей Степени окисления атомов и формулы веществ
Степени окисления атомов и формулы веществ Неравновесные явления в сложных химических процессах. Часть 1: электрохимия
Неравновесные явления в сложных химических процессах. Часть 1: электрохимия Закон сохранения массы веществ
Закон сохранения массы веществ Дисахаридтер. Сахароза
Дисахаридтер. Сахароза Функціональні матеріали для високоенергетичної електроніки. (Лекція 2)
Функціональні матеріали для високоенергетичної електроніки. (Лекція 2) Защита от коррозии каменных и бетонных строительных материалов и конструкций
Защита от коррозии каменных и бетонных строительных материалов и конструкций Гидролиз органических и неорганических соединений
Гидролиз органических и неорганических соединений Общая химия
Общая химия Марганец и хром
Марганец и хром Теория электролитической диссоциации
Теория электролитической диссоциации Лекция 5. Нуклеофильное замещение при насыщенном атоме углерода
Лекция 5. Нуклеофильное замещение при насыщенном атоме углерода