Содержание
- 2. ЛИТЕРАТУРА Физическая химия. Кн. 2, Электрохимия. Химическая кинетика и катализ : Учеб. Пособие для вузов: В
- 3. Раздел 1. Термодинамика растворов электролитов и электрохимических систем 1.1. Общие понятия об электрохимических системах Электрохимия –
- 4. 1.2. Проводники электрических зарядов Проводники электрического тока делятся на электронные, или проводники I рода, и ионные
- 5. Электролиз – это химическое превращение в электрической системе под действием внешнего электрического поля. При электролизе отрицательные
- 6. Соотношение между (количеством) массой прореагировавших веществ и количеством постоянного электрического выражается законами Фарадея. I закон Фарадея:
- 7. II закон Фарадея дает физический смысл Kэ: Кэ – это количество вещества, которое претерпевает превращение при
- 8. Диссоциация воды: H2O ⇆ H+ + OH- Ионы щелочных металлов не восстанавливаются, на катоде идет восстановление
- 9. 2. Растворы электролитов и их свойства 2.1. Сильные и слабые электролиты Электролитами называют вещества, которые в
- 10. К слабым электролитам относят слабые кислоты (H2SO4, H3PO4, CH3COOH), слабые основания (NH4OH) и некоторые соли (HgCI2).
- 11. 2.2. Электролитическая диссоциация в растворе Процесс распада растворенного вещества в растворе на ионы называется электролитической диссоциацией.
- 12. В состоянии равновесия доля молекул, распавшихся на ионы, характеризует степень диссоциации электролита которая зависит от: природы
- 13. Свойства растворов электролитов существенно отличаются от свойств идеальных растворов. Это объясняется увеличением числа частиц в растворе
- 14. Ионы в растворах электролитов сольватированы молекулами растворителя, поэтому при написании выражений для константы диссоциации необходимо учитывать
- 15. Сложнее обстоит дело с диссоциацией двухосновных кислот (H2S, H2CO3, H2SO3 и т.д.) Обозначим их общей формулой
- 16. 2.3. Механизм переноса тока в растворах электролитов. В растворе электролита сольватированные ионы находятся в беспорядочном тепловом
- 17. Абсолютная скорость движения (подвижность) ионов ui не зависит от Е и h и определяется соотношением Абсолютная
- 18. 2.4. Удельная и эквивалентная электрические проводимости растворов электролитов Мерой способности проводить электрический ток является электрическая проводимость
- 19. æ зависит от концентрации растворов, Р и Т. В области высоких концентраций снижается скорость движения ионов
- 20. Эквивалентной электропроводимостью электролитов называют электропроводимость такого объема раствора V=1/c, в котором содержится 1 г-экв вещества и
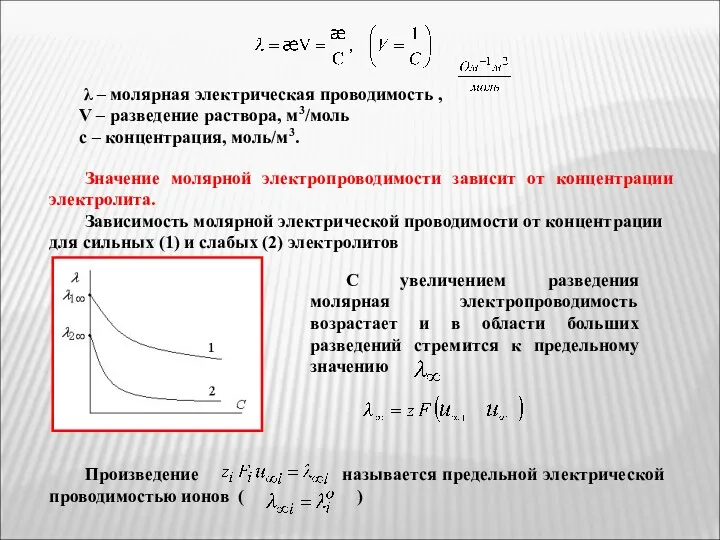
- 21. λ – молярная электрическая проводимость , V – разведение раствора, м3/моль с – концентрация, моль/м3. Значение
- 22. Гипотетический бесконечно разбавленный раствор характеризуется полной диссоциацией электролита и отсутствием электростатических сил. λ ∞ иона =
- 23. Теория электролитической проводимости растворов Дебая - Онзагера: Снижение молярной электрической проводимости при переходе от разбавленных растворов
- 24. 2.6. Молярная электрическая проводимость ионов гидроксония и гидроксида В водных растворах протон (ион) водорода записывают в
- 25. 1. При наложении электрического поля переход протона от H3O+ к молекуле воды повышается в направлении поля.
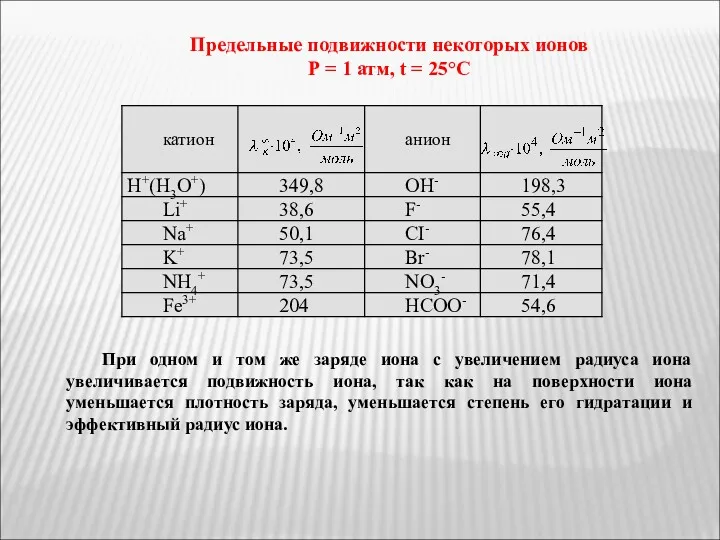
- 26. Предельные подвижности некоторых ионов Р = 1 атм, t = 25°С При одном и том же
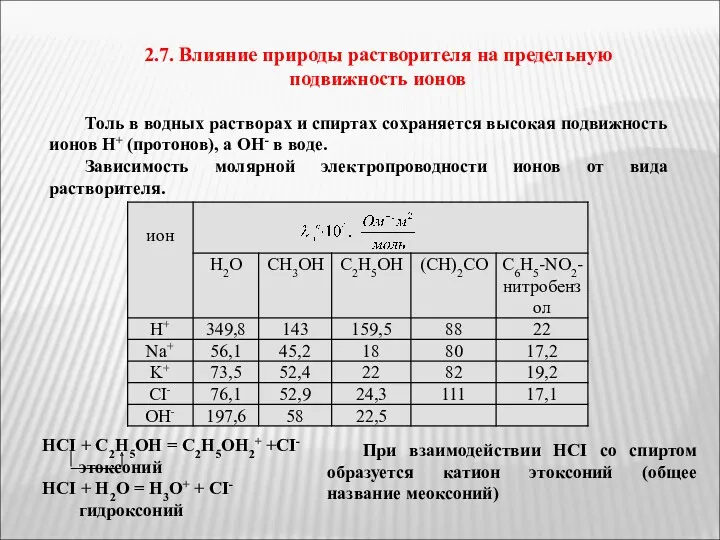
- 27. 2.7. Влияние природы растворителя на предельную подвижность ионов Толь в водных растворах и спиртах сохраняется высокая
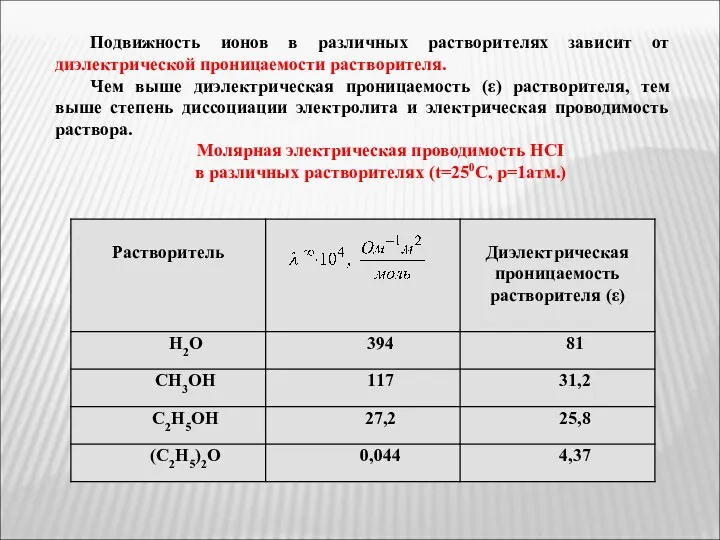
- 28. Подвижность ионов в различных растворителях зависит от диэлектрической проницаемости растворителя. Чем выше диэлектрическая проницаемость (ε) растворителя,
- 29. 2.8. Зависимость молярной электропроводимости от температуры Изменение электропроводимости раствора проводят в термостате, т.к. она в сильной
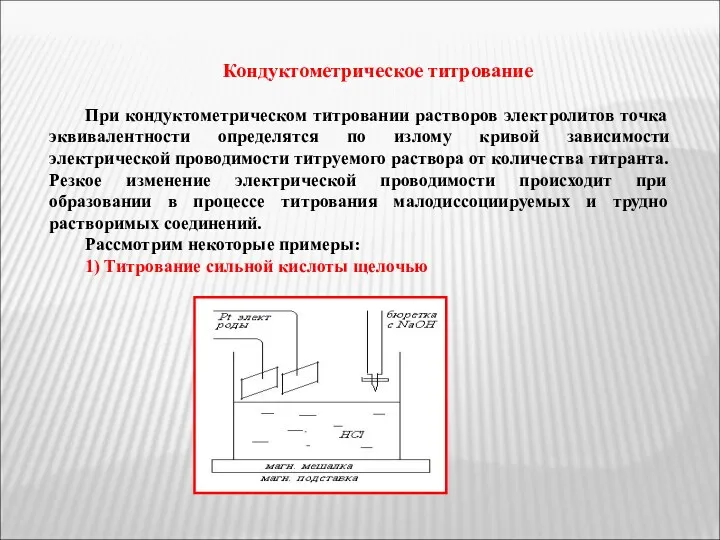
- 30. Кондуктометрическое титрование При кондуктометрическом титровании растворов электролитов точка эквивалентности определятся по излому кривой зависимости электрической проводимости
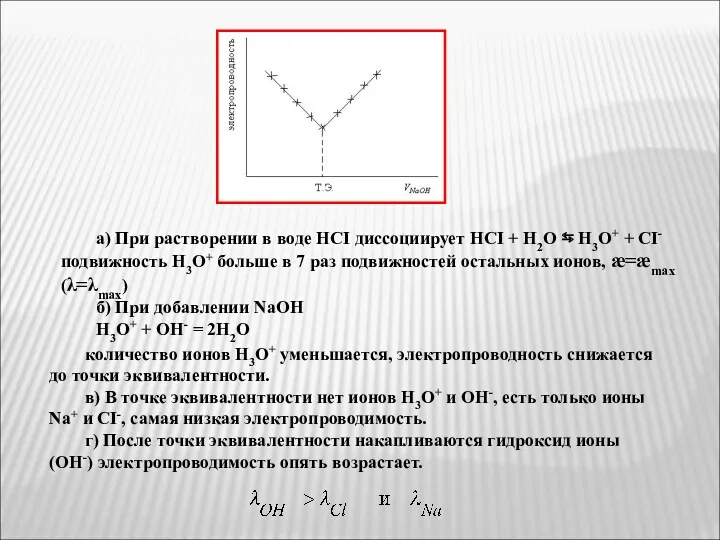
- 31. а) При растворении в воде HCI диссоциирует HCI + H2O ⇆ H3O+ + CI- подвижность H3O+
- 32. Если вместо NaOH взять любую щелочь (NH4OH), α =10-2, то линия после точки эвтектики пойдет ниже
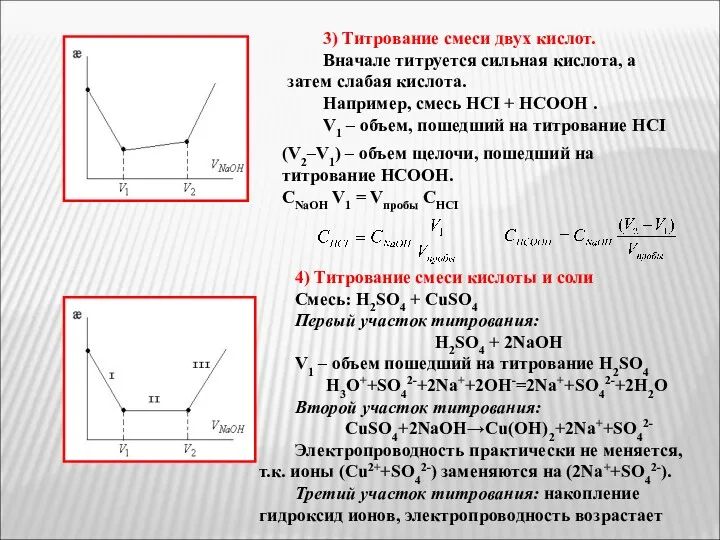
- 33. 3) Титрование смеси двух кислот. Вначале титруется сильная кислота, а затем слабая кислота. Например, смесь HCI
- 34. 3. Ионные равновесия в растворах электролитов 3.1. Термодинамическая константа диссоциации растворов электролитов Константа равновесия любого химического
- 35. Обычно в растворах С0,1≫С0,2, т.е. концентрация растворителя значительно больше концентрации растворенного вещества. Кдисс включает в себя
- 36. Кс – концентрационная константа диссоциации, которая зависит от С, Т и природы растворителя. Выразим Кс через
- 37. Значение константы Кс можно определить экспериментальным путем по значению α: λ ∞ рассчитывают по уравнению Кольрауша:
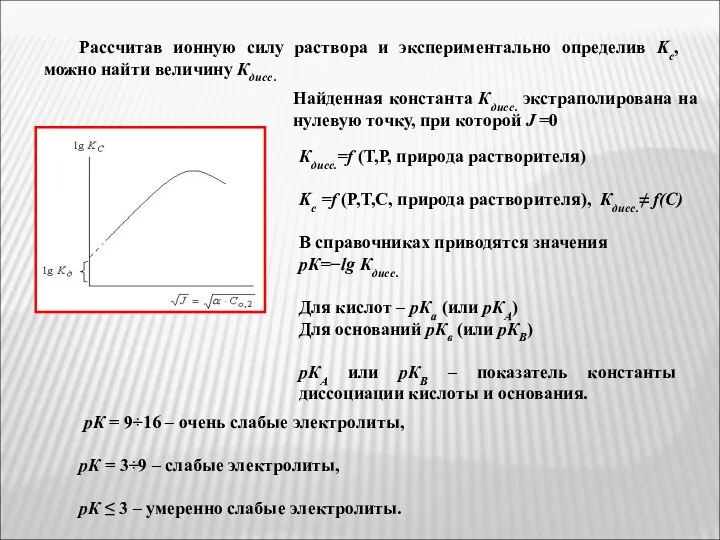
- 38. Рассчитав ионную силу раствора и экспериментально определив Kc, можно найти величину Кдисс. Найденная константа Кдисс. экстраполирована
- 39. Кислотно-основная теория Бренстеда Согласно теории протолитических равновесий Аррениуса кислотой (НА) является соединение, диссоциирующее на протоны Н+
- 40. 3.2. Диссоциация воды. Ионное произведение воды Вода – это довольно слабый электролит. Рассмотрим диссоциацию воды: Н2О
- 41. По уравнению Дебая – Хюккеля С→0; Ионная сила воды Кд определяется концентрацией Н2О. - это ионное
- 42. В чистой воде моль/л Зоренсоном был введен водородный показатель рН как От значений Кw рассчитывается шкала
- 43. Раздел 2. Гальванический элемент 2.1. ЭДС электрохимической системы. Электродный потенциал Электрохимическая цепь – представляет собой систему,
- 44. Где L1 и L2 – два раствора электролита, в которые опущены электроды, изготовленные из металлов М1
- 45. Водородный электрод взят в стандартном состоянии парциальное давление газа равно нормальному атмосферному р = 1,013∙105 Па.
- 46. 2.2. Строение ДЭС на границе раствор-металл Под строением ДЭС понимают распределение зарядов в его ионной обкладке.
- 47. Рассмотрим два случая: 1) , т.е. химический потенциал катиона в кристаллической решетке больше химического потенциала катиона
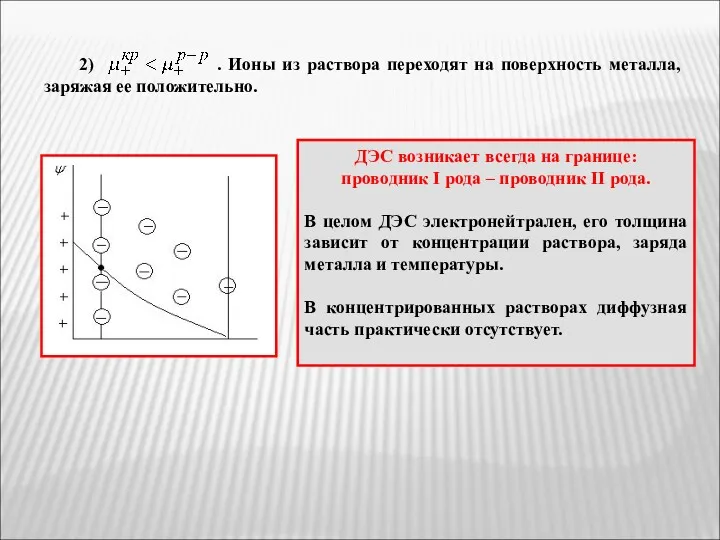
- 48. 2) . Ионы из раствора переходят на поверхность металла, заряжая ее положительно. ДЭС возникает всегда на
- 49. 2.3. Устройство и изображение гальванического элемента Гальваническим элементом называется любое устройство, дающее возможность получать электрический ток
- 50. Рассмотрим устройство химического ГЭ на примере элемента Даниеля-Якоби: Zn | Zn2+ ‖ Cu2+ | Cu Обычно
- 51. Zn + Cu2+ = Cu0 + Zn2+ - суммарная окислительно-восстановительная реакция. При протекании окислительно-восстановительной реакции возникает
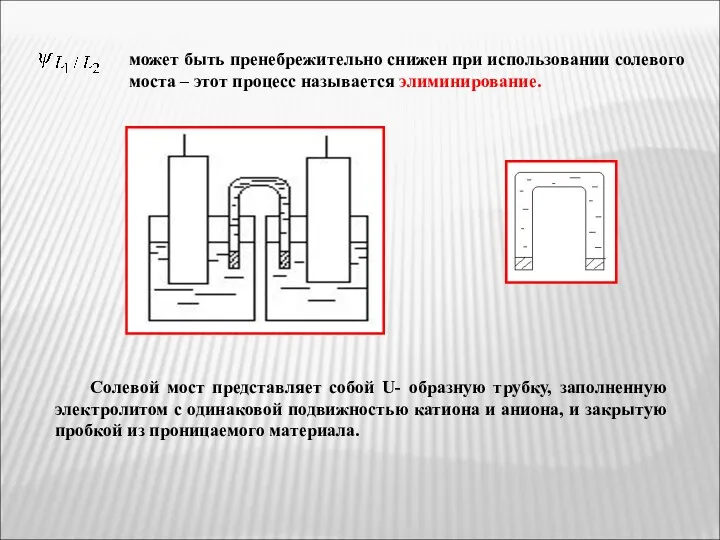
- 52. может быть пренебрежительно снижен при использовании солевого моста – этот процесс называется элиминирование. Солевой мост представляет
- 53. 2.4. Компенсационный метод измерения ЭДС Измерение ЭДС гальванического элемента компенсационным методом проводится при использовании потенциометра. Источником
- 54. 2.5. Термодинамика гальванического элемента Любой самопроизвольный процесс, протекающий при постоянном давлении и температуре, сопровождается уменьшением энергии
- 55. Измерение ЭДС гальванического элемента можно проводить компенсационным методом при любой температуре. С увеличением температуры ЭДС увеличивается
- 56. 2.6. Вывод уравнения Нернста для расчета ЭДС гальванического элемента Изменение энергии Гиббса в ходе химического процесса:
- 58. Скачать презентацию













































 Топлива и их свойства
Топлива и их свойства Жесткость воды
Жесткость воды Реакция обменного разложения веществ водой - гидролиз
Реакция обменного разложения веществ водой - гидролиз Svante Arrhenius and the theory of electrolytic and non-electrolytic dissociation
Svante Arrhenius and the theory of electrolytic and non-electrolytic dissociation Охрана труда в кабинете (лаборатории) химии образовательного учреждения
Охрана труда в кабинете (лаборатории) химии образовательного учреждения Фенол. Состав молекулы фенола
Фенол. Состав молекулы фенола Оксиди нітрогену
Оксиди нітрогену Химические свойства карбоновых кислот. Лабораторная работа № 8
Химические свойства карбоновых кислот. Лабораторная работа № 8 Строение атома
Строение атома Вуглеводи
Вуглеводи Витамины. Аскорбиновая кислота
Витамины. Аскорбиновая кислота Выделение транс-анетола из эфирных масел
Выделение транс-анетола из эфирных масел Соединения серы
Соединения серы Алюминий на кухне - опасный враг или верный помощник
Алюминий на кухне - опасный враг или верный помощник Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Производные фурана, пиррола, тиофена
Производные фурана, пиррола, тиофена Азот и его соединения
Азот и его соединения Галогенопроизводные углеводородов
Галогенопроизводные углеводородов Перегонка с водяным паром
Перегонка с водяным паром Пластмассы
Пластмассы Взаємодія кисню зі складними та простими речовинами. Урок 31. 7 клас
Взаємодія кисню зі складними та простими речовинами. Урок 31. 7 клас Nitraty
Nitraty 20231112_alkeny
20231112_alkeny Электрондардың атомдарда орналасуы
Электрондардың атомдарда орналасуы Псевдоморфозы. Образование псевдоморфоз
Псевдоморфозы. Образование псевдоморфоз Положение в ПСХЭ водорода, лантаноидов, актиноидов и искусственно полученных элементов
Положение в ПСХЭ водорода, лантаноидов, актиноидов и искусственно полученных элементов Философы химии Кант и Гегель
Философы химии Кант и Гегель топ през
топ през