Содержание
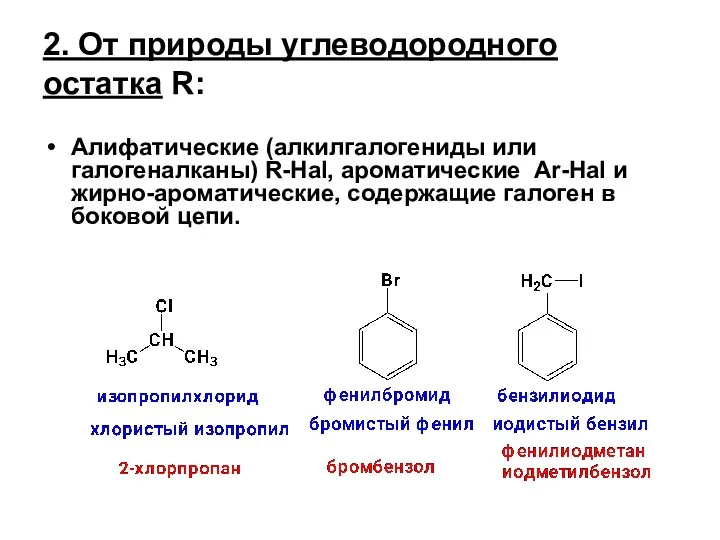
- 2. 2. От природы углеводородного остатка R: Алифатические (алкилгалогениды или галогеналканы) R-Hal, ароматические Ar-Hal и жирно-ароматические, содержащие
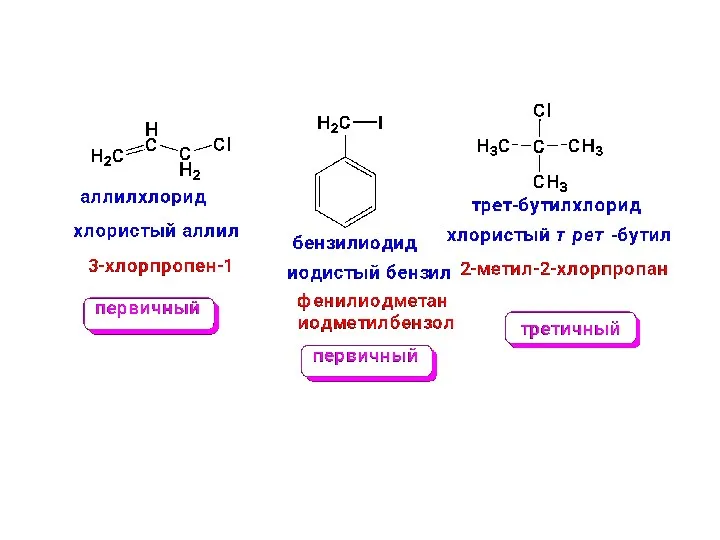
- 3. 3. По характеру С в sp3-гибридном состоянии, с которым связан галоген: Первичные – R-СН2- Hal, вторичные
- 4. Номенклатура Радикально-функциональные названия: строятся путем прибавления названия галогена в форме прилагательного перед названием R, или после
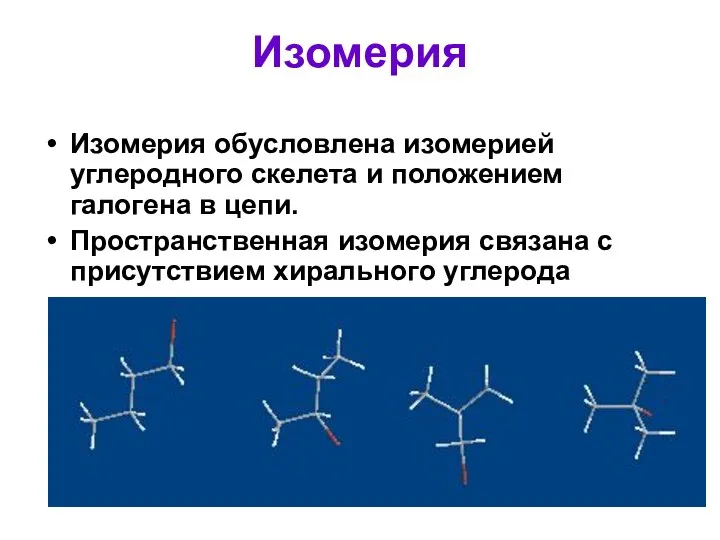
- 6. Изомерия Изомерия обусловлена изомерией углеродного скелета и положением галогена в цепи. Пространственная изомерия связана с присутствием
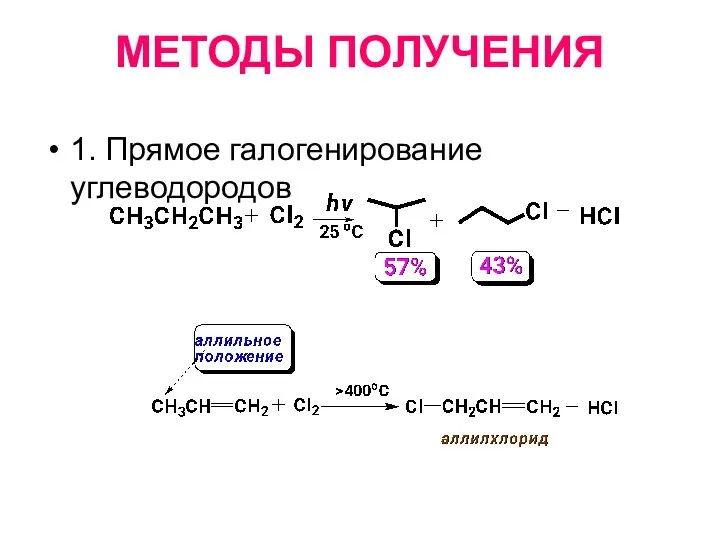
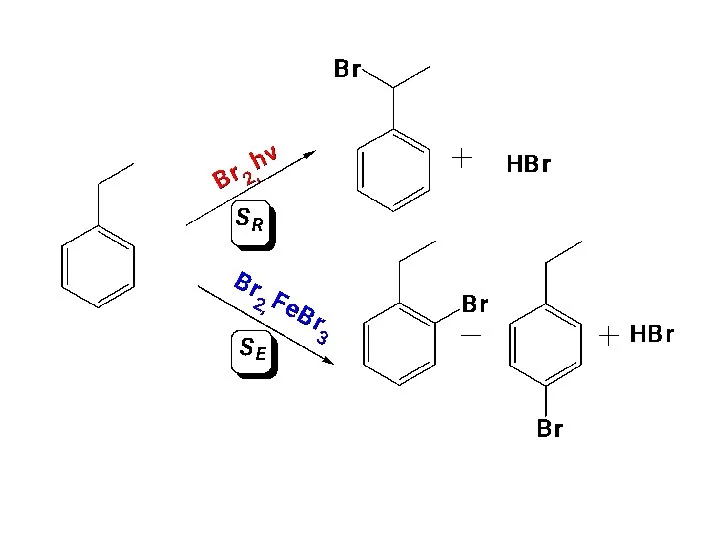
- 7. МЕТОДЫ ПОЛУЧЕНИЯ 1. Прямое галогенирование углеводородов
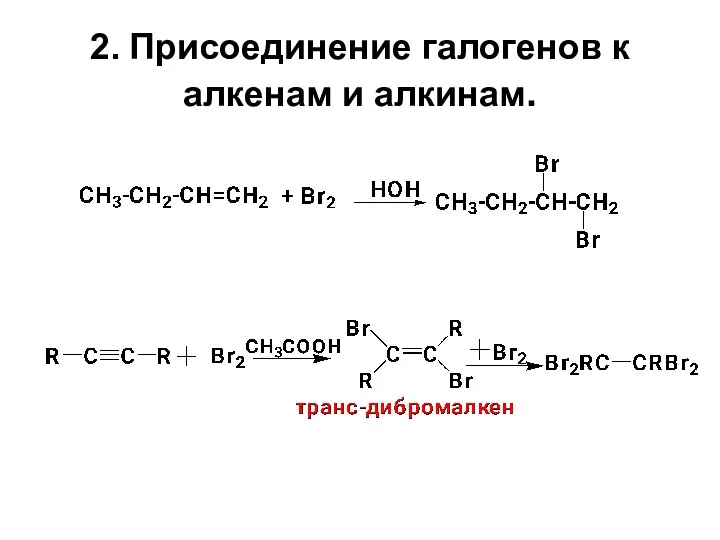
- 9. 2. Присоединение галогенов к алкенам и алкинам.
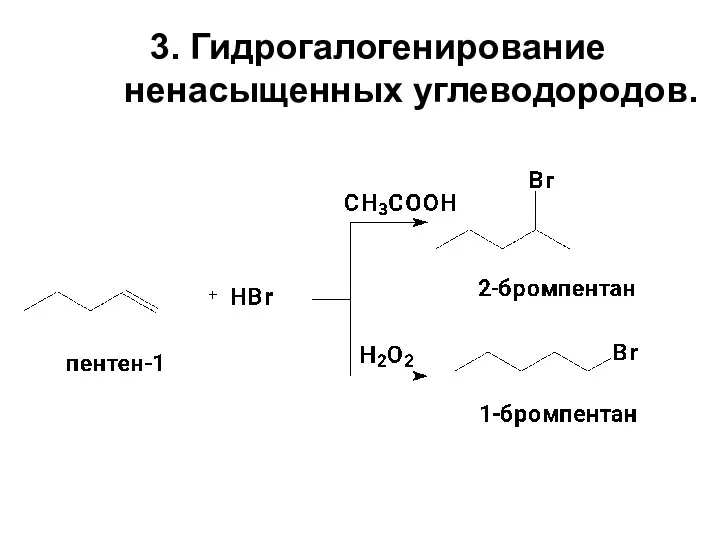
- 10. 3. Гидрогалогенирование ненасыщенных углеводородов.
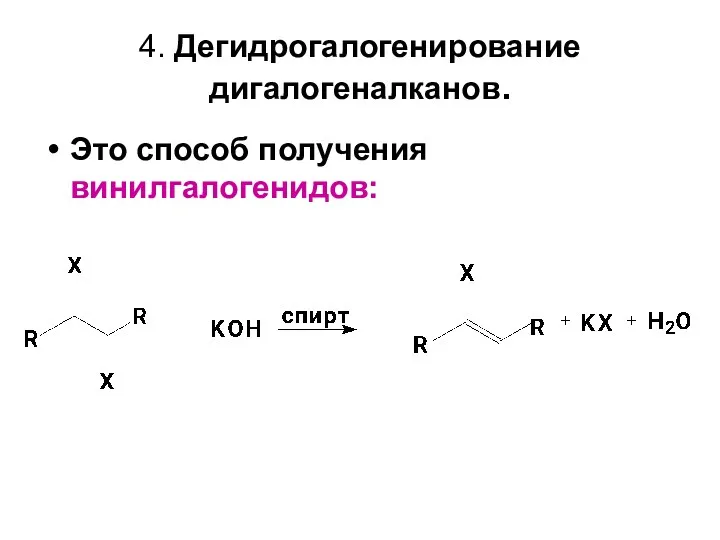
- 11. 4. Дегидрогалогенирование дигалогеналканов. Это способ получения винилгалогенидов:
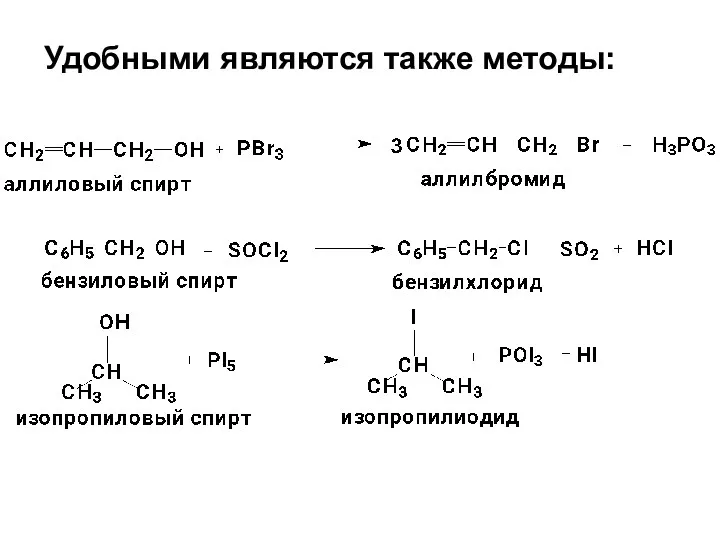
- 12. 5. Замещение HO-группы в спиртах на галоген. Реакционная способность спиртов уменьшается в ряду: третичный>вторичный>первичный.
- 13. Удобными являются также методы:
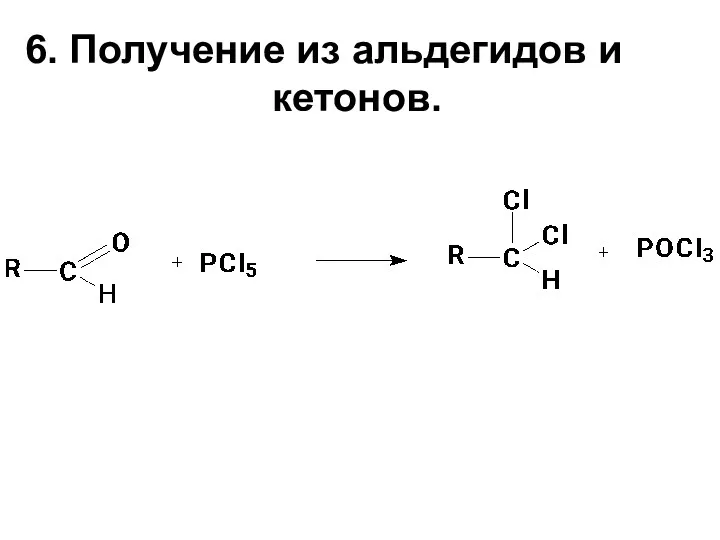
- 14. 6. Получение из альдегидов и кетонов.
- 15. 7. Получение иодпроизводных реакцией Финкельштейна
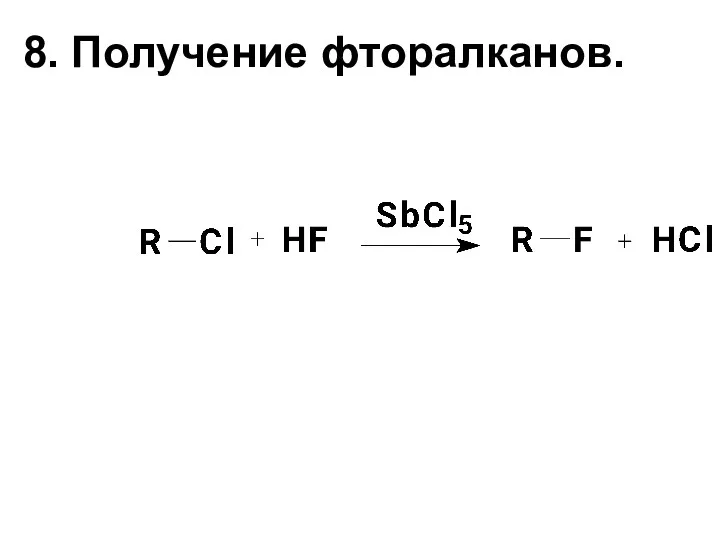
- 16. 8. Получение фторалканов.
- 17. ФИЗИЧЕСКИЕ СВОЙСТВА Физические свойства галогеналканов зависят от природы и числа атомов галогена в молекуле. Низшие и
- 18. Полифторалканы заметно отличаются по свойствам от других галогеналканов. Переход от одного галогена к другому заметно отражается
- 19. Галогеноуглеводороды – полярные соединения, но они почти нерастворимы в воде , так как не образуют с
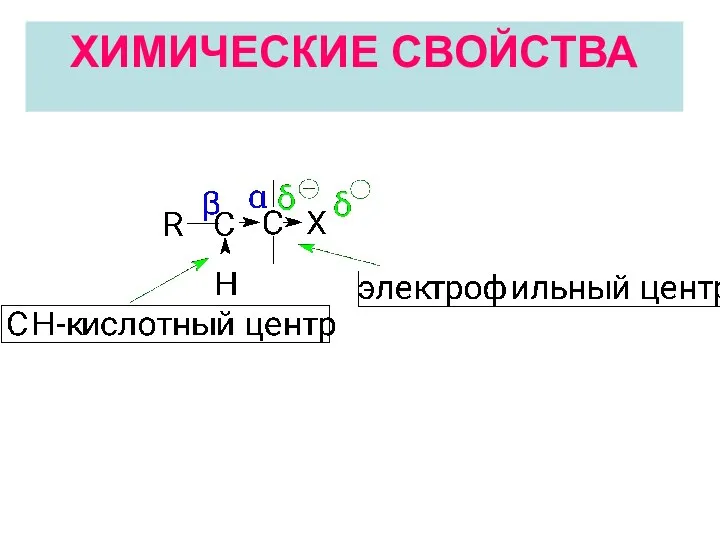
- 20. ХИМИЧЕСКИЕ СВОЙСТВА
- 21. Электрофильный центр (α-атом углерода) возникает вследствие поляризации связи С-Нal и может подвергаться атаке нуклеофилом. В результате
- 22. 1. Реакции нуклеофилов–наиболее распространенные превращения галогеналканов. Именно эти реакции позволяют вводить в органические соединения самые разнообразные
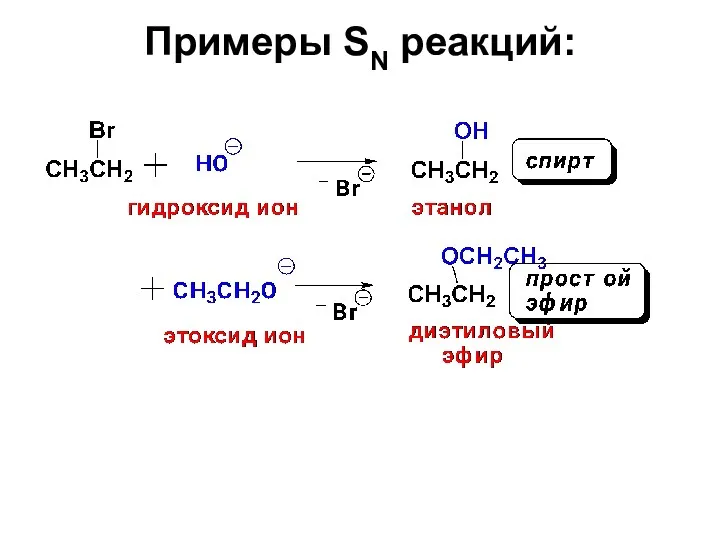
- 23. Примеры SN реакций:
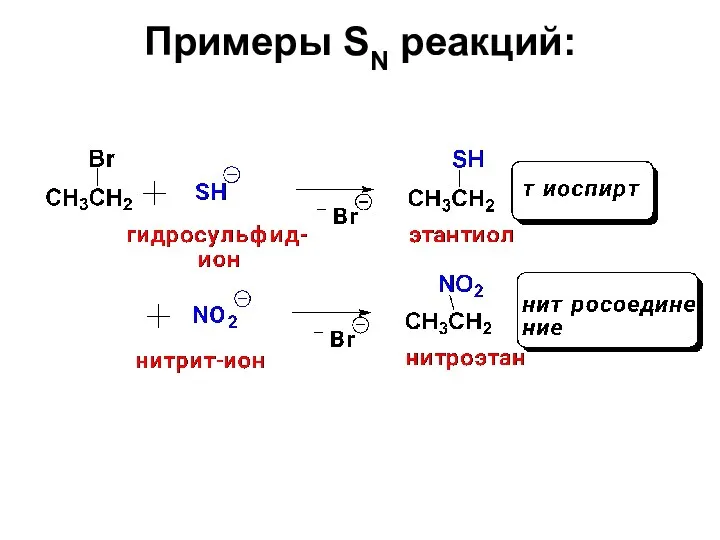
- 24. Примеры SN реакций:
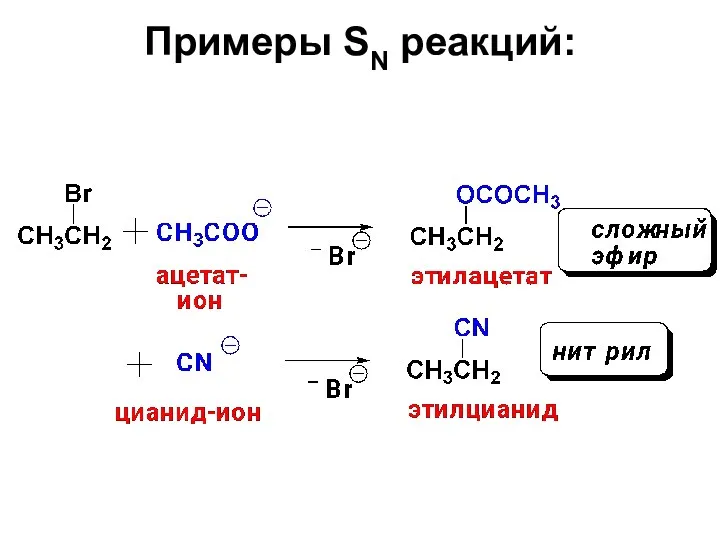
- 25. Примеры SN реакций:
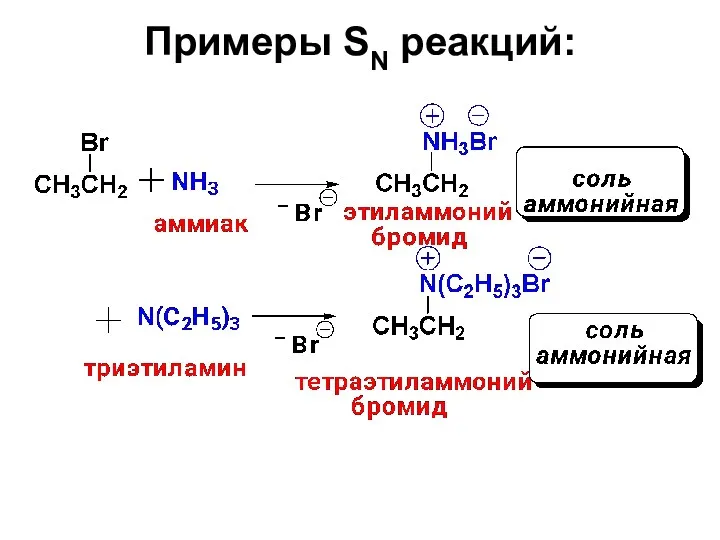
- 26. Примеры SN реакций:
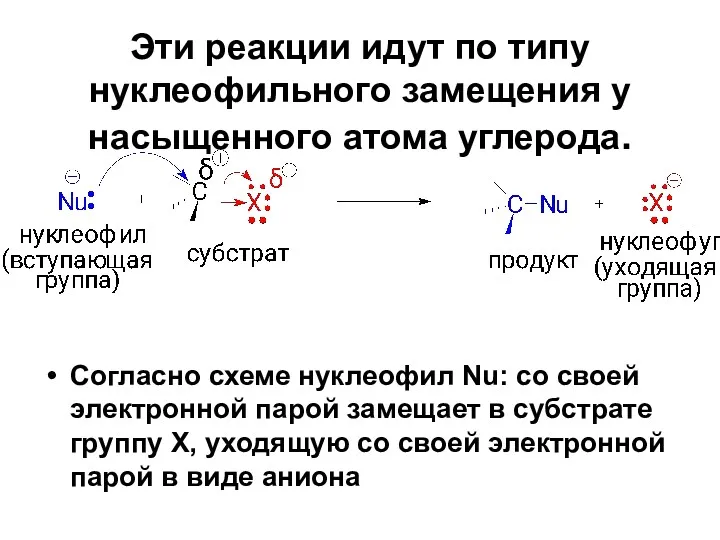
- 27. Эти реакции идут по типу нуклеофильного замещения у насыщенного атома углерода. Согласно схеме нуклеофил Nu: со
- 28. Нуклеофильные реагенты - это частицы (атомы или молекулы) доноры электронной пары при образовании связи с любым
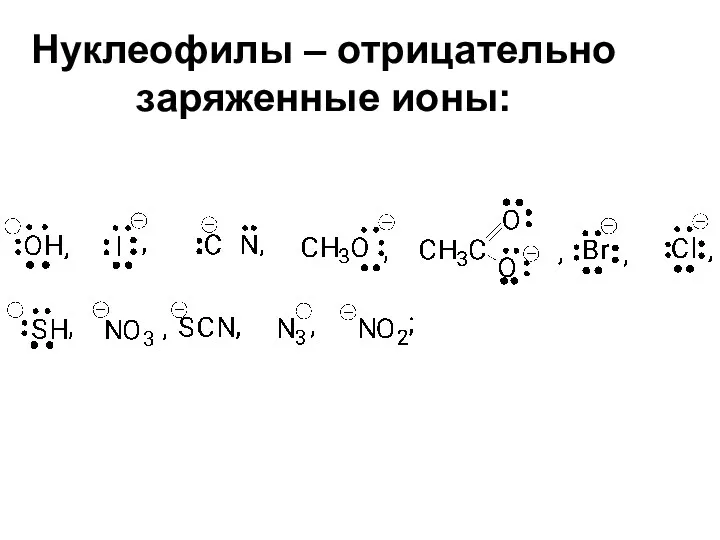
- 29. Нуклеофилы – отрицательно заряженные ионы:
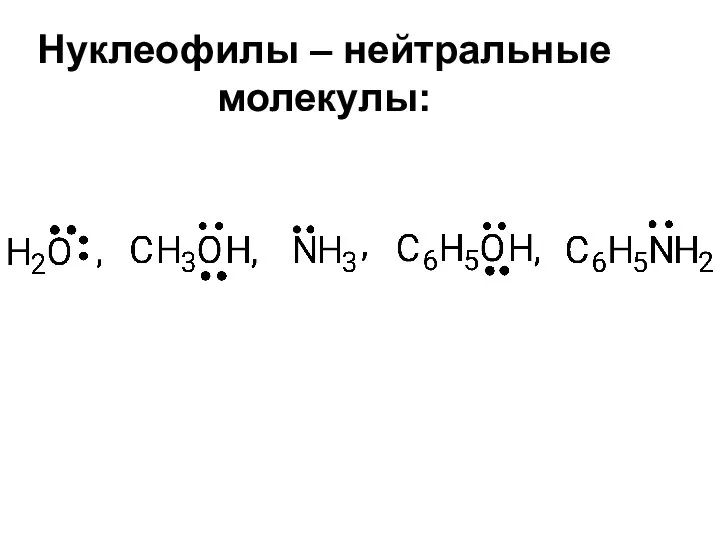
- 30. Нуклеофилы – нейтральные молекулы:
- 31. Реакции нуклеофильного замещения идут по одной из следующих схем: бимолекулярное нуклеофильное замещение (SN2); мономолекулярное нуклеофильное замещение
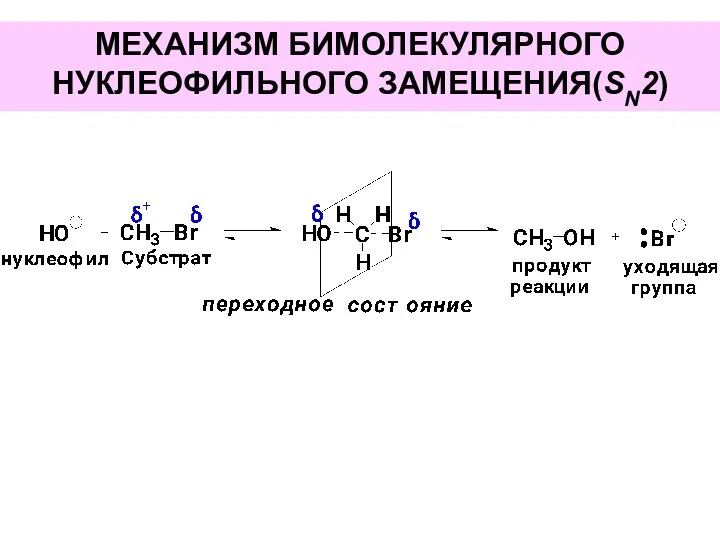
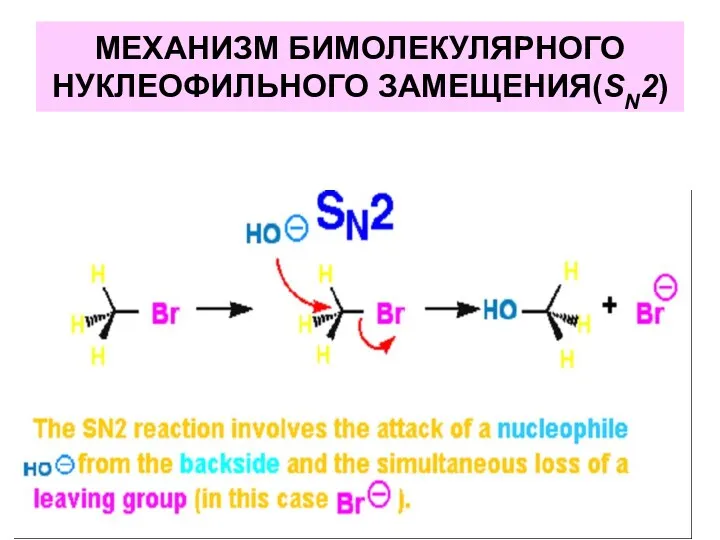
- 32. МЕХАНИЗМ БИМОЛЕКУЛЯРНОГО НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ(SN2)
- 33. МЕХАНИЗМ БИМОЛЕКУЛЯРНОГО НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ(SN2)
- 34. Кинетика реакции: V=k[субстрат] [реагент]
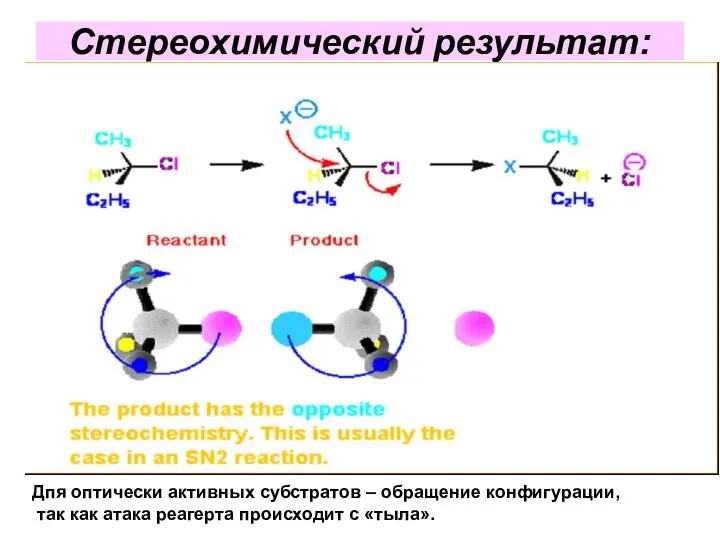
- 35. Стереохимический результат: Дпя оптически активных субстратов – обращение конфигурации, так как атака реагерта происходит с «тыла».
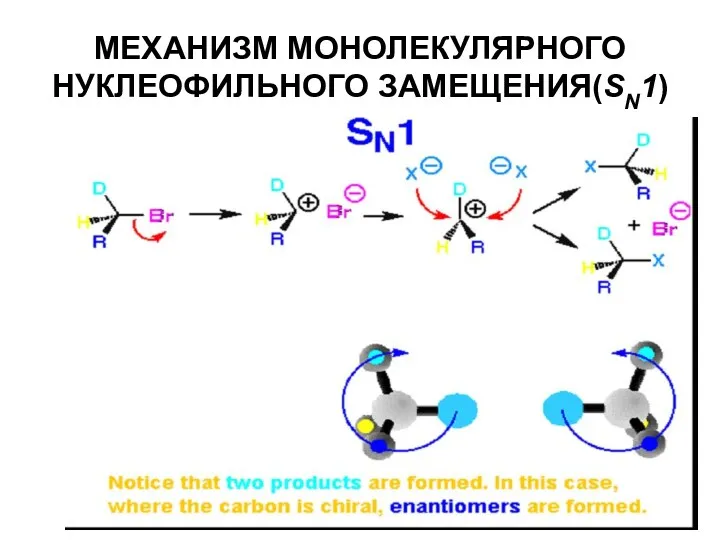
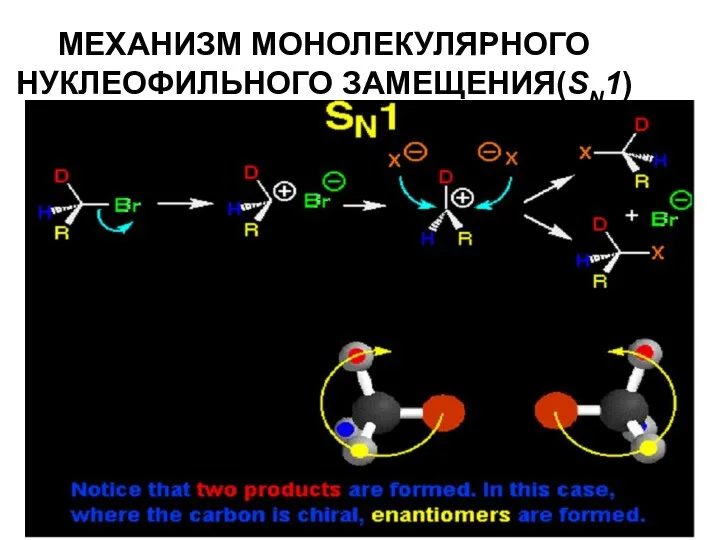
- 36. МЕХАНИЗМ МОНОЛЕКУЛЯРНОГО НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ(SN1)
- 37. МЕХАНИЗМ МОНОЛЕКУЛЯРНОГО НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ(SN1)
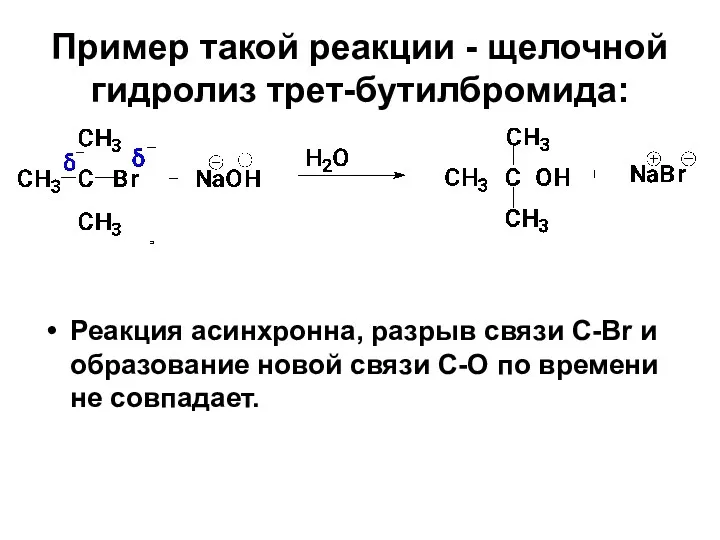
- 38. Пример такой реакции - щелочной гидролиз трет-бутилбромида: Реакция асинхронна, разрыв связи С-Br и образование новой связи
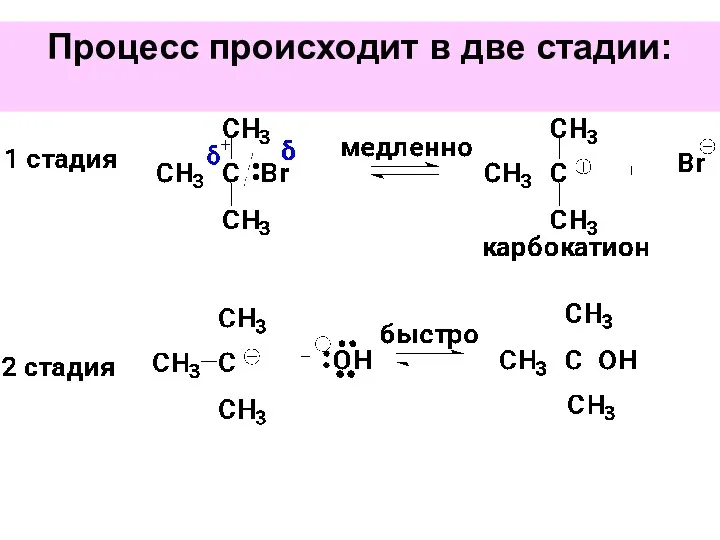
- 39. Процесс происходит в две стадии:
- 40. Кинетика реакции: V=k[субстрат] Концентрация нуклеофила на скорость реакции не влияет.
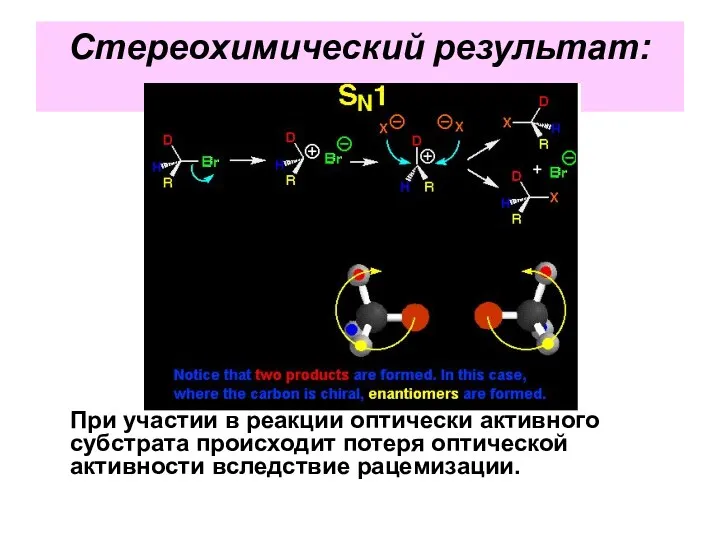
- 41. Стереохимический результат: При участии в реакции оптически активного субстрата происходит потеря оптической активности вследствие рацемизации.
- 42. Факторы,влияющие на ход нуклеофильного замещения 1. Строение субстрата. 2. Природа уходящей группы. 3. Природа растворителя. 4.
- 43. Строение субстрата. Природа углеводородного радикала, связанного с галогеном, играет важную роль. С точки зрения реакционной способности
- 44. а) Соединения с нормальной реакционной способностью (нормальной подвижностью галогена в SN реакциях); б) Соединения с пониженной
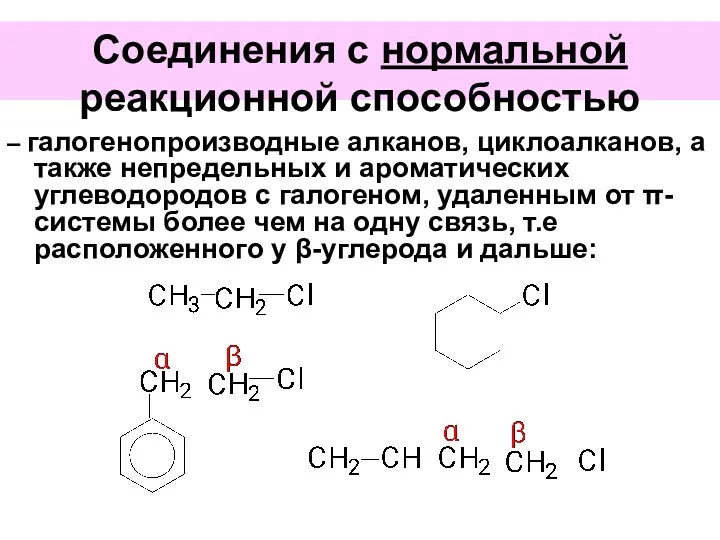
- 45. Соединения с нормальной реакционной способностью – галогенопроизводные алканов, циклоалканов, а также непредельных и ароматических углеводородов с
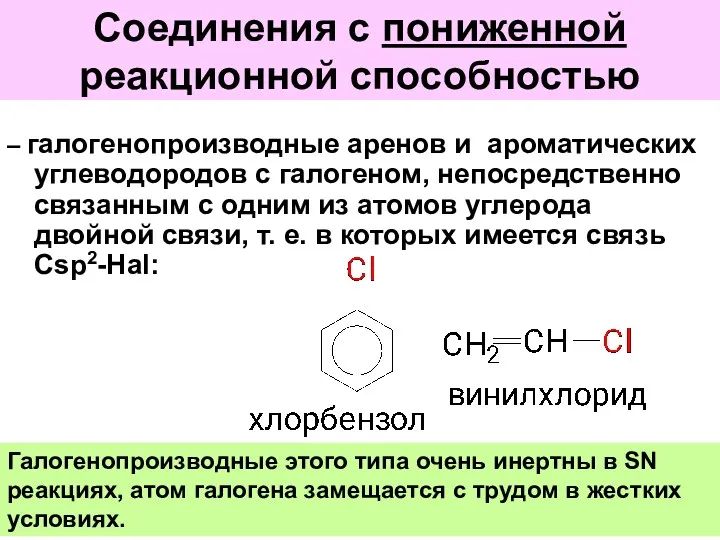
- 46. Соединения с пониженной реакционной способностью – галогенопроизводные аренов и ароматических углеводородов с галогеном, непосредственно связанным с
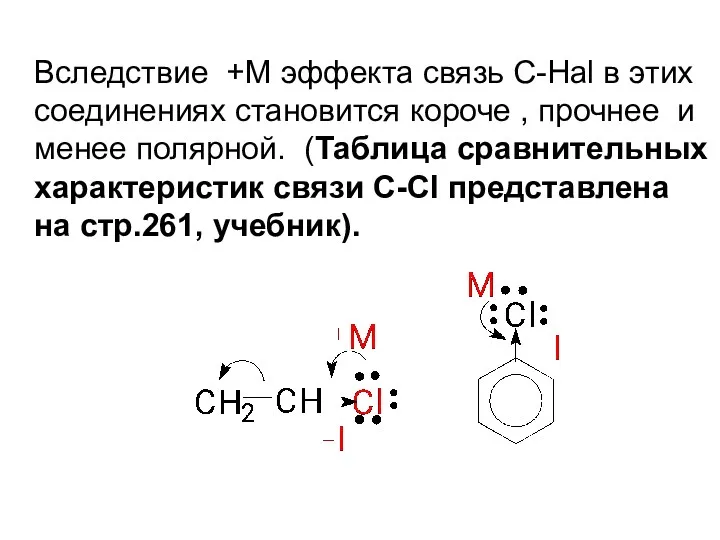
- 47. Вследствие +М эффекта связь С-Hal в этих соединениях становится короче , прочнее и менее полярной. (Таблица
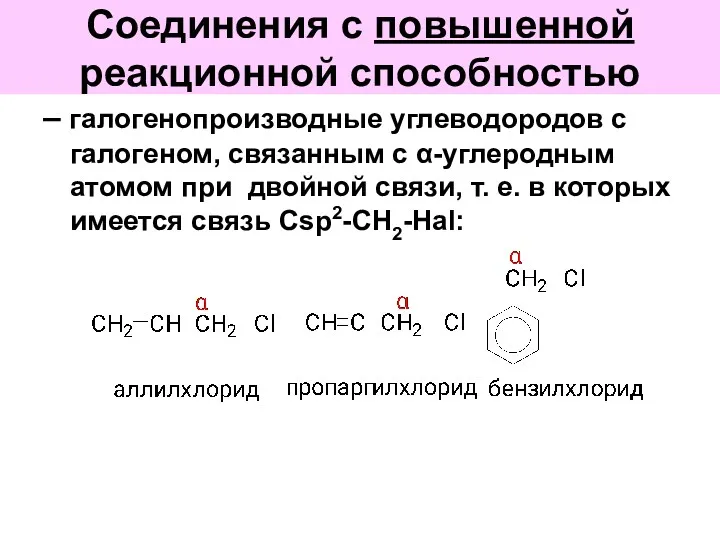
- 48. Соединения с повышенной реакционной способностью – галогенопроизводные углеводородов с галогеном, связанным с α-углеродным атомом при двойной
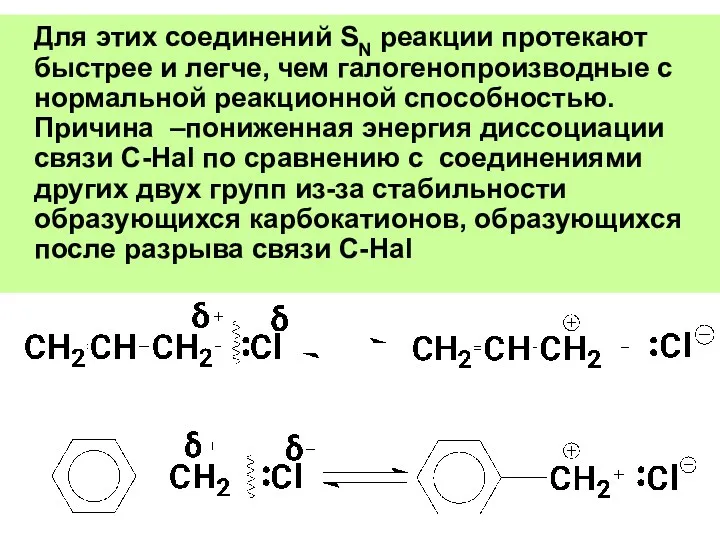
- 49. Для этих соединений SN реакции протекают быстрее и легче, чем галогенопроизводные с нормальной реакционной способностью. Причина
- 50. Природа R влияет и на предпочтительность реализации замещения по (SN1) или (SN2) механизмам. Склонность субстрата вступать
- 51. В случае SN2 реакции определяющим является стерический фактор: большие по объему R при атоме С уменьшают
- 52. SN1 Реакции могут протекать для тех субстратов, у которых связь С-Hal легко диссоциирует с образованием стабильного
- 53. Таким образом, третичные субстраты обычно вступают в SN1, а первичные – SN2-реакции. Субстраты вторичные, а также
- 54. Влияние природы уходящей группы (нуклеофуга) Хорошие уходящие группы бедны энергией, т.е. являются устойчивыми ионами или нейтральными
- 55. Влияние природы растворителя. Роль полярного растворителя: 1) принимает участие в ионизации молекул исходных веществ; 2) стабилизирует
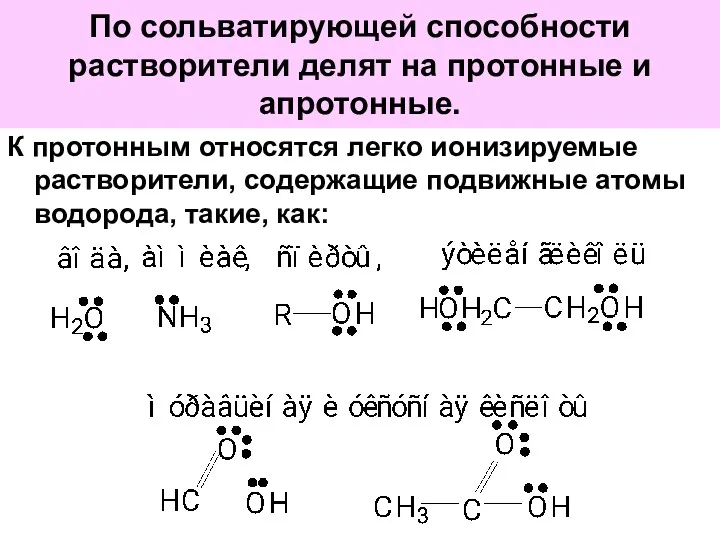
- 56. По сольватирующей способности растворители делят на протонные и апротонные. К протонным относятся легко ионизируемые растворители, содержащие
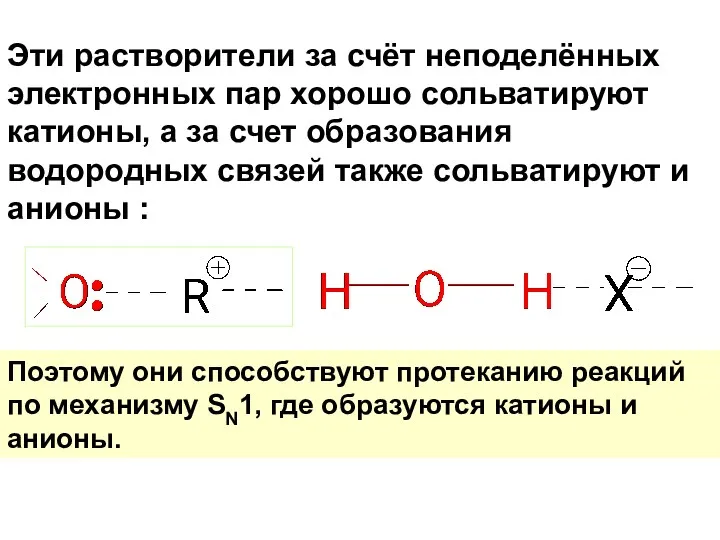
- 57. Эти растворители за счёт неподелённых электронных пар хорошо сольватируют катионы, а за счет образования водородных связей
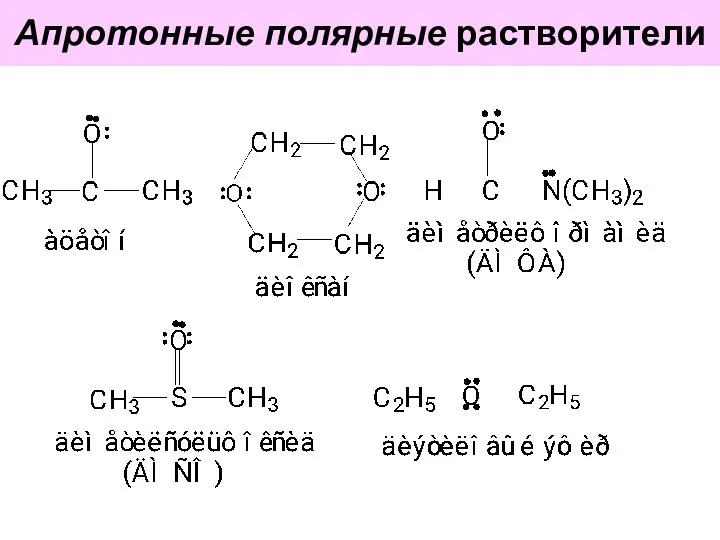
- 58. Апротонные полярные растворители
- 59. Апротонные полярные растворители за счёт неподелённых электронных пар гетероатомов хорошо сольватируют катионы. Анионы не сольватируют,т.к. они
- 60. Таким образом, характер растворителя оказывает существенное влияние на скорость реакций и её механизм. Это позволяет, подбирая
- 61. Влияние нуклеофильности реагента. Активность нуклеофила сказывается на скорости реакций типа SN2, поскольку он принимает участие в
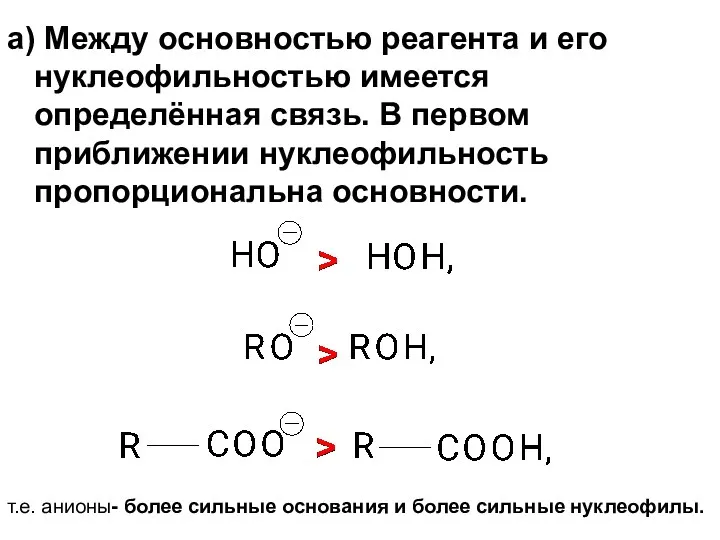
- 62. а) Между основностью реагента и его нуклеофильностью имеется определённая связь. В первом приближении нуклеофильность пропорциональна основности.
- 63. б) Нуклеофильность определяется ещё и поляризуемостью. Чем больше размер атома, тем выше его нуклеофильность. Легкополяризуемые реагенты
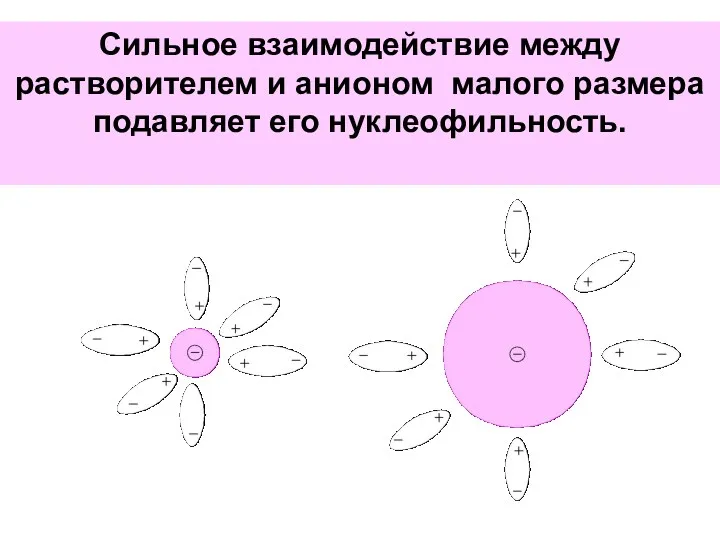
- 64. в) На нуклеофильность слабополяризуемых ионов значительное влияние оказывает природа растворителя. В полярных растворителях ионы находятся в
- 65. Сильное взаимодействие между растворителем и анионом малого размера подавляет его нуклеофильность.
- 66. Реагенты по возрастанию их нуклеофильности в SN2-реакциях в протонных растворителях можно расположить таким образом:
- 67. Апротонный растворитель не способен сольватировать анионы за счёт образования водородных связей с ними, поэтому анионы в
- 68. Порядок нуклеофильности в апротонном растворителе диметилформамиде (ДМФА) становится следующим: Таблица сравнения SN1- и SN2-реакций представлена на
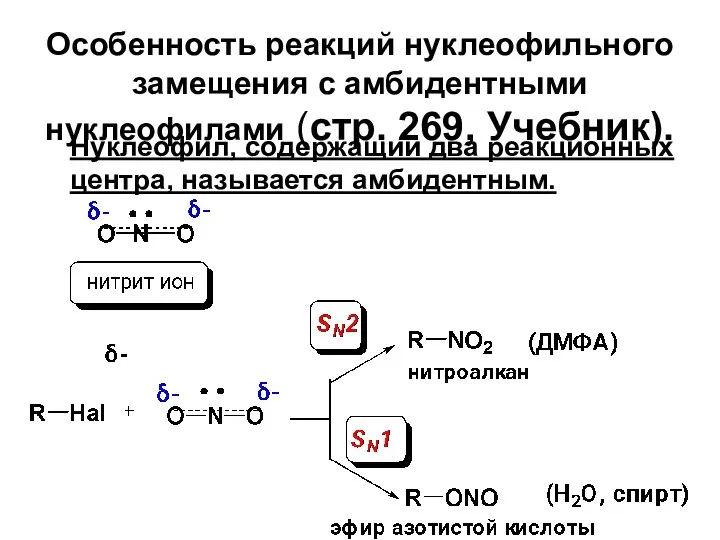
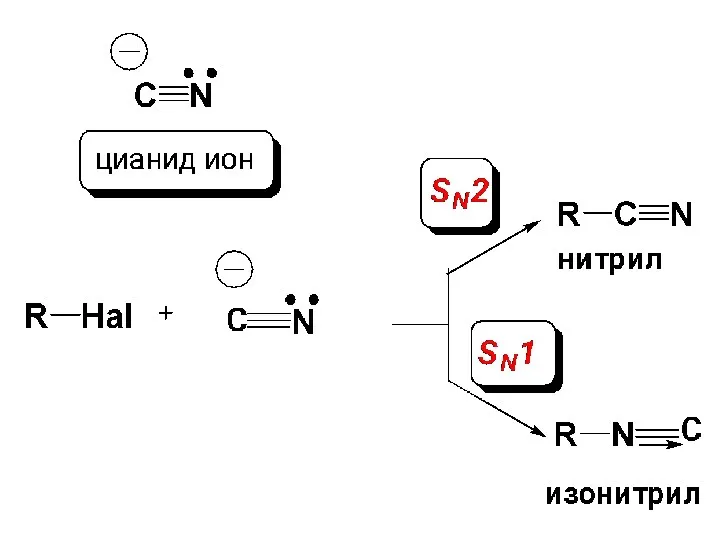
- 69. Особенность реакций нуклеофильного замещения с амбидентными нуклеофилами (стр. 269, Учебник). Нуклеофил, содержащий два реакционных центра, называется
- 71. Правило Корнблюма: В SN2-реакциях атакующим атомом амбидентного нуклеофила будет более нуклеофильный атом, а в SN1-реакциях –
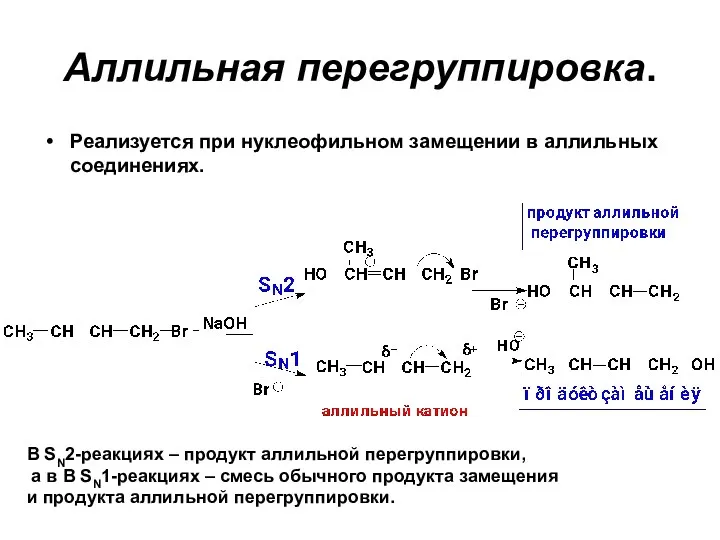
- 72. Аллильная перегруппировка. Реализуется при нуклеофильном замещении в аллильных соединениях. В SN2-реакциях – продукт аллильной перегруппировки, а
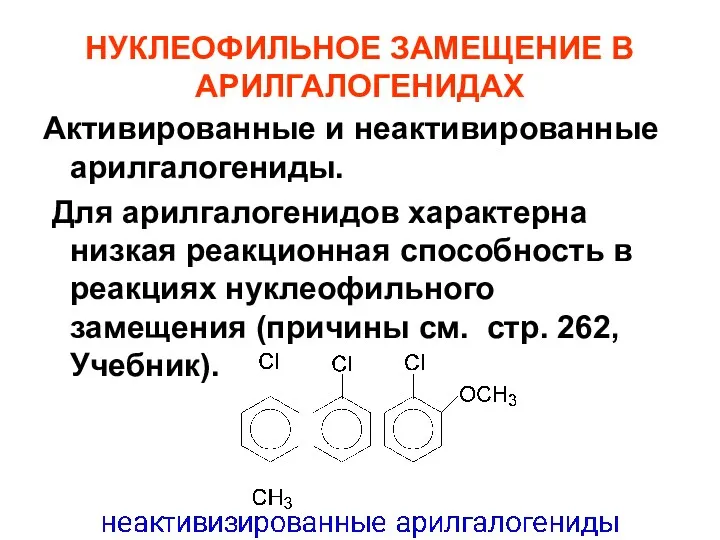
- 73. НУКЛЕОФИЛЬНОЕ ЗАМЕЩЕНИЕ В АРИЛГАЛОГЕНИДАХ Активированные и неактивированные арилгалогениды. Для арилгалогенидов характерна низкая реакционная способность в реакциях
- 74. Подвижность галогена можно увеличить введением в о- или п-положение сильных электроноакцепторных групп, обладающих –I- и –М-эффектами
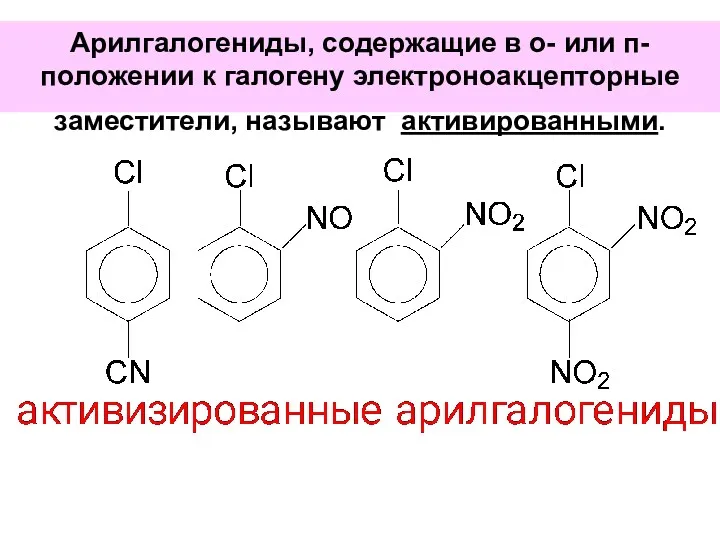
- 75. Арилгалогениды, содержащие в о- или п-положении к галогену электроноакцепторные заместители, называют активированными.
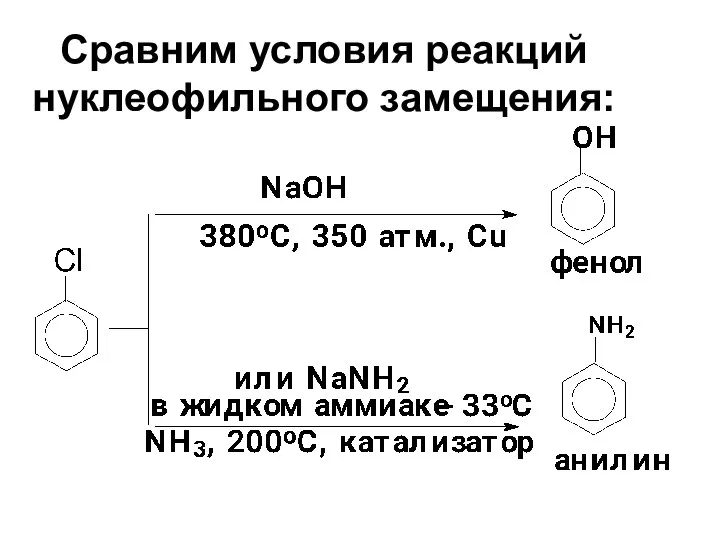
- 76. Сравним условия реакций нуклеофильного замещения:
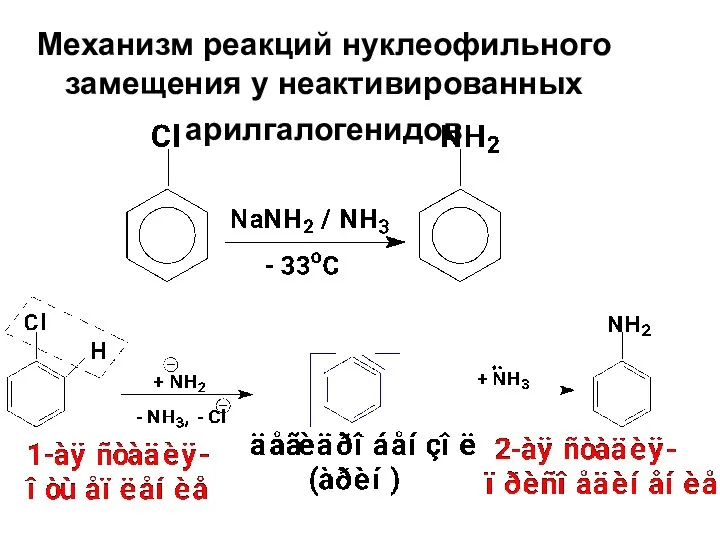
- 78. Механизм реакций нуклеофильного замещения у неактивированных арилгалогенидов
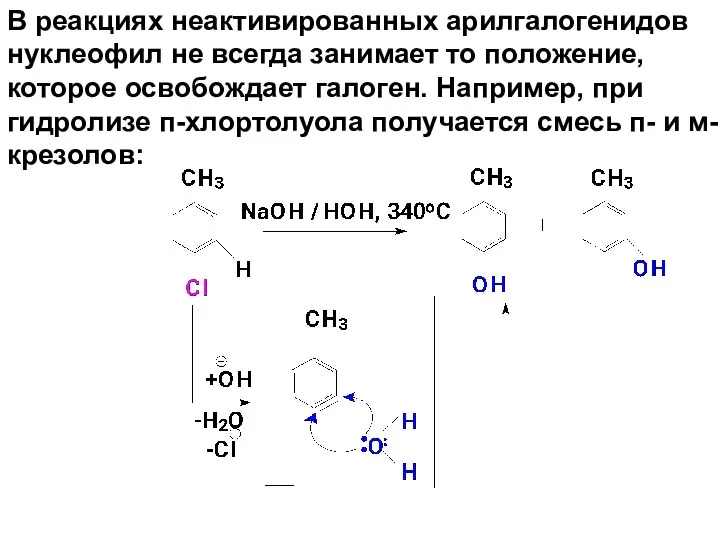
- 79. В реакциях неактивированных арилгалогенидов нуклеофил не всегда занимает то положение, которое освобождает галоген. Например, при гидролизе
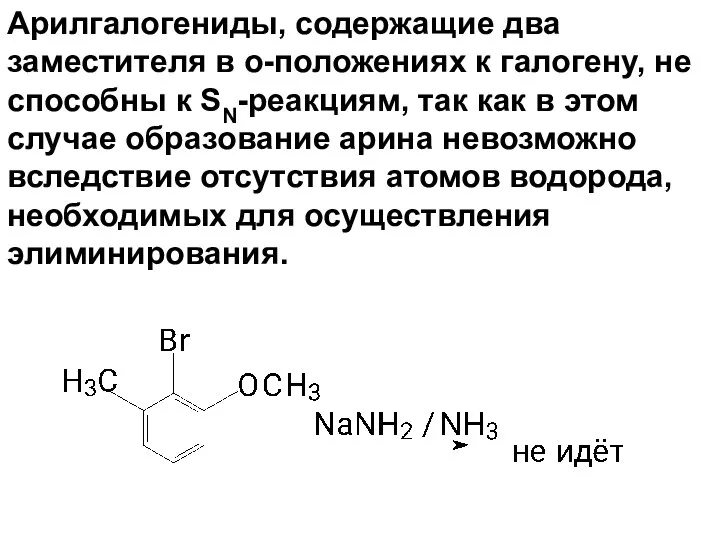
- 80. Арилгалогениды, содержащие два заместителя в о-положениях к галогену, не способны к SN-реакциям, так как в этом
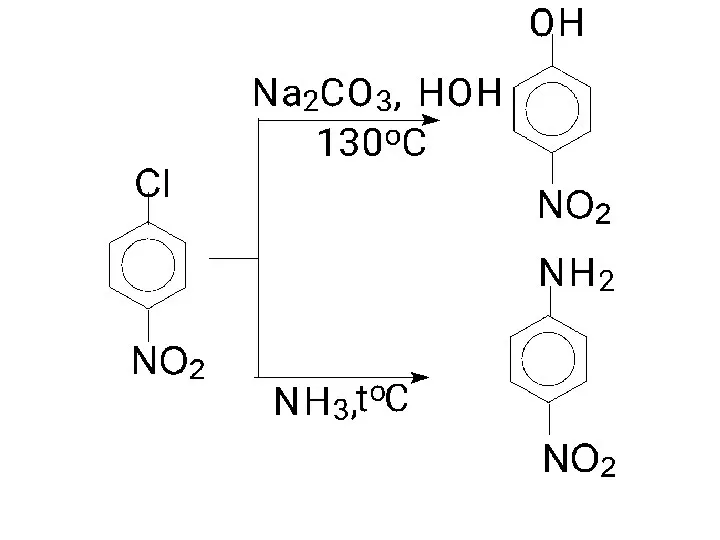
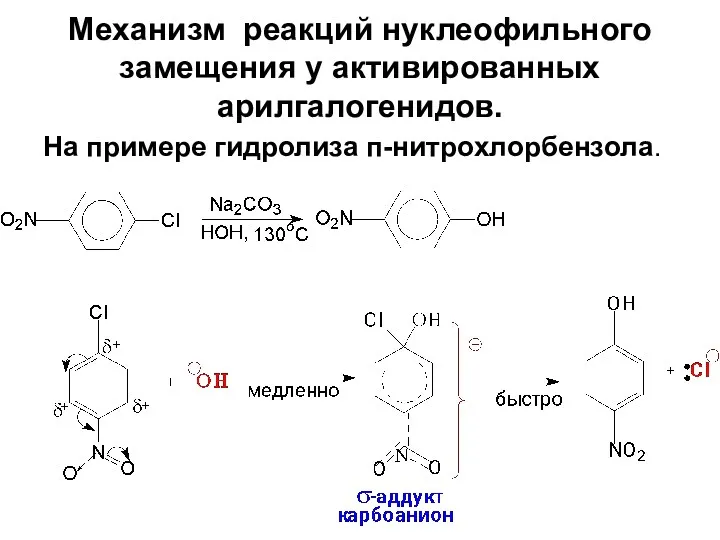
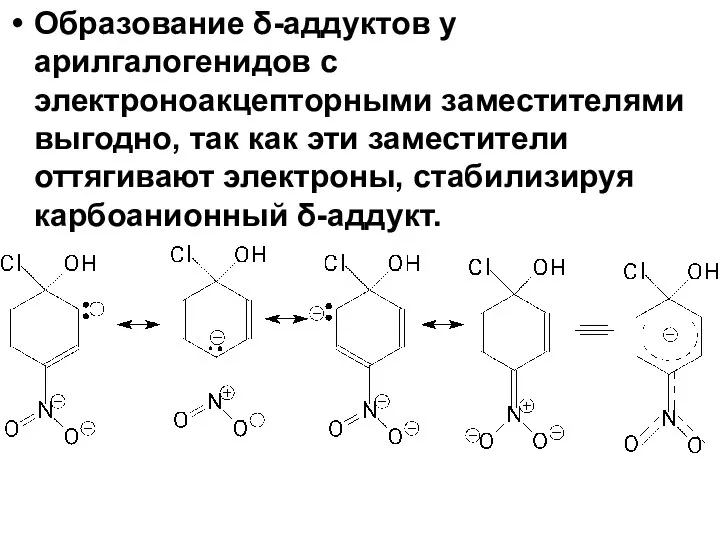
- 81. Механизм реакций нуклеофильного замещения у активированных арилгалогенидов. На примере гидролиза п-нитрохлорбензола.
- 82. Образование δ-аддуктов у арилгалогенидов с электроноакцепторными заместителями выгодно, так как эти заместители оттягивают электроны, стабилизируя карбоанионный
- 83. Т.к. в lim-стадии участвуют два вещества реакция по своему типу относится к SN2аром. Сравнение реакций SN2аром
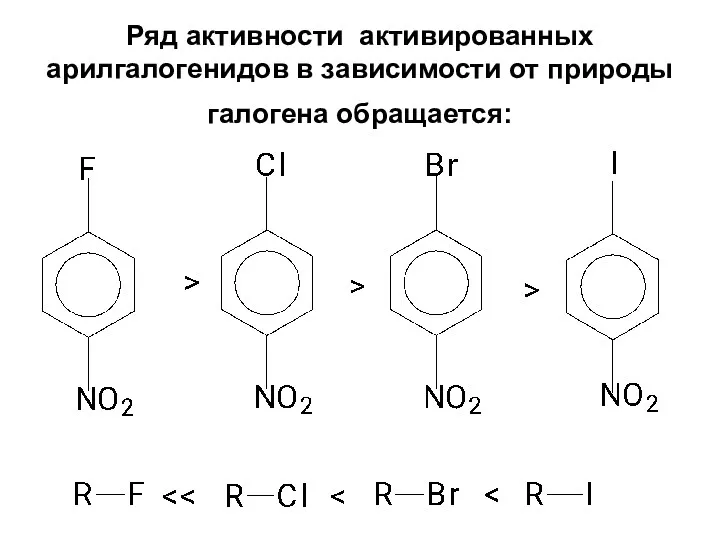
- 84. Ряд активности активированных арилгалогенидов в зависимости от природы галогена обращается:
- 85. 2. РЕАКЦИИ ЭЛИМИНИРОВАНИЯ Нуклеофильные реагенты являются также основаниями, способными отщеплять протон, поэтому SN сопровождается дегидрогалогенированием (элиминированием
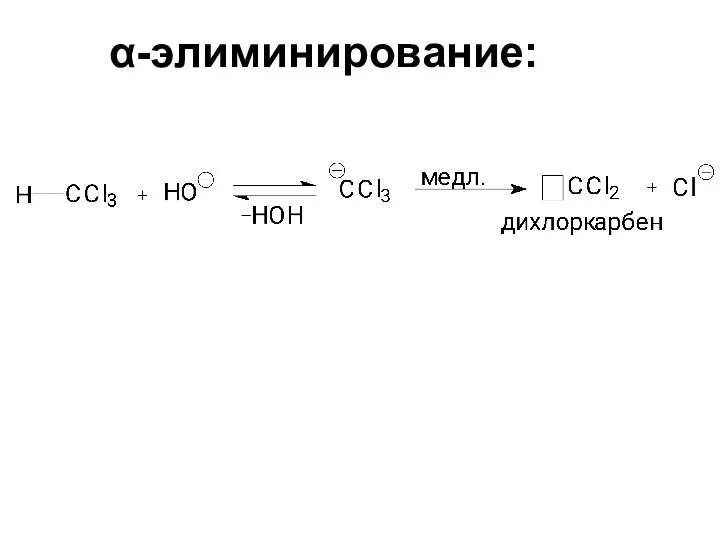
- 86. α-элиминирование:
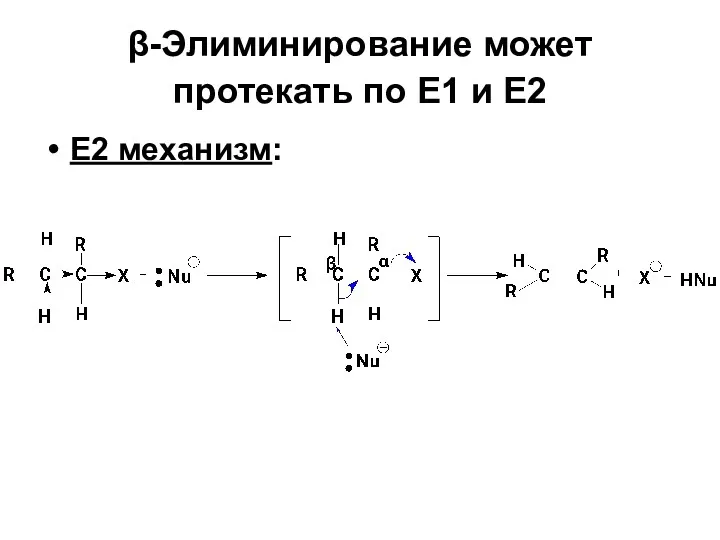
- 87. β-Элиминирование может протекать по Е1 и Е2 Е2 механизм:
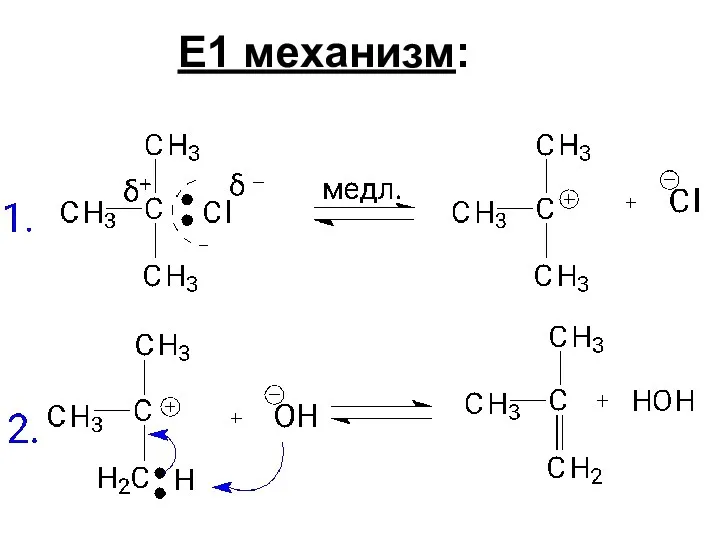
- 88. Е1 механизм:
- 89. Направление и стереохимия реакций элиминирования. в соответствии с правилом Зайцева: Правило Зайцева не соблюдается при наличии
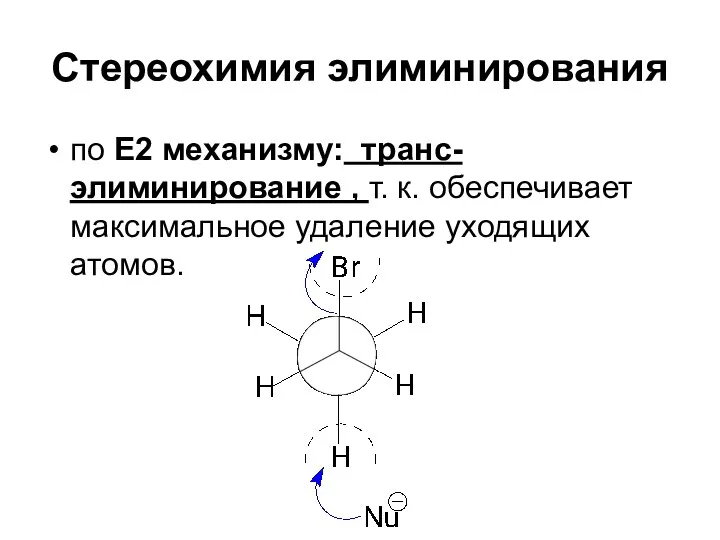
- 90. Стереохимия элиминирования по Е2 механизму: транс-элиминирование , т. к. обеспечивает максимальное удаление уходящих атомов.
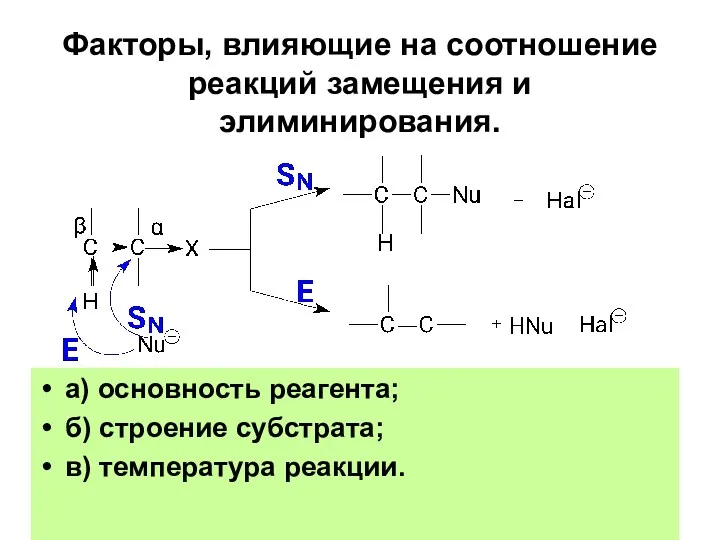
- 91. Факторы, влияющие на соотношение реакций замещения и элиминирования. а) основность реагента; б) строение субстрата; в) температура
- 92. а) Основность реагента как сродство к протону увеличивает вклад Е-реакций:
- 93. б) строение субстрата В зависимости от природ Hal при одинаковом R скорость отщепления изменяется в соответствии
- 94. в) температура реакции. Повышение температуры увеличивает вклад Е-реакций.
- 95. 3.РЕАКЦИИ ГАЛОГЕНПРОИЗВОДНЫХ С МЕТАЛЛАМИ Алкил- и арилгалогениды реагируют с металлами с образованием металлоорганических соединений. Происходит образование
- 96. Li образует ковалентную связь с угдеродом, в то время как Na-производные в основном ионные соединения. Они
- 97. При переходе от R-Ha1 к Li - и Na-органическим соединениям происходит обращение поляризации атома углерода от
- 98. Mg-органические галогениды –реактивы Гриньяра ( 1912 г. Нобелевская премия). Роль диэтилового эфира : 1) эфир растворяет
- 99. Реакции магнийорганических соединений. В реактивах Гриньяра связь достаточно полярна, что определяет карбанионный характер атома углерода ,
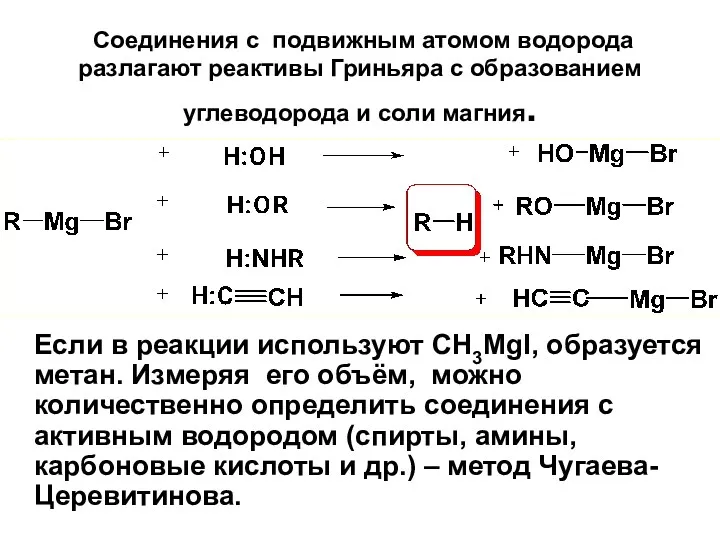
- 100. Соединения с подвижным атомом водорода разлагают реактивы Гриньяра с образованием углеводорода и соли магния. Если в
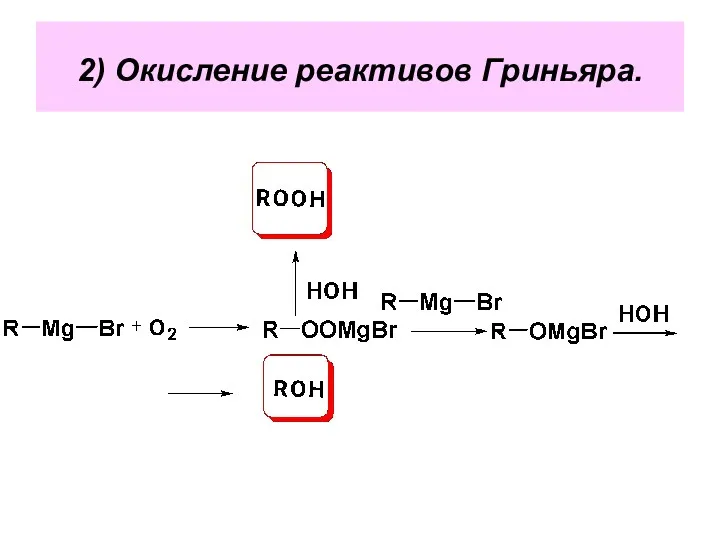
- 101. 2) Окисление реактивов Гриньяра.
- 103. Скачать презентацию











![Кинетика реакции: V=k[субстрат] [реагент]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/339612/slide-33.jpg)
![Кинетика реакции: V=k[субстрат] Концентрация нуклеофила на скорость реакции не влияет.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/339612/slide-39.jpg)






























 Алюминий. Строение и свойства атома
Алюминий. Строение и свойства атома Оксиды. Классификация и химические свойства
Оксиды. Классификация и химические свойства Каменный уголь. Фенол
Каменный уголь. Фенол Спирты. Состав, строение спиртов
Спирты. Состав, строение спиртов Методы обучения химии
Методы обучения химии Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Разноцветные кристаллы
Разноцветные кристаллы Простые вещества (урок для 8 класса)
Простые вещества (урок для 8 класса) Физико-химия дисперсных систем в функционировании живых систем
Физико-химия дисперсных систем в функционировании живых систем Массовая доля элемента в сложном веществе
Массовая доля элемента в сложном веществе Алкены. Гомологический ряд и изомерия
Алкены. Гомологический ряд и изомерия Приборы радиационной и химической разведки
Приборы радиационной и химической разведки Классификация химических реакций
Классификация химических реакций Химия и пища
Химия и пища Спирттер мен фенолдар
Спирттер мен фенолдар Растворимость, ее зависимость от разных факторов. Насыщенные и ненасыщенные растворы. Физико-химическая сущность растворения
Растворимость, ее зависимость от разных факторов. Насыщенные и ненасыщенные растворы. Физико-химическая сущность растворения Альтернативная бытовая химия
Альтернативная бытовая химия Кристаллография и основы кристаллохимии. Закон постоянства углов. Методы проецирования кристаллов. Лекция №6
Кристаллография и основы кристаллохимии. Закон постоянства углов. Методы проецирования кристаллов. Лекция №6 Побочная подгруппа. 8 группы
Побочная подгруппа. 8 группы Золото. История открытия
Золото. История открытия Химия элементов 16 (VIA) группы
Химия элементов 16 (VIA) группы Кристаллические решетки
Кристаллические решетки Азот. Нахождение азота в природе
Азот. Нахождение азота в природе Щелочные металлы
Щелочные металлы Изменения, происходящие с липидами в процессах технологической переработки сырья и параметры, характеризующие их
Изменения, происходящие с липидами в процессах технологической переработки сырья и параметры, характеризующие их Ртуть (Hydrargyrum, жидкое серебро)
Ртуть (Hydrargyrum, жидкое серебро) Простые вещества – неметаллы. Аллотропия
Простые вещества – неметаллы. Аллотропия Химическое кафе Кислоты
Химическое кафе Кислоты