Слайд 2

АЛКЕНЫ -
это ациклические углеводороды, содержащие в молекуле, помимо одинарных связей, одну
двойную связь между атомами углерода и соответствующие общей формуле CnH2n олефины
Слайд 3
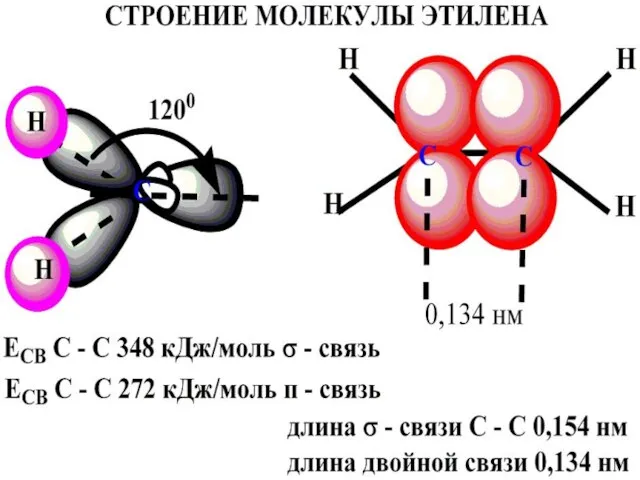
Слайд 4
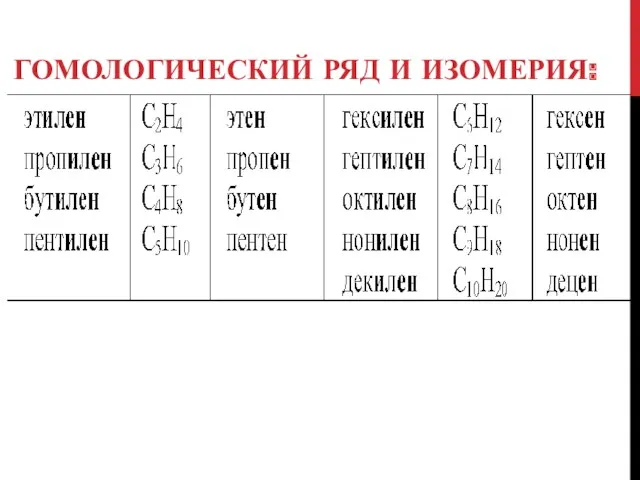
ГОМОЛОГИЧЕСКИЙ РЯД И ИЗОМЕРИЯ:
Слайд 5
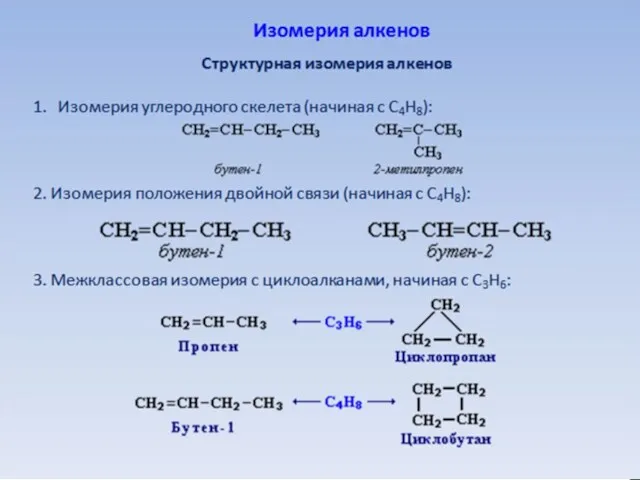
Слайд 6

ФИЗИЧЕСКИЕ СВОЙСТВА:
2-4 – газы (без цвета, вкуса, запаха)
5-16 – жидкости,
17 –
твердые вещества
t кипения и плавления увеличивается с увеличением цепи
Слайд 7

ХИМИЧЕСКИЕ СВОЙСТВА:
1. р-ция присоединения (электрофильное присоединения)
1) гидрирование (+Н, в присутствии Ni,
Pt, Pd) экзотермическая
СН3-СН2-СН=СН2+Н2→ СН3-СН2-СН2-СН3 (при повышение t идет обратная р-ия)
2) галогенирование (присоединение галогенов)
СН2=СН2+Br2→ СН2Br -СН2Br 1,2-дибромэтан
Слайд 8

3) гидрогалогенирование (прис. галогеноводорода)
СН3-СН=СН2+НBr→ СН3-СНBr-СН3
2-бромпропан
правила Марковникова
При присоединении галогенводорода
к алкену водород присоединяется к более гидрированному атому углерода, т. е. атому, при котором находится больше атомов водорода, а галоген – к менее гидрированному.
Слайд 9
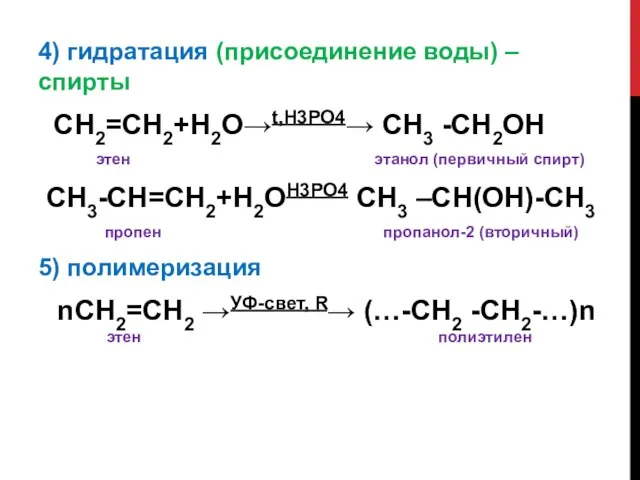
4) гидратация (присоединение воды) – спирты
СН2=СН2+Н2О→t,H3PO4→ СН3 -СН2OH
этен
этанол (первичный спирт)
СН3-СН=СН2+Н2ОH3PO4 СН3 –СН(ОН)-СН3
пропен пропанол-2 (вторичный)
5) полимеризация
nСН2=СН2 →УФ-свет, R→ (…-СН2 -СН2-…)n этен полиэтилен
Слайд 10

2. Реакция окисления
горят с образованием CO2 и H2O
СН2=СН2+3О2→ СО2 +2Н2O
Слайд 11
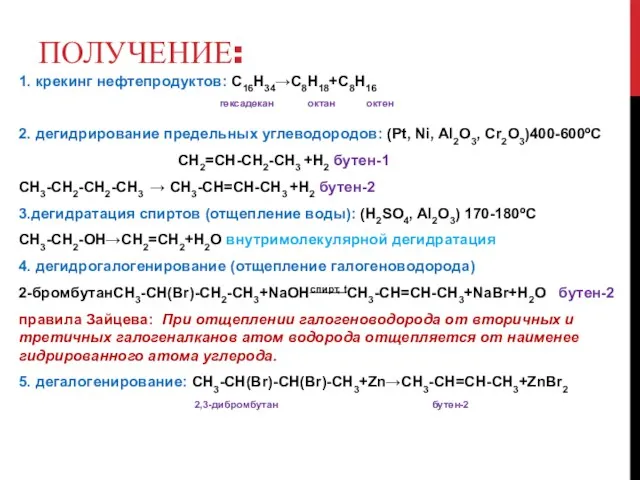
ПОЛУЧЕНИЕ:
1. крекинг нефтепродуктов: С16Н34→С8Н18+С8Н16
гексадекан октан октен
2. дегидрирование предельных углеводородов: (Pt,
Ni, Al2O3, Cr2O3)400-600ºC
СН2=СН-СН2-СН3 +Н2 бутен-1
СН3-СН2-СН2-СН3 → СН3-СН=СН-СН3 +Н2 бутен-2
3.дегидратация спиртов (отщепление воды): (H2SO4, Al2O3) 170-180ºC
СН3-СН2-ОН→СН2=СН2+Н2О внутримолекулярной дегидратация
4. дегидрогалогенирование (отщепление галогеноводорода)
2-бромбутанСН3-СН(Br)-СН2-СН3+NaOHспирт, tСН3-СН=СН-СН3+NaBr+Н2О бутен-2
правила Зайцева: При отщеплении галогеноводорода от вторичных и третичных галогеналканов атом водорода отщепляется от наименее гидрированного атома углерода.
5. дегалогенирование: СН3-СН(Br)-CH(Br)-CH3+Zn→CH3-CH=CH-CH3+ZnBr2
2,3-дибромбутан бутен-2










 Спирти. Історична довідка
Спирти. Історична довідка Вещества и их превращения Роль химии в нашей жизни
Вещества и их превращения Роль химии в нашей жизни Окисно-відновні реакції. Процеси окиснення, відновлення, окисник та відновник
Окисно-відновні реакції. Процеси окиснення, відновлення, окисник та відновник Кислоты. Серная кислота-H₂SO₄
Кислоты. Серная кислота-H₂SO₄ Виды и свойства текстильных материалов из химических волокон. 6 класс
Виды и свойства текстильных материалов из химических волокон. 6 класс Железо. Физические свойства
Железо. Физические свойства Молярна маса речовини
Молярна маса речовини Өсімдіктердегі су алмасу физиологиясы. Судың өсiмдiк тiршiлiгiндеri маңызы
Өсімдіктердегі су алмасу физиологиясы. Судың өсiмдiк тiршiлiгiндеri маңызы Карбоновые кислоты
Карбоновые кислоты Закон збереження маси речовини. Хімічні рівняння
Закон збереження маси речовини. Хімічні рівняння Амфотерные органические и неорганические соединения
Амфотерные органические и неорганические соединения Иондар және олардың түзілуі
Иондар және олардың түзілуі Бытовая химическая грамотность
Бытовая химическая грамотность Галогенопроизводные углеводородов 1
Галогенопроизводные углеводородов 1 Карбоновые кислоты. Классификация карбоновых кислот
Карбоновые кислоты. Классификация карбоновых кислот Реакции подлинности лекарственных веществ
Реакции подлинности лекарственных веществ Задание 5. Перегонка паром
Задание 5. Перегонка паром Топливный элемент: проблемы и перспективы
Топливный элемент: проблемы и перспективы Химия. Викторина
Химия. Викторина Химия в повседневной жизни человека
Химия в повседневной жизни человека Тепловой эффект химических реакций
Тепловой эффект химических реакций Основания, их классификация и свойства
Основания, их классификация и свойства Натуральные, искуственные и синтетические материалы
Натуральные, искуственные и синтетические материалы Азотсодержащие органические соединения. Аминокислоты (часть 2)
Азотсодержащие органические соединения. Аминокислоты (часть 2) Периодический закон и периодический закон Д.И. Менделеева
Периодический закон и периодический закон Д.И. Менделеева Phosphorus
Phosphorus Кислотність твердих тіл. Основні методи дослідження. Суперкислотність
Кислотність твердих тіл. Основні методи дослідження. Суперкислотність Задачи по химии
Задачи по химии