Слайд 2

АКТУАЛІЗАЦІЯ ОПОРНИХ ЗНАНЬ
Хімічний диктант
Записати рівняння реакцій, вказати їх типи.
1 варіант 2 варіант
1.
SO3 + H2O? 1. SO2 + H2O ?
2. Fe + HCl ? 2. Al + HCl?
3. N2O5 + H2O? 3. P2O5 + H2O?
4. CaO + HCl? 4. MgO + HCl?
5. FeO + H2SO4? 5. CaO + H2O?
6. Cu + H2SO4? 6. Na2O + H2SO4?
7. CO2 + H2O? 7. Hg + H2SO4?
8. KOH + H2SO4? 8. Cu(OH)2 + HCl?
9. Fe(OH)3? 9. H2CO3?
10. Fe + CuSO4? 10. Zn + HgCl2?
Слайд 3

ОКИСНО-ВІДНОВНІ РЕАКЦІЇ, ЇХ ЗНАЧЕННЯ
На сьогоднішньому уроці перед вами стоять завдання:
з’ясувати роль
окисно-відновних реакцій у природі, техніці, житті людини;
удосконалити вміння визначати ступені окиснення, записувати схеми процесів окиснення та відновлення, підбирати коефіцієнти методом електронного балансу.
Слайд 4

Запишемо рівняння реакції
Fe 0+Cu+2 SO4 = Fe +2 SO4 + Сu0
Слайд 5

Fe 0+Cu+2 SO4 = Fe +2 SO4 + Сu0
Відновник Fe0 -
2e = Fe+2
Окисник Cu+2 + 2e = Cu0
Слайд 6

Основні поняття
Окиснення — це процес віддачі електрона.
Відновлення — процес прийому
електрона.
Атом, що віддає електрони, називається відновником.
Атом, що приймає електрони, називається окисником.
Слайд 7

АЛГОРИТМ СКЛАДАННЯ ЕЛЕКТРОННОГО БАЛАНСУ
Визначити, які елементи в процесі хімічної реакції
змінюють ступінь окиснення.
Записати окремо процеси окиснення та відновлення з указівкою кількості електронів, що беруть участь у кожнім процесі.
У записаному рівнянні реакції визначити ступені окиснення всіх елементів.
Визначити окисник і відновник.
Визначити коефіцієнти, на які необхідно помножити рівняння окиснення й відновлення, щоб кількість електронів, відданих відновником і прийнятих окисником, була однаковою.
Просумувати рівняння окиснення й відновлення з урахуванням отриманих коефіцієнтів або розставити відповідні коефіцієнти у вихідному рівнянні.
Слайд 8

Оформлення окисно-відновної реакції з електронним балансом
Слайд 9

Окисно-відновні реакції в природі та житті людини:
- процеси дихання у тварин
-
процес фотосинтезу у рослин
- процес дихання у людини
- металургія
- електроніка
- електротехніка
- енергетика
- косметологія








 Алкадиены. Непредельные углеводороды
Алкадиены. Непредельные углеводороды Классификация моторных масел
Классификация моторных масел Получение водорода. Проверка Н2 на чистоту. Практическая работа
Получение водорода. Проверка Н2 на чистоту. Практическая работа Симметрия в химии
Симметрия в химии Использование потенциостата-гальваностата Elins p-20x в электрохимических исследованиях
Использование потенциостата-гальваностата Elins p-20x в электрохимических исследованиях Переработка газа. Первичная переработка нефти. Лекция 9
Переработка газа. Первичная переработка нефти. Лекция 9 Титан және оның қорытпалары. Титаннан жасалған құралдар
Титан және оның қорытпалары. Титаннан жасалған құралдар Коллигативные свойства растворов
Коллигативные свойства растворов Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Распространение пламени в газах
Распространение пламени в газах Молекулярно-кінетичні явища в дисперсних системах
Молекулярно-кінетичні явища в дисперсних системах Элементы химической термодинамики. 1 и 2 законы термодинамики. Химическое равновесие
Элементы химической термодинамики. 1 и 2 законы термодинамики. Химическое равновесие Роль хімії у житті суспільства
Роль хімії у житті суспільства Химическая связь
Химическая связь Карбоновые кислоты. (Лекция 6.3)
Карбоновые кислоты. (Лекция 6.3) Кристаллы и минералы
Кристаллы и минералы Получение полимеров из низкомолекулярных соединений
Получение полимеров из низкомолекулярных соединений Неон. Физические свойства
Неон. Физические свойства XXI ғасыр көшбасшысы
XXI ғасыр көшбасшысы Электрохимические процессы. Лекция 7
Электрохимические процессы. Лекция 7 Закономерности управления каталитическими процессами
Закономерности управления каталитическими процессами Кислород и его применение
Кислород и его применение Материаловедение. Контрольная работа
Материаловедение. Контрольная работа Умные полимеры в биотехнологии и медицине
Умные полимеры в биотехнологии и медицине Аммиак. 9 класс
Аммиак. 9 класс Гидролиз органических и неорганических соединений
Гидролиз органических и неорганических соединений Оксиды
Оксиды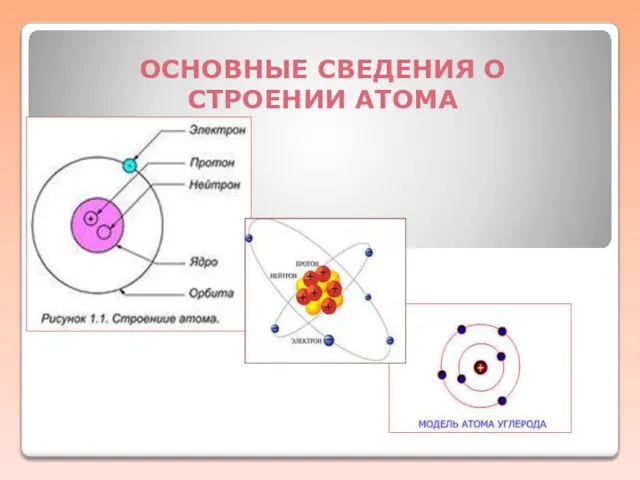 Основные сведения о строении атома
Основные сведения о строении атома