Содержание
- 2. Водородный автомобиль 2001 г. Автомобиль «Нива» (Россия) на топливном элементе, разработанном для космического корабля «Буран» 2001
- 3. Цель и средства программа бюджетных инвестиций США предполагает в ближайшие 10 лет вложить 5.5 млрд. долл.
- 4. 1973 год: нефтяное эмбарго
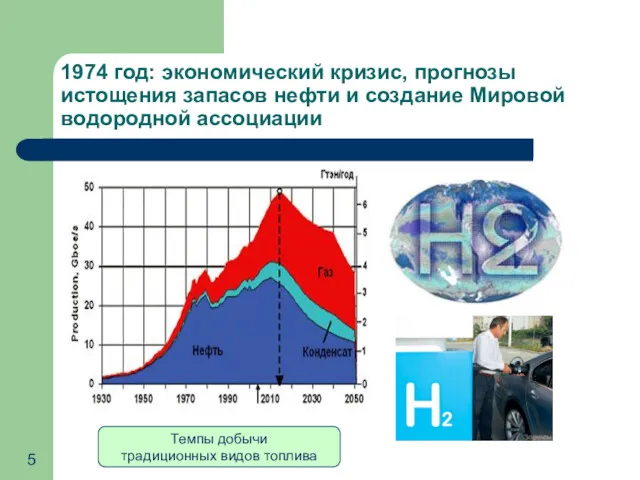
- 5. 1974 год: экономический кризис, прогнозы истощения запасов нефти и создание Мировой водородной ассоциации Темпы добычи традиционных
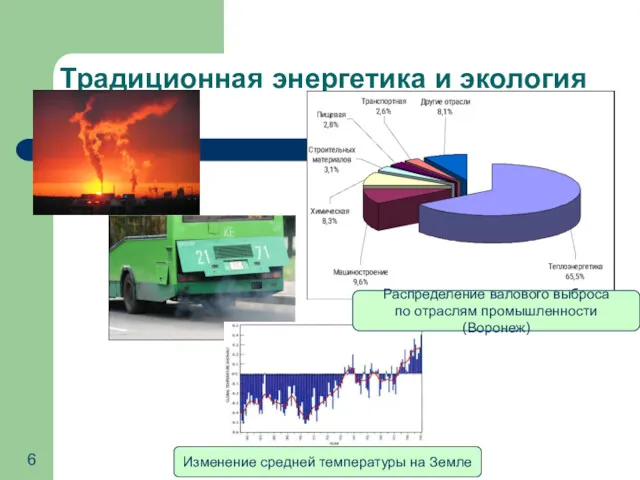
- 6. Традиционная энергетика и экология Распределение валового выброса по отраслям промышленности (Воронеж) Изменение средней температуры на Земле
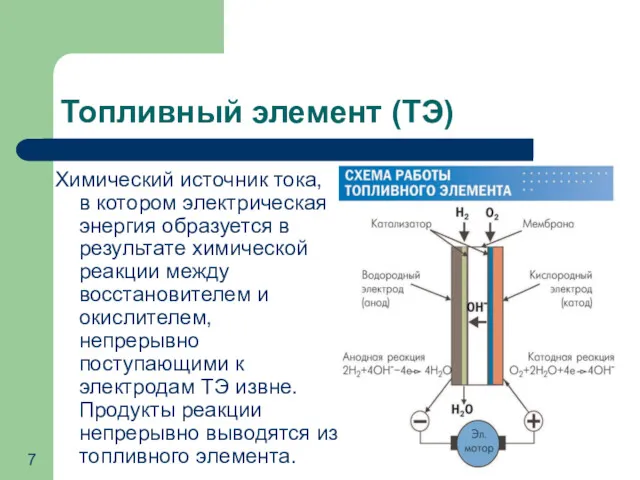
- 7. Топливный элемент (ТЭ) Химический источник тока, в котором электрическая энергия образуется в результате химической реакции между
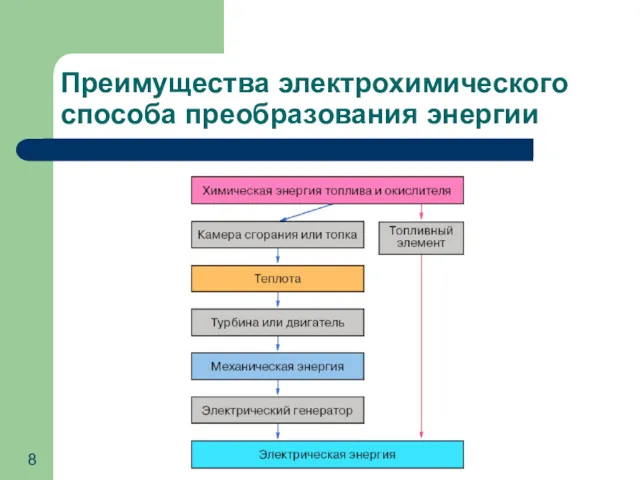
- 8. Преимущества электрохимического способа преобразования энергии
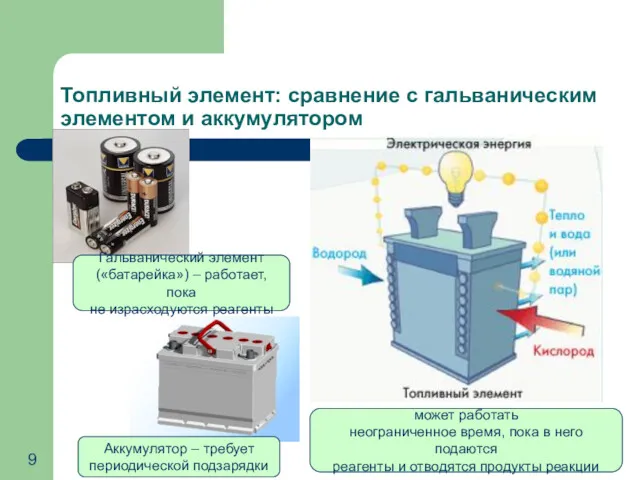
- 9. Топливный элемент: сравнение с гальваническим элементом и аккумулятором Гальванический элемент («батарейка») – работает, пока не израсходуются
- 10. Открытие топливного элемента Вильям Гроув (1811 – 1896) Людвиг Монд (1839 – 1909) Вильгельм Оствальд (1853-1932)
- 11. Водород – идеальное топливо для ТЭ химически активный экологически чистый – при его окислении образуется вода
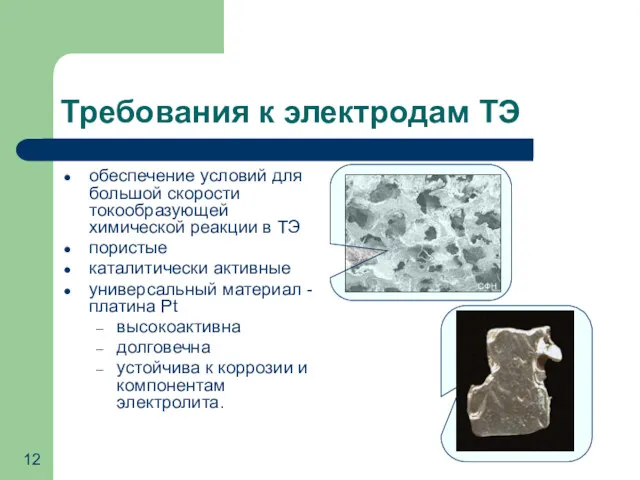
- 12. Требования к электродам ТЭ обеспечение условий для большой скорости токообразующей химической реакции в ТЭ пористые каталитически
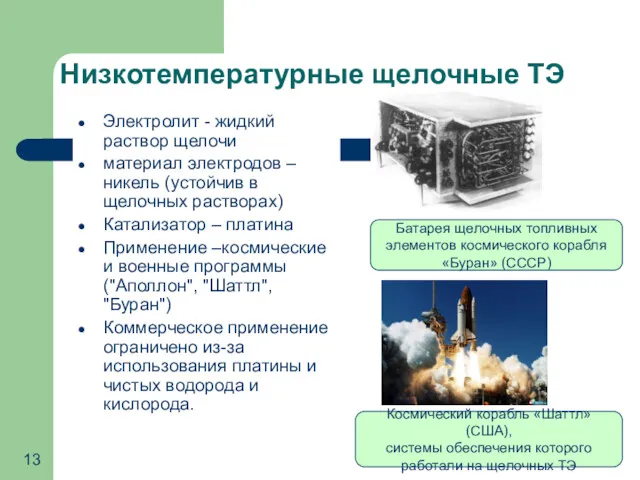
- 13. Низкотемпературные щелочные ТЭ Электролит - жидкий раствор щелочи материал электродов – никель (устойчив в щелочных растворах)
- 14. Низкотемпературные кислотные ТЭ Электролит - жидкий раствор кислоты Материал электродов – графит (устойчив в кислотных растворах)
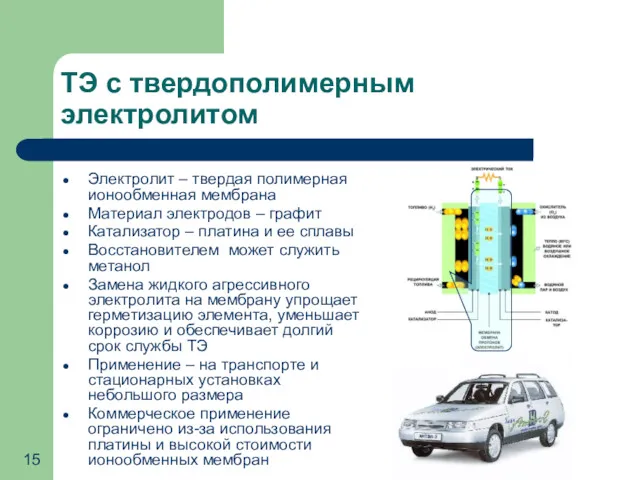
- 15. ТЭ с твердополимерным электролитом Электролит – твердая полимерная ионообменная мембрана Материал электродов – графит Катализатор –
- 16. Недостатки платиновых катализаторов высокая стоимость дефицит природных запасов платины платиновые электроды резко снижают свою активность ("отравляются")
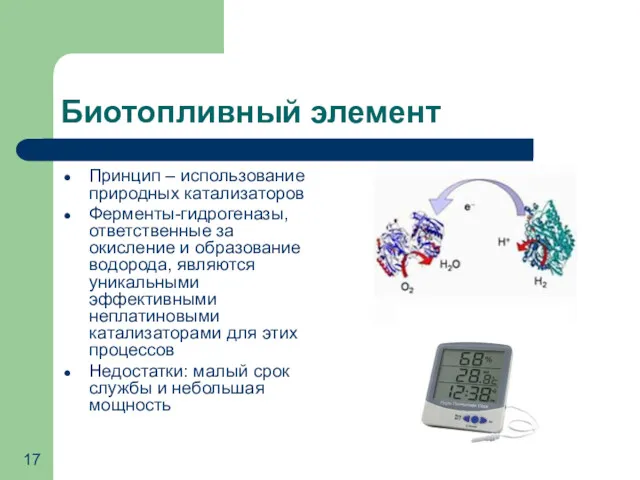
- 17. Биотопливный элемент Принцип – использование природных катализаторов Ферменты-гидрогеназы, ответственные за окисление и образование водорода, являются уникальными
- 18. Высокотемпературные ТЭ: ускорение реакций на электродах при значительном повышении температуры Тип 1 электролит - из расплава
- 19. Преимущества топливных элементов высокий коэффициент полезного действия экологическая чистота бесшумность широкий диапазон мощностей и применяемого топлива
- 20. Проблемы коммерциализации ТЭ высокая стоимость по сравнению с традиционными установками недостаточный срок службы
- 22. Скачать презентацию










 Типы химических реакций
Типы химических реакций Закон сохранения массы веществ
Закон сохранения массы веществ Современная химия. (Лекция 6)
Современная химия. (Лекция 6) Зиянды организмдерге қарсы органикалық және органикалық емес қосылыстарды қолдануға негізделген тәсіл
Зиянды организмдерге қарсы органикалық және органикалық емес қосылыстарды қолдануға негізделген тәсіл Кристаллические решетки
Кристаллические решетки Аналитические химические реакции. Классификация аналитических химических реакций
Аналитические химические реакции. Классификация аналитических химических реакций Материаловедение и технологии конструкционных материалов
Материаловедение и технологии конструкционных материалов Хімічний склад жувальної гумки
Хімічний склад жувальної гумки Мыльное чудо своими руками. История мыловарения. Изготовление мыла в домашних условиях
Мыльное чудо своими руками. История мыловарения. Изготовление мыла в домашних условиях Элементы триады железа: Fe, Co, Ni. (Лекция 16)
Элементы триады железа: Fe, Co, Ni. (Лекция 16) Техника безопасности в химической лаборатории и на уроках химии
Техника безопасности в химической лаборатории и на уроках химии Моющие средства
Моющие средства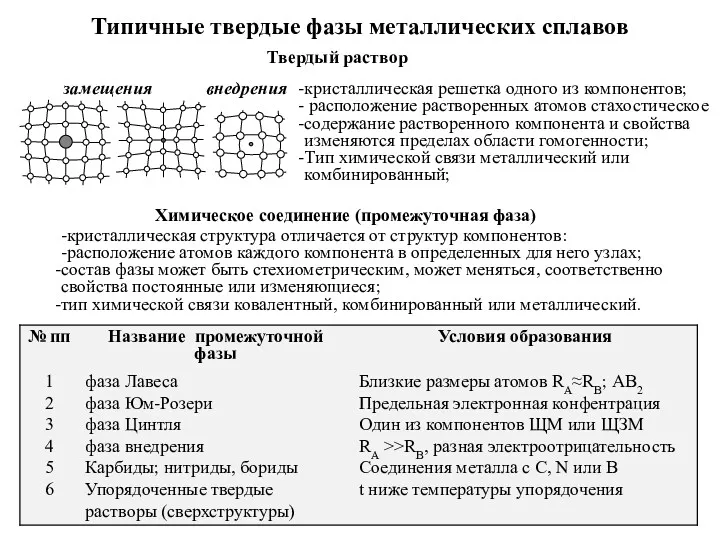 Типичные твердые фазы металлических сплавов
Типичные твердые фазы металлических сплавов Гигиена питания школьников
Гигиена питания школьников Классификация химических реакций
Классификация химических реакций Геохимия литосферы
Геохимия литосферы Гомополисахариды (углеводы растений)
Гомополисахариды (углеводы растений) Простые вещества. Металлы и неметаллы
Простые вещества. Металлы и неметаллы Полифенолды қосылыстар. Флавоноидтар
Полифенолды қосылыстар. Флавоноидтар Физико-химические свойства белков. Количественные (колориметрические) методы определения концентрации белка
Физико-химические свойства белков. Количественные (колориметрические) методы определения концентрации белка Гидролиз солей
Гидролиз солей Необоротні і оборотні хімічні процеси. Хімічна рівновага. Принцип Ле Шательє
Необоротні і оборотні хімічні процеси. Хімічна рівновага. Принцип Ле Шательє Введение. Развитие химической технологии как науки
Введение. Развитие химической технологии как науки Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Щелочные металлы IА группы. Литий
Щелочные металлы IА группы. Литий Окисно-відновні реакції. 9 клас
Окисно-відновні реакції. 9 клас Пластмассы, синтетические каучуки
Пластмассы, синтетические каучуки Роль химии в создании новых материалов
Роль химии в создании новых материалов