Слайд 2 118 ЭЛЕМЕНТОВ.
96 – МЕТАЛЛОВ. 16 НЕМЕТАЛЛОВ, 8 ИНЕРТНЫХ ГАЗОВ.
Что такое инертные(благородные) газы?
Слайд 3СОСТАВИТЬ СХЕМУ СТРОЕНИЯ И ЗАПИСАТЬ ЭЛЕКТРОННУЮ ФОРМУЛУ СЛЕДУЮЩИХ АТОМОВ:
K, Ca, P, Cl
Слайд 4ОСОБЕННОСТИ СТРОЕНИЯ АТОМОВ МЕТАЛЛОВ
От 1 до 3 электронов на внешнем энергоуровне атома
Радиус атомов
в периоде уменьшается слева направо. Металлы стоят вначале периода.
В главной подгруппе радиус увеличивается сверху вниз.
Связь между атомами в простых веществах металлическая химическая
Слайд 5ОСОБЕННОСТИ СТРОЕНИЯ АТОМОВ НЕМЕТАЛЛОВ
От 4 до 8 электронов на внешнем энергоуровне атома
Радиус меньше
радиуса атомов металлов
В простых веществах химическая связь ковалентная неполярная.
Слайд 6АЛЛОТРОПИЯ ОЛОВА
Экспедиция Р.Скотта к Южному полюсу в 1912 г. погибла из-за того, что
потеряла весь запас горючего, которое было в запаянных оловом баках. Какой химический процесс лежал в основе этого?
Слайд 7АЛЛОТРОПНЫЕ МОДИФИКАЦИИ ОЛОВА
Альфа – олово – неметалл, серый порошок
Бета – олово – металл
серебристо-белого цвета
Слайд 8ФИЗИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ
Блеск
Пластичность
Электропроводность
Теплопроводность
Ковкость
Слайд 9АЛЛОТРОПИЯ – СПОСОБНОСТЬ ОДНОГО ХИМИЧЕСКОГО ЭЛЕМЕНТА ОБРАЗОВЫВАТЬ НЕСКОЛЬКО ПРОСТЫХ ВЕЩЕСТВ, КОТОРЫЕ НАЗЫВАЮТ МОДИФИКАЦИЯМИ
ДАННОГО ЭЛЕМЕНТА.
 Лекция 2 Периодический закон
Лекция 2 Периодический закон Аммиак. Состав вещества
Аммиак. Состав вещества Синтетический каучук и его применение
Синтетический каучук и его применение Развивающие занятия в ГПД Поделочные камни
Развивающие занятия в ГПД Поделочные камни Вещества
Вещества Реакции солей в растворе. Гидролиз солей. Водородный показатель рН
Реакции солей в растворе. Гидролиз солей. Водородный показатель рН Альдегиды, свойства, получение, применение
Альдегиды, свойства, получение, применение Дифузія в побуті
Дифузія в побуті Granite
Granite Алкадиены (диены)
Алкадиены (диены) Классификация химических реакций
Классификация химических реакций Кремний және оның қосылыстары
Кремний және оның қосылыстары Карбонильные соединения. Альдегиды
Карбонильные соединения. Альдегиды Alyuminiy_ego_soedinenia
Alyuminiy_ego_soedinenia ООО Ангарский Азотно-туковый завод. Основы производства аммиака
ООО Ангарский Азотно-туковый завод. Основы производства аммиака Нефть. Состав. Свойства. Переработка
Нефть. Состав. Свойства. Переработка Классификация химических реакций
Классификация химических реакций Мицеллярные растворы ПАВ. Солюбилизация. Микроэмульсии
Мицеллярные растворы ПАВ. Солюбилизация. Микроэмульсии Химиялық жарыс кеші
Химиялық жарыс кеші Технологическая установка Л 24-6
Технологическая установка Л 24-6 Подготовка к ГИА. В3. Степень окисления химических элементов. Окислительно-восстановительные реакции
Подготовка к ГИА. В3. Степень окисления химических элементов. Окислительно-восстановительные реакции Добування кисню
Добування кисню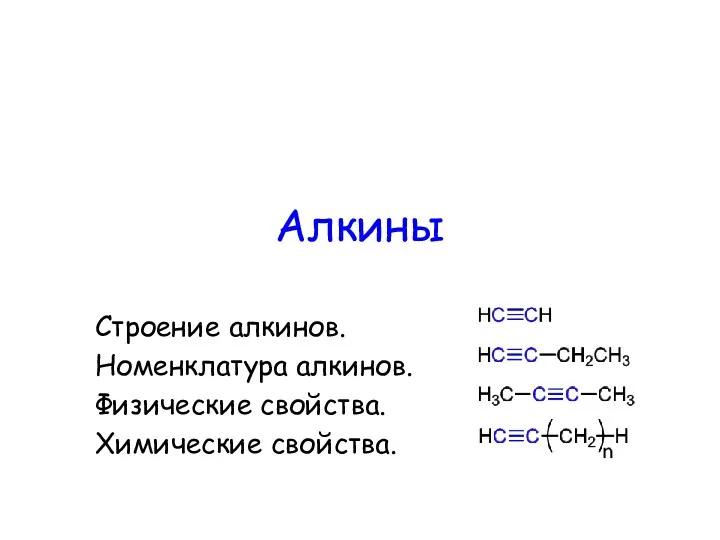 Алкины. Строение алкинов. Номенклатура алкинов. Физические свойства. Химические свойства
Алкины. Строение алкинов. Номенклатура алкинов. Физические свойства. Химические свойства Возникновение двойного электрического слоя
Возникновение двойного электрического слоя Классификация химических элементов. 8 класс
Классификация химических элементов. 8 класс Спектрофометрия
Спектрофометрия Нанокаталіз. Активність каталізатора
Нанокаталіз. Активність каталізатора Степень диссоциации. 9 класс
Степень диссоциации. 9 класс