Слайд 2

Алкины -
непредельные углеводороды, молекулы которых содержат, помимо одинарных связей,
одну тройную углерод-углеродную связь.
Общая формула: CnH2n-2
Слайд 3
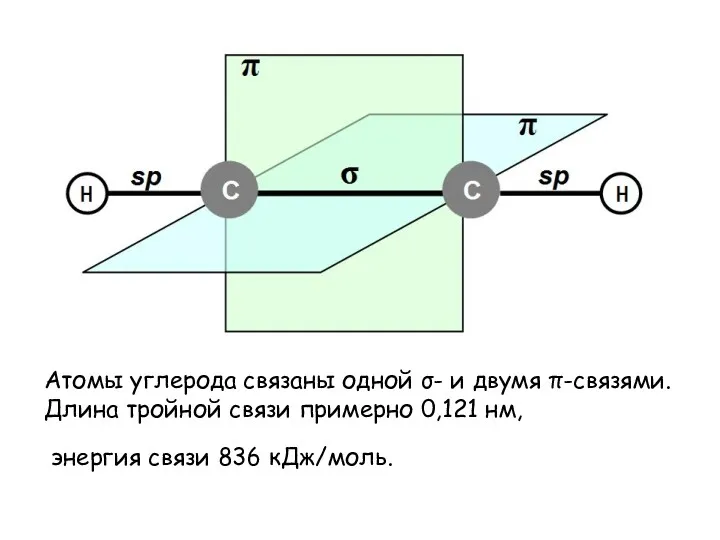
Атомы углерода связаны одной σ- и двумя π-связями.
Длина тройной связи примерно
0,121 нм,
энергия связи 836 кДж/моль.
Слайд 4
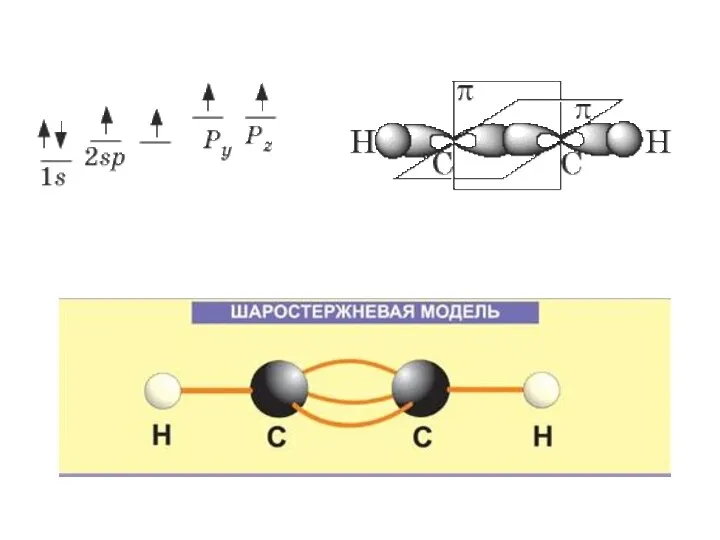
Слайд 5

Номенклатура алкинов
Простейшим алкином является этин (ацетилен C2H2).
По номенклатуре IUPAC названия
алкинов образуются от названий соответствующих алканов заменой суффикса «-ан» на «-ин»;
положение тройной связи указывается арабскими цифрами.
Слайд 6

Из приведенного перечня веществ
выпишите в тетрадь алкины
и дайте им
названия по номенклатуре IUPAC
Слайд 7

Изомерия алкинов
1. Структурная изомерия:
Изомерия углеродного скелета (пентин-1, 3-метилбутин-1);
Изомерия положения кратной связи
(бутин-1, бутин-2).
2. Межклассовая изомерия:
Алкины;
Алкадиены (диены)
Например, гексин-1 и гексадиен-1,3
Слайд 8

Физические свойства
низшие (до С4) — газы без цвета и запаха,
плохо растворимы
в воде,
лучше — в органических растворителях.
Слайд 9

Ацетилен (по ИЮПАК — этин) C2H2
Физические свойства:
бесцветный газ,
малорастворим в воде,
легче
воздуха.
Температура кипения − 83,8 °C.
При сжатии разлагается со взрывом,
Взрывоопасный.
Слайд 10

Способы получения ацетилена
Ацетилен был открыт Г. Дэви в 1836 году в
продуктах разложения метана, под действием искровых электрических разрядов
В 1860 г. М. Бертло синтезировал ацетилен из простых веществ, пропуская водород через электрическую дугу между угольными электродами.
В 1862 г. Ф. Велер получил ацетилен из карбида кальция, действуя на него водой.
Напишите уравнения реакций.
Слайд 11

Способы получения ацетилена
3.
Карбидный способ
Слайд 12

Химические свойства:
Горение
Температура ацетилено-кислородного пламени достигает 3200°С.
Используют для резки и сварки металлов.
2С2Н2
+ 5О2 4СО2 + 2Н2О
Слайд 13

Реакции присоединения
Гидрирование.
Галогенирование (2 стадии).
Гидратация.
Гидрогалогенирование.
Слайд 14

Слайд 15
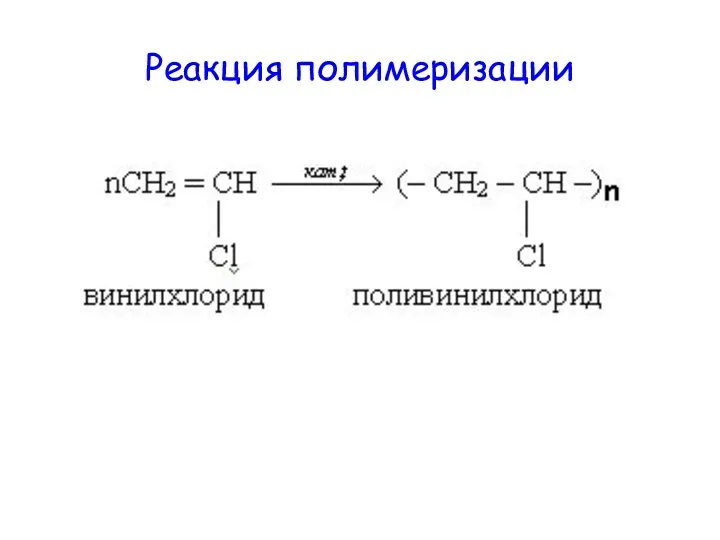
Слайд 16

ПОЛИВИНИЛХЛОРИД
Углекислый газ
Хлорорганические соединения
Вода
ЯД!
НЕ СЖИГАТЬ!
Слайд 17
















 Нафталин
Нафталин Периодический закон Д.И. Менделеева. Периодическая система химических элементов
Периодический закон Д.И. Менделеева. Периодическая система химических элементов Адсорбция на твердых телах
Адсорбция на твердых телах Оксиды. Физические и химические свойства
Оксиды. Физические и химические свойства Алкены (олефины). Лекция 3
Алкены (олефины). Лекция 3 СпиртыПростыеЭфиры-1
СпиртыПростыеЭфиры-1 Сучасні каталізатори у процесах нафтопереробки та нафтохімії
Сучасні каталізатори у процесах нафтопереробки та нафтохімії Влияние спирта на здоровье человека
Влияние спирта на здоровье человека Производные фурана, пиррола, тиофена
Производные фурана, пиррола, тиофена Арены
Арены Химическая связь. Взаимное влияние атомов в молекуле. Классификация реакций и реагентов
Химическая связь. Взаимное влияние атомов в молекуле. Классификация реакций и реагентов Анілін. Фізичні властивості
Анілін. Фізичні властивості Готовимся к экзамену по химии. 9 класс
Готовимся к экзамену по химии. 9 класс Протолитические равновесия и процессы. Лекция 3
Протолитические равновесия и процессы. Лекция 3 Кислоты. Общая характеристика, химические свойства
Кислоты. Общая характеристика, химические свойства Периодическая система химических элементов. Периоды
Периодическая система химических элементов. Периоды Теоретические основы металлургии. Благородные металлы
Теоретические основы металлургии. Благородные металлы Общая характеристика металлов. Металлическая связь
Общая характеристика металлов. Металлическая связь Растворы
Растворы Подгруппа азота
Подгруппа азота Металлы в природе. Общие способы их получения
Металлы в природе. Общие способы их получения Поливинилхлорид
Поливинилхлорид Фосфор. Открытие фосфора
Фосфор. Открытие фосфора Характеристика химического элемента на основании его положения в Периодической системе Д.И. Менделеева
Характеристика химического элемента на основании его положения в Периодической системе Д.И. Менделеева Обратимость химических реакций. Химическое равновесие и способы его смещения
Обратимость химических реакций. Химическое равновесие и способы его смещения Мини-проект по дисциплине: Физико-химические методы исследования и техника лабораторных работ
Мини-проект по дисциплине: Физико-химические методы исследования и техника лабораторных работ Горные породы
Горные породы Химический состав клетки. Неорганические вещества
Химический состав клетки. Неорганические вещества