Слайд 2Открытие фосфора
Гамбургский алхимик
Хеннинг Бранд
1669 год
«Фосфор» -
от греческого «светоносный»
Слайд 3Алхимик Х.Бранд, пытаясь отыскать «философский камень»,
получил удивительное вещество. Оказалось, что это был фосфор
.
Слайд 4Фосфор – простое вещество.
1.Химическая формула – Р.
2.Mr(Р) =31
3. М (Р) = 31г/моль
4. Физические
свойства.
Фосфор образует несколько аллотропных модификаций:
Химические свойства.
а) Фосфор – окислитель
1) Взаимодействие с металлами:
2P + 3Ca = Ca3P2 (фосфид кальция)
б) Фосфор – восстановитель
1) Горение
4Р + 5О2 =2Р2О5
2) Взаимодействие с галогенами (при нагревании)
2Р + 5CI2 = 2PCI5 (при избытке галогена)
2Р + 3CI2 = 2PCI3 (при избытке фосфора)
3) Взаимодействие с серой
2P + 5S = P2S5
2P + 3S = P2S3
С водородом фосфор непосредственно не реагирует. Газообразный фосфин РН3 получают косвенным путем, например:
Ca3P2 + 6H2O = 3Ca(OH)2 + 2PH3
Слайд 5Апати́т (от др.-греч. ἀπατάω «обманываю») — минерал класса фосфатов, как правило, бледно-зеленоватого, голубого, желто-зеленого
или розового цвета со стеклянным блеском.
Слайд 7Молекулы P4 имеют форму тетраэдра.
Слайд 10Являются атомными веществами с полимерной кристаллической решеткой
Слайд 12Слоистая атомная кристаллическая решетка
Слайд 14Химические свойства
Взаимодействие с простыми веществами
Фосфор легко окисляется кислородом
Взаимодействует со многими простыми веществами — галогенами,
серой, некоторыми металлами.
с металлами — окислитель, образует фосфиды
фосфиды разлагаются водой и кислотами с образованием фосфина
с неметаллами — восстановитель
Не взаимодействует с водородом.
Взаимодействие с водой
Взаимодействует с водяным паром при температуре выше 500 градусов по Цельсию, протекает реакция диспропорционирования с образованием фосфина и фосфорной кислоты:
Взаимодействие со щелочами
В холодных концентрированных растворах щелочей также медленно протекает реакция диспропорционирования:
Восстановительные свойства
Сильные окислители превращают фосфор в фосфорную кислоту
Реакция окисления фосфора происходит при поджигании спичек, в качестве окислителя выступает бертолетова соль
Слайд 15ПРИМЕНЕНИЕ ФОСФОРА
Р
удобрения
ядохимикаты
Производство
спичек
Создание
дымовых завес
полупроводники
Производство
красок
Защита от
коррозии
умягчение воды
моющие средства
Слайд 16Войска США
использовали фосфорные
Бомбы
в Ираке,
2004 г.
Слайд 17Р
ОРГАНИЗМЫ
МИНЕРАЛЫ
ФОСФОЛИПИДЫ,
ФЕРМЕНТЫ,
ФОСФАТ КАЛЬЦИЯ
ЭФИРЫ
ОРТОФОСФОРНОЙ
КИСЛОТЫ
В ЗУБАХ И КОСТЯХ
ФОСФОРИТ
БИРЮЗА
АПАТИТ
НАХОЖДЕНИЕ В ПРИРОДЕ
АПАТИТ
 Химические свойства основных оксидов
Химические свойства основных оксидов Методы разделения и концентрирования органических соединений. Сорбционные методы. (Лекция 3)
Методы разделения и концентрирования органических соединений. Сорбционные методы. (Лекция 3) Признаки химических реакций. (Практическая работа 5,4)
Признаки химических реакций. (Практическая работа 5,4)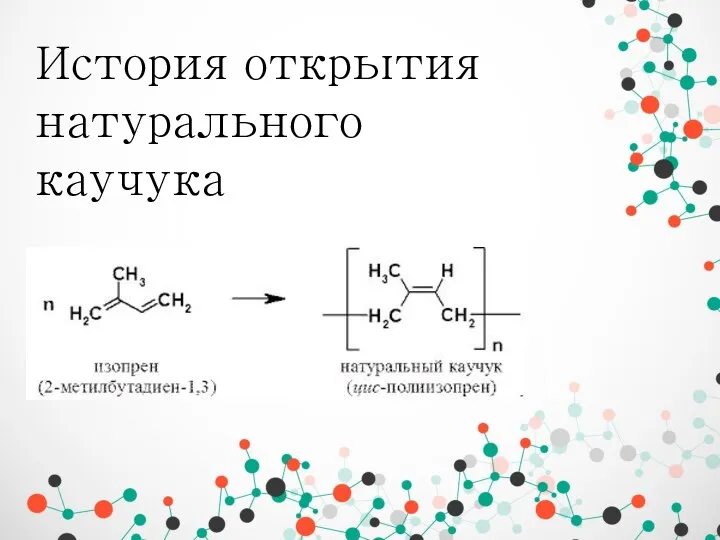 История открытия натурального каучука
История открытия натурального каучука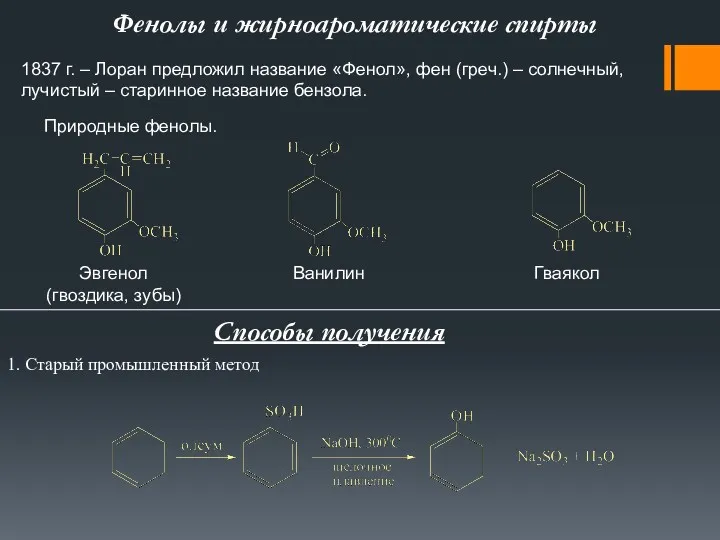 Фенолы и жирноароматические спирты
Фенолы и жирноароматические спирты Современные тенденции развития химии
Современные тенденции развития химии Закон сохранения массы веществ
Закон сохранения массы веществ Камни и минералы
Камни и минералы Реакции ионного обмена
Реакции ионного обмена Аминокислоты. Производные карбоновых кислот,
Аминокислоты. Производные карбоновых кислот, Хлор
Хлор Кислород. Химия. 8 класс
Кислород. Химия. 8 класс Мир запахов
Мир запахов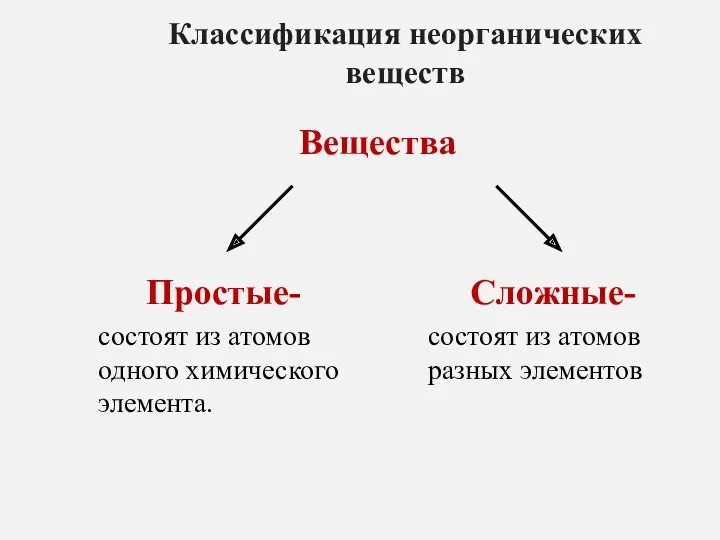 Классификация неорганических веществ
Классификация неорганических веществ Кто хочет стать химиком
Кто хочет стать химиком Основания. Состав, классификация, свойства, получение
Основания. Состав, классификация, свойства, получение Строение и переваривание липидов. Классификация и роль жирных кислот. Нутриомика. Липофильных соединений
Строение и переваривание липидов. Классификация и роль жирных кислот. Нутриомика. Липофильных соединений Основные понятия и законы химии
Основные понятия и законы химии Алюминий
Алюминий Молекулярно-кинетические свойства дисперсных систем
Молекулярно-кинетические свойства дисперсных систем Научно-исследовательская работа Вся правда о продуктах с сахарозаменителями
Научно-исследовательская работа Вся правда о продуктах с сахарозаменителями Жесткость воды и способы её устранения
Жесткость воды и способы её устранения Гетероциклдік қосылыстар
Гетероциклдік қосылыстар Cleaners for
Cleaners for Непредельные углеводороды: алкены, олефины
Непредельные углеводороды: алкены, олефины Химический элементы в нашей жизни
Химический элементы в нашей жизни Задача №5. Аккумулятор на основе железа
Задача №5. Аккумулятор на основе железа Проект Кабинет химии будущего
Проект Кабинет химии будущего