Содержание
- 2. условие 5. Железный аккумулятор На сегодняшний день создано большое количество различных аккумуляторов – химических источников тока
- 3. Виды аккумуляторов Свинцово-Кислотные Никель-кадмиевые Никель-железные Никель-металлогидридные Никель-цинковые Серебряно-цинковые Никель-водородные Литий-ионные Литий-полимерные марганцево-цинковые Кислотно-свинцовый аккумулятор Литий-ионный аккамклятор
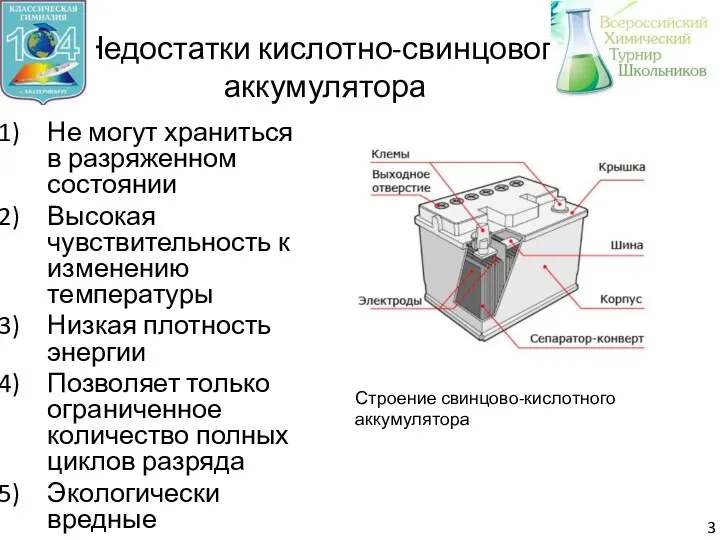
- 4. Недостатки кислотно-свинцового аккумулятора Не могут храниться в разряженном состоянии Высокая чувствительность к изменению температуры Низкая плотность
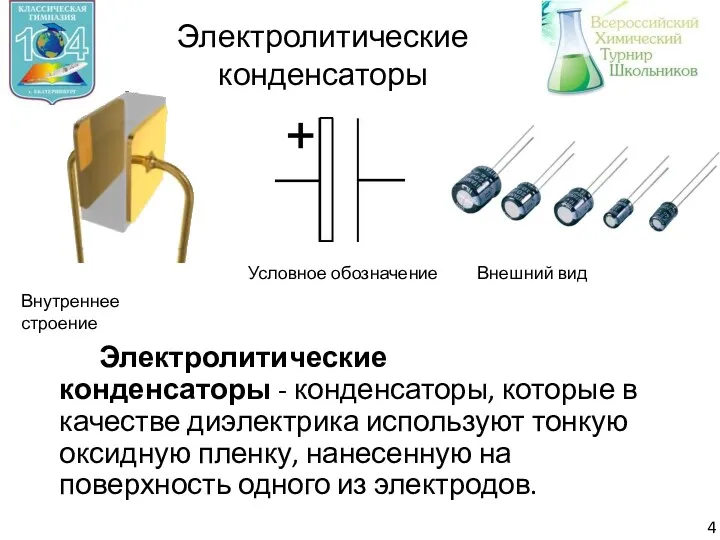
- 5. Электролитические конденсаторы Электролитические конденсаторы - конденсаторы, которые в качестве диэлектрика используют тонкую оксидную пленку, нанесенную на
- 6. Преймущества и недостатки элетролитических конденсаторов Преймущества: большая ёмкость энегрии небольшие габариты низкая стоимость Простота производства Недостатки:
- 7. Электрический аккумулятор на основе солей железа VI патент №2170476 Один из электродов-анод, а другой - катод
- 8. Способы получения солей железа VI 7
- 9. вывод образовалолось два варианта создания и применения аккумуляторов на основе железа. предпочтение отдаётся второму(петент №2170476). 8
- 11. Скачать презентацию





 Материаловедение и технология обработки материалов
Материаловедение и технология обработки материалов Лекция 1 эквивалент 2
Лекция 1 эквивалент 2 c0198e3edf1db804a5527004a7864ed1
c0198e3edf1db804a5527004a7864ed1 Процессы сульфирования в промышленности
Процессы сульфирования в промышленности Химические реакции. Реакции обмена
Химические реакции. Реакции обмена Игровая программа по химии Самый умный. Химические свойства оксидов, оснований, кислот и солей
Игровая программа по химии Самый умный. Химические свойства оксидов, оснований, кислот и солей Знакомство с образцами химических средств санитарии и гигиены
Знакомство с образцами химических средств санитарии и гигиены Минералы и Близнецы
Минералы и Близнецы Серная кислота H2SO4
Серная кислота H2SO4 Химический состав воздуха
Химический состав воздуха Дисперсные системы
Дисперсные системы Жир жиру рознь. Супер омега 3
Жир жиру рознь. Супер омега 3 Важнейшие оксиды в природе и жизни человека
Важнейшие оксиды в природе и жизни человека Электронное и пространственное строение молекул органических соединений – основа их биологической активности
Электронное и пространственное строение молекул органических соединений – основа их биологической активности Виды камней
Виды камней Лекция 5. Коллигативные свойства растворов
Лекция 5. Коллигативные свойства растворов 20231104_prezentatsiya_teoriya_elektroliticheskoy_dissotsiatsii
20231104_prezentatsiya_teoriya_elektroliticheskoy_dissotsiatsii Общие проблемы определения низких концентраций
Общие проблемы определения низких концентраций Автомобильные бензины
Автомобильные бензины Чистые вещества и смеси. Способы разделения смесей
Чистые вещества и смеси. Способы разделения смесей Природные источники углеводородов. 10 класс
Природные источники углеводородов. 10 класс Растворы. Способы выражения концентраций. Сильные и слабые электролиты. Закон разведения Оствальда. Лекция 02-1
Растворы. Способы выражения концентраций. Сильные и слабые электролиты. Закон разведения Оствальда. Лекция 02-1 Физико-химические процессы в системе свинец - сталь - кислород, для энергетических ядерных реакторов
Физико-химические процессы в системе свинец - сталь - кислород, для энергетических ядерных реакторов Процессы в растворах: электролитическая диссоциация (ЭД)
Процессы в растворах: электролитическая диссоциация (ЭД) Строение атомов. Понятие о квантовой механике
Строение атомов. Понятие о квантовой механике Серная кислота. Свойства разбавленной серной кислоты, соли серной кислоты
Серная кислота. Свойства разбавленной серной кислоты, соли серной кислоты Химикаты для сельского хозяйства
Химикаты для сельского хозяйства ПРОСТЫЕ ВЕЩЕСТВА -НЕМЕТАЛЛЫ
ПРОСТЫЕ ВЕЩЕСТВА -НЕМЕТАЛЛЫ