Содержание
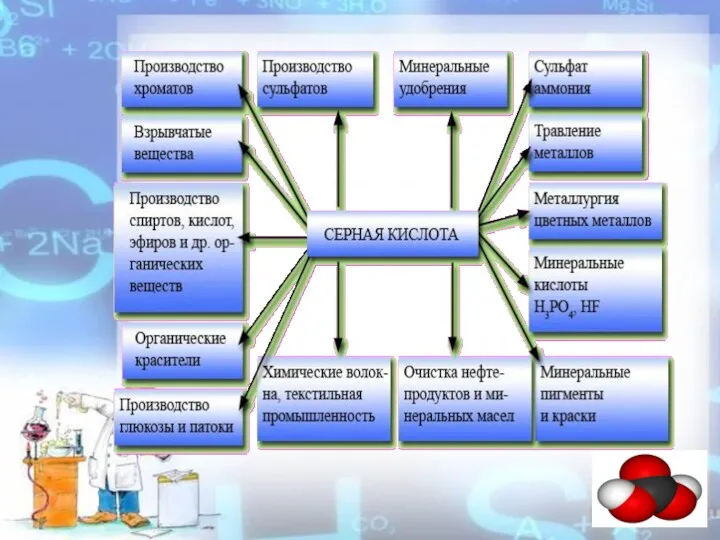
- 2. Серная кислота H2SO4 — сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6). При обычных условиях
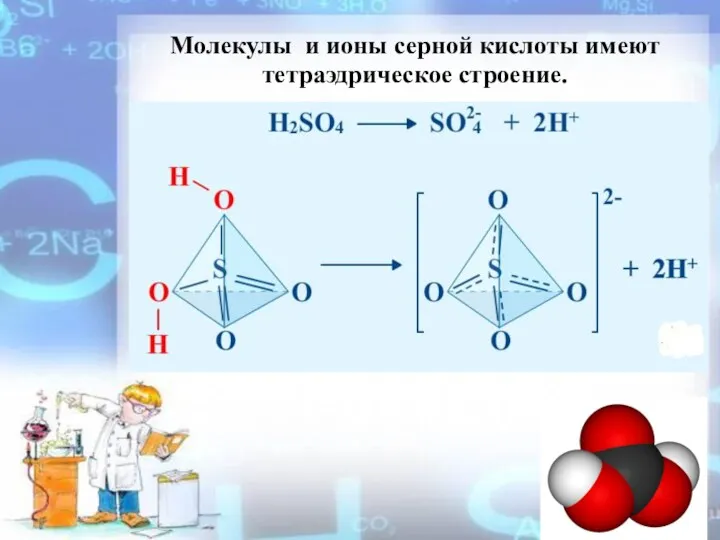
- 3. Молекулы и ионы серной кислоты имеют тетраэдрическое строение.
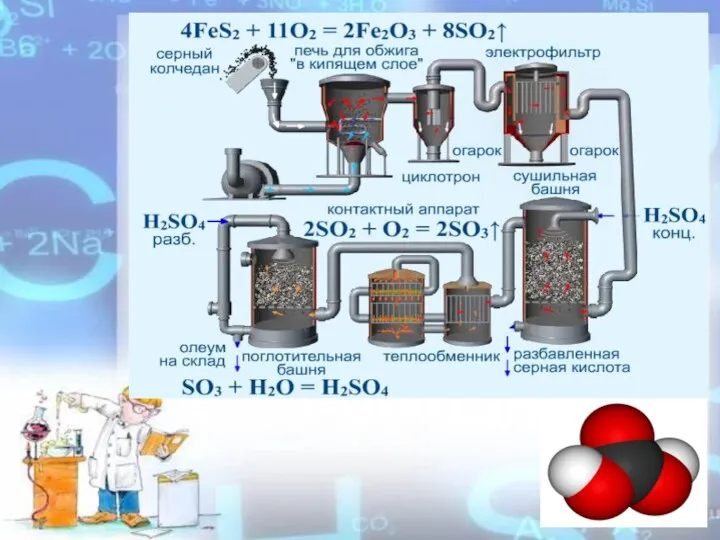
- 4. FeS2 S H2S SO2 → SO3 → H2SO4 Пирит Серный колчедан Получение серной кислоты
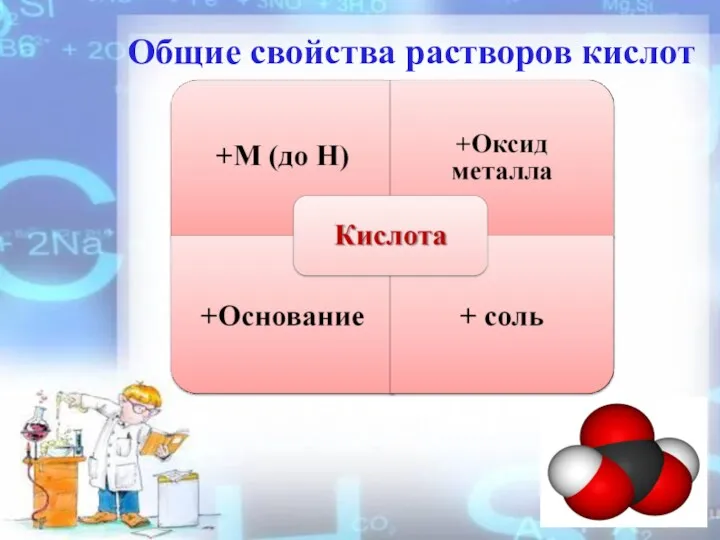
- 6. Общие свойства растворов кислот
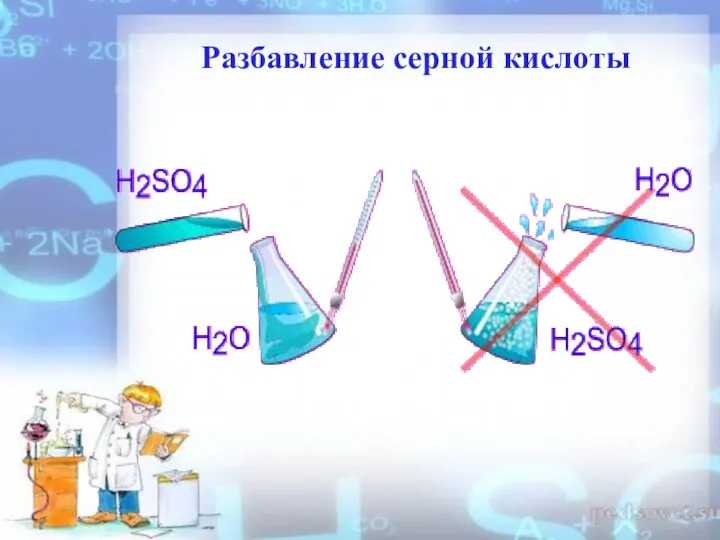
- 7. Разбавление серной кислоты
- 8. I. Химические свойства разбавленной серной кислоты 1.Диссоциация: H2SO4 H+ + HSO4- HSO4- ↔ H+ + SO42-
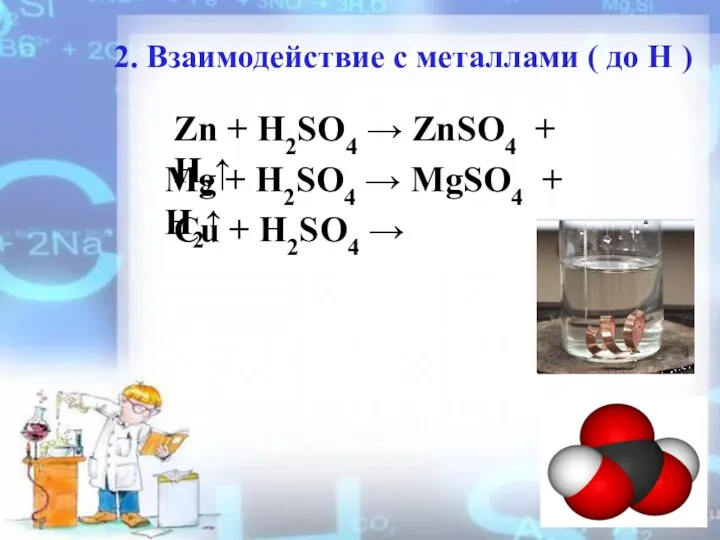
- 9. 2. Взаимодействие с металлами ( до Н ) Zn + H2SO4 → ZnSO4 + H2↑ Mg
- 10. 3. Взаимодействие с оcновными и амфотерными оксидами CuO + H2SO4 → CuSO4 + H2O CuO +
- 11. 4. Взаимодействие с основаниями и амфотерными гидроксидами 2NaOH + H2SO4 → Na2SO4 +2 H2O H+ +
- 12. 5.Взаимодействие с солями H2SO4+BaCI2 = BaSO4 ↓ + 2HCI Ba2++SO42- = BaSO4 ↓ K2CO3 + H2SO4
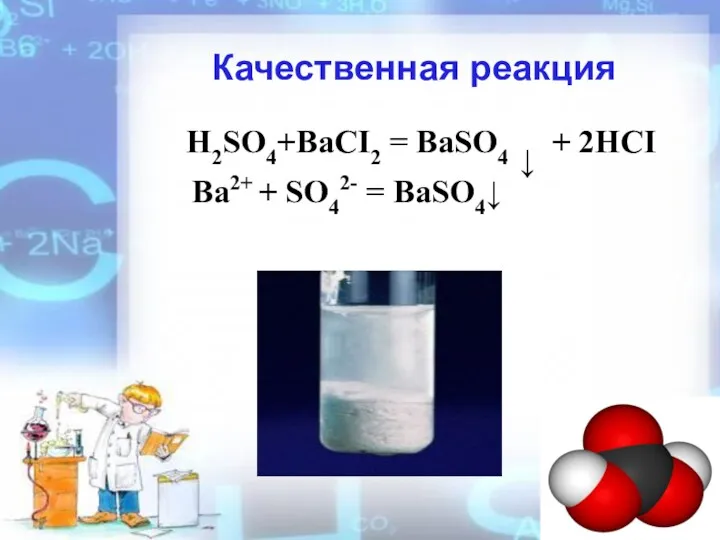
- 13. Качественная реакция H2SO4+BaCI2 = BaSO4 ↓ + 2HCI Ba2+ + SO42- = BaSO4↓
- 14. Серная кислота вытесняет более летучие кислоты NaCI + H2SO4 → NaHSO4 + HCI
- 15. Свойства концентрированной серной кислоты Органические вещества обугливаются !!! C12H22O11 (сахароза) → 12С (уголь)
- 16. концентрированная серная кислота окисляет неметаллы неМе + H2SO4(конц.) = H2O + SO2 + кислородсодержащая кислота неМе,
- 17. концентрированная серная кислота окисляет металлы концентрированная H2+6SO4 – сильный окислитель; при взаимодействии с металлами (кроме Au,
- 20. Скачать презентацию










 Различные теории кислот и оснований
Различные теории кислот и оснований Электролитическая диссоциация. Положительно-заряженный электрод
Электролитическая диссоциация. Положительно-заряженный электрод Методические рекомендации по изучению курса Коррозия и защита металлов
Методические рекомендации по изучению курса Коррозия и защита металлов Энергетика химических процессов. Термодинамика. (Лекция 4)
Энергетика химических процессов. Термодинамика. (Лекция 4) Тренувальні вправи. Задачі
Тренувальні вправи. Задачі Циклоалканы. Предельные углеводороды с замкнутой (циклической) углеродной цепью
Циклоалканы. Предельные углеводороды с замкнутой (циклической) углеродной цепью Карбоновые кислоты
Карбоновые кислоты Метали IV групи побічної підгрупи (Ti, Zr, Hf)
Метали IV групи побічної підгрупи (Ti, Zr, Hf) Типы химических реакций
Типы химических реакций Общая характеристика металлов главных подгрупп I-III групп ПСХЭ Д.И. Менделеева
Общая характеристика металлов главных подгрупп I-III групп ПСХЭ Д.И. Менделеева Химические и физические свойства воды
Химические и физические свойства воды Каучук туралы жалпы мәліметтер
Каучук туралы жалпы мәліметтер Чисті речовини та суміші. Основні способи розділення сумішей (7 клас)
Чисті речовини та суміші. Основні способи розділення сумішей (7 клас) Химический элемент алюминий
Химический элемент алюминий Спирты
Спирты Типы химических реакций
Типы химических реакций Электролиты и неэлектролиты. Механизм электролитической диссоциации
Электролиты и неэлектролиты. Механизм электролитической диссоциации Теория электролитической диссоциации
Теория электролитической диссоциации Бериллий, магний и щелочноземельные металлы
Бериллий, магний и щелочноземельные металлы Механизмы органических реакций
Механизмы органических реакций Мицеллярные растворы ПАВ. Солюбилизация. Микроэмульсии
Мицеллярные растворы ПАВ. Солюбилизация. Микроэмульсии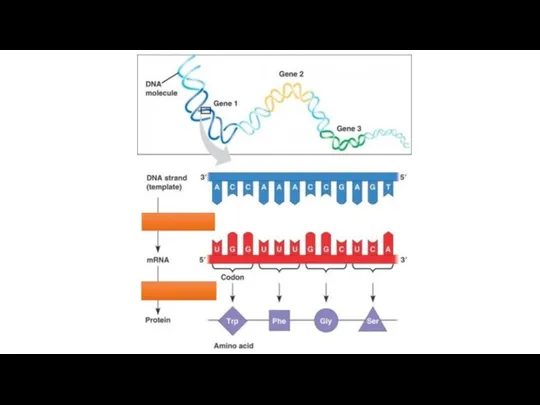 The translation and transcription
The translation and transcription Основи. Фізичні властивості основ
Основи. Фізичні властивості основ Готовимся к экзамену по химии. 9 класс
Готовимся к экзамену по химии. 9 класс Ионоселективные электроды
Ионоселективные электроды Виртуозы химического эксперимента
Виртуозы химического эксперимента Химический состав воздуха
Химический состав воздуха Типы химических соединений, номенклатура, свойства
Типы химических соединений, номенклатура, свойства