Содержание
- 3. РОЗ’ЯЗОК ЗАДАЧ І рівень - легкий Яка маса ферум (ІІ) сульфіду утвориться при взаємодії 8 г
- 4. ІІ рівень – середньої складності Німецький хімік Йоганн Рудольф Глаубер відкрив методи добування багатьох солей і
- 5. 2) Англійський хімік технолог Генрі Дікон у 1867 році розробив спосіб добування хлору шляхом каталітичного окислення
- 7. Скачать презентацию
Слайд 2
Слайд 3
РОЗ’ЯЗОК ЗАДАЧ
І рівень - легкий
Яка маса ферум (ІІ) сульфіду утвориться
РОЗ’ЯЗОК ЗАДАЧ
І рівень - легкий
Яка маса ферум (ІІ) сульфіду утвориться
при взаємодії 8 г заліза і 8 г сірки?
Чи досить нітратної кислоти масою 60г для взаємодії з кальцій гідроксидом масою 37г? Яка маса кальцій нітрату утвориться?
Амоніак масою 85кг був пропущений через нітритну кислоту масою 300кг. Яку масу амоній нітриту отримали?
Чи досить нітратної кислоти масою 60г для взаємодії з кальцій гідроксидом масою 37г? Яка маса кальцій нітрату утвориться?
Амоніак масою 85кг був пропущений через нітритну кислоту масою 300кг. Яку масу амоній нітриту отримали?
Слайд 4
ІІ рівень – середньої складності
Німецький хімік Йоганн Рудольф Глаубер відкрив методи
ІІ рівень – середньої складності
Німецький хімік Йоганн Рудольф Глаубер відкрив методи
добування багатьох солей і кислот. В історії хімії найбільше відомі дві реакції Глаубера: одержання натрій сульфату (“глауберової солі”) і хлороводню під час взаємодії кухонної солі з сульфатною кислотою, і синтез “сурм’яного масла”. “Сурм’яне масло” – це старовинна назва стибій (III) хлориду SbCI3. Як ви, вважаєте, для чого можна застосовувати дану сполуку?.
Глаубер отримав SbCI3 (“сурм’яне масло”) із наступної реакції:
3HgCI2+Sb2S3 = 2SbCI3↑+3HgS.
Скільки золотників “сурм’яного масла” (1 золотник=4,266 г) можна добути із 153,32 г HgCI2 і 64,53 г Sb2S3.
Глаубер отримав SbCI3 (“сурм’яне масло”) із наступної реакції:
3HgCI2+Sb2S3 = 2SbCI3↑+3HgS.
Скільки золотників “сурм’яного масла” (1 золотник=4,266 г) можна добути із 153,32 г HgCI2 і 64,53 г Sb2S3.
Слайд 5
2) Англійський хімік технолог Генрі Дікон у 1867 році розробив спосіб
2) Англійський хімік технолог Генрі Дікон у 1867 році розробив спосіб
добування хлору шляхом каталітичного окислення хлороводню киснем повітря при температурі 400º С в присутності каталізатора – купрум (ІІ) хлориду:
CuCl2 + 4HCl + O2 = 2Cl2 + 2H2O.
Цей метод отримав назву реакції Дікона, а промислова технологія – процес Дікона.
Обчисліть, який об’єм хлору можна добути, в ході процесу Дікона з 100 (кг) хлороводню і 16 (мл) кисню.
CuCl2 + 4HCl + O2 = 2Cl2 + 2H2O.
Цей метод отримав назву реакції Дікона, а промислова технологія – процес Дікона.
Обчисліть, який об’єм хлору можна добути, в ході процесу Дікона з 100 (кг) хлороводню і 16 (мл) кисню.




 Химический элемент уран
Химический элемент уран Азот. Элемент V группы главной подгруппы
Азот. Элемент V группы главной подгруппы Алкины. Ацетилен.
Алкины. Ацетилен. Periodic Table and Trends
Periodic Table and Trends Непредельные углеводороды. Алкены
Непредельные углеводороды. Алкены Классификация процессов и производств в химической технологии
Классификация процессов и производств в химической технологии Химический элемент. Неон
Химический элемент. Неон Предмет органической химии
Предмет органической химии Закон Авогадро. Молярный объём газов
Закон Авогадро. Молярный объём газов Производство серной кислоты контактным способом
Производство серной кислоты контактным способом Роль химии в создании новых материалов
Роль химии в создании новых материалов Пластмаси. Пластичні маси
Пластмаси. Пластичні маси Основания
Основания Типы химических реакций
Типы химических реакций Аминокислоты. Номенклатура
Аминокислоты. Номенклатура Производные фурана, пиррола, тиофена
Производные фурана, пиррола, тиофена Функциональные производные углеводородов. Галогенопроизводные углеводородов
Функциональные производные углеводородов. Галогенопроизводные углеводородов Анализ технологии производства с использованием принципов Зеленой химии
Анализ технологии производства с использованием принципов Зеленой химии Минералогия. Формы нахождения минералов в природе. Свойства минералов
Минералогия. Формы нахождения минералов в природе. Свойства минералов Решение расчетных задач по уравнениям реакций
Решение расчетных задач по уравнениям реакций Знакомство с образцами химических средств санитарии и гигиены
Знакомство с образцами химических средств санитарии и гигиены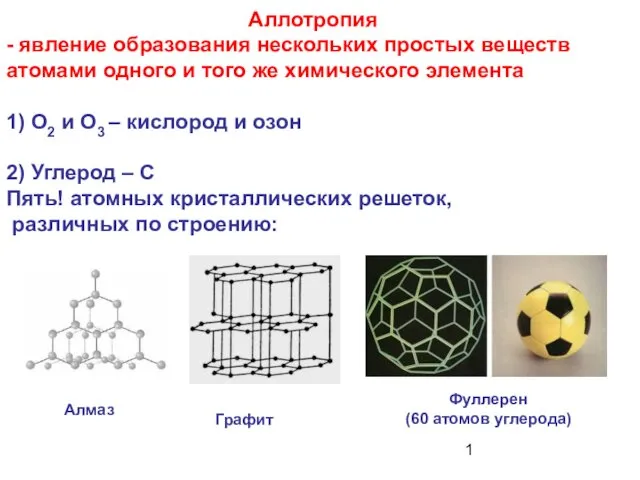 Аллотропия - явление образования нескольких простых веществ атомами одного и того же химического элемента
Аллотропия - явление образования нескольких простых веществ атомами одного и того же химического элемента Йод. Йодтың ашылуы
Йод. Йодтың ашылуы Кристалічний і аморфний стани твердих речовин
Кристалічний і аморфний стани твердих речовин Термохимия. Расчет тепловых эффектов химических реакций
Термохимия. Расчет тепловых эффектов химических реакций Применение центрифугирования
Применение центрифугирования Кислоты
Кислоты Таблица Менделеева
Таблица Менделеева