Все благородные газы имеют завершенную электронную оболочку, поэтому они химически инертны. Химическая
инертность неонаисключительна, в этом с ним может конкурировать только гелий. Пока не получено ни одного его валентного соединения. Даже так называемые клатратные соединения неона с водой (Ne·6Н2О), гидрохиноном и другими веществами (подобные соединения тяжелых благородных газов — радона, ксенона, криптона и даже аргона — широко известны) получить и сохранить очень трудно.
Однако, с помощью методов оптической спектроскопии и масс-спектрометрии установлено существование ионов Ne+, (NeAr)+, (NeH)+, и (HeNe)+.
Химические свойства






 Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон и периодическая система химических элементов Д.И. Менделеева Строение атома
Строение атома Спирты
Спирты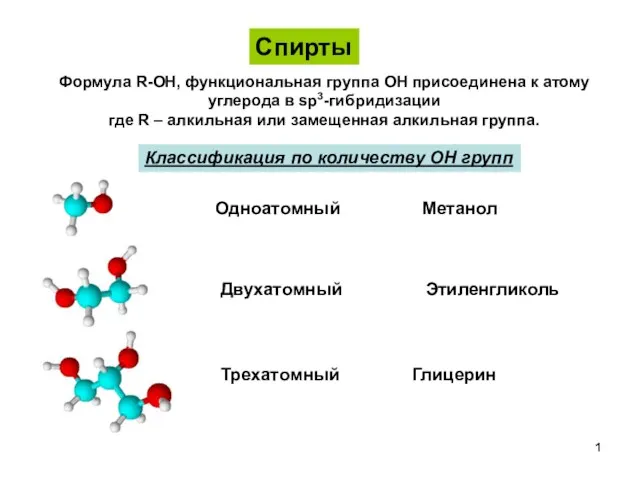 Спирты, фенолы, простые эфиры
Спирты, фенолы, простые эфиры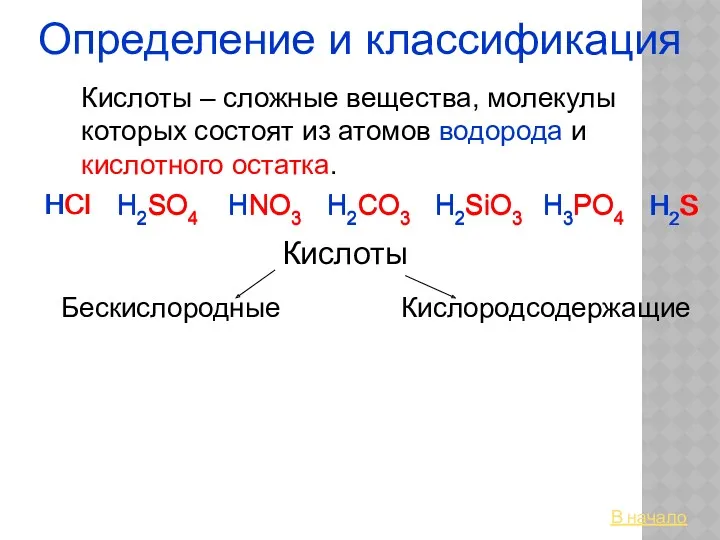 Кислоты. Определение и классификация
Кислоты. Определение и классификация Хлор. Состав. Строение
Хлор. Состав. Строение Дисперсная система
Дисперсная система Галогены. Строение атома
Галогены. Строение атома Электролиз. Области использования электролиза
Электролиз. Области использования электролиза Предмет и история геохимии
Предмет и история геохимии Простые вещества металлы
Простые вещества металлы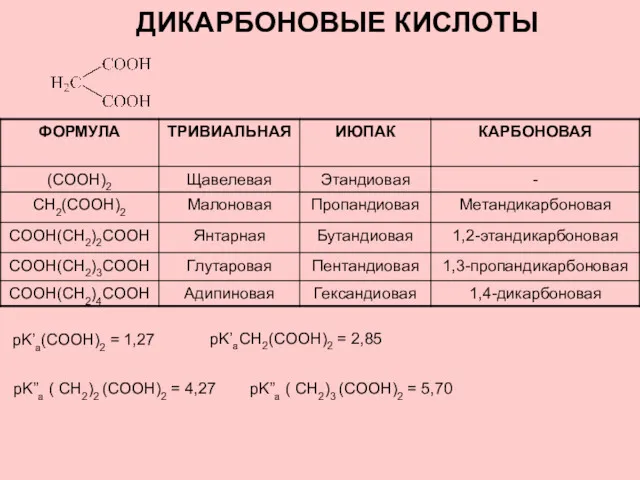 Дикарбоновые кислоты
Дикарбоновые кислоты Гидролиз органических и неорганических веществ, солей
Гидролиз органических и неорганических веществ, солей Висмут, ртуть, сурьма
Висмут, ртуть, сурьма Аффинаж солей урана. Получение оксидов урана
Аффинаж солей урана. Получение оксидов урана Витамины. Аскорбиновая кислота
Витамины. Аскорбиновая кислота Теоретические и экспериментальные методы исследования в химии
Теоретические и экспериментальные методы исследования в химии Курс лекций: Методы диагностики и анализа микро- и наносистем
Курс лекций: Методы диагностики и анализа микро- и наносистем ОСНОВАНИЯ, ИХ КЛАССИФИКАЦИЯ И СВОЙСТВА
ОСНОВАНИЯ, ИХ КЛАССИФИКАЦИЯ И СВОЙСТВА Карбонаты. Классификация
Карбонаты. Классификация Щелочноземельные металлы
Щелочноземельные металлы Виявлення в розчині гідроксид-іонів та йонів Гідрогену. Якісні реакції на деякі йони. Застосування якісних реакцій
Виявлення в розчині гідроксид-іонів та йонів Гідрогену. Якісні реакції на деякі йони. Застосування якісних реакцій Композиционные материалы. Материалы порошковой металлургии: пористые, конструкционные, электротехнические
Композиционные материалы. Материалы порошковой металлургии: пористые, конструкционные, электротехнические Выделение ферментных препаратов методами осаждения и высаливания
Выделение ферментных препаратов методами осаждения и высаливания Качественный анализ. Классификация катионов и анионов. (Лекция 2)
Качественный анализ. Классификация катионов и анионов. (Лекция 2) Качественный анализ (часть 1)
Качественный анализ (часть 1) Визитка химического элемента. Водород
Визитка химического элемента. Водород Фосфор и его соединения
Фосфор и его соединения