Содержание
- 2. Содержание : 1. Определение сущности процесса электролиза 2. Электролиз в расплавах: а) процессы на катоде б)
- 3. Электролиз – это окислительно-восстановительный процесс, протекающий на электродах в растворах или расплавах электролитов при пропускании электрического
- 4. Электролиз в расплавах На катоде происходит процесс восстановления • В расплавах катионы металла восстанавливаются до свободного
- 5. Электролиз в расплавах На аноде происходит процесс окисления • В расплавах анионы бескислородных кислот (кроме фторидов)
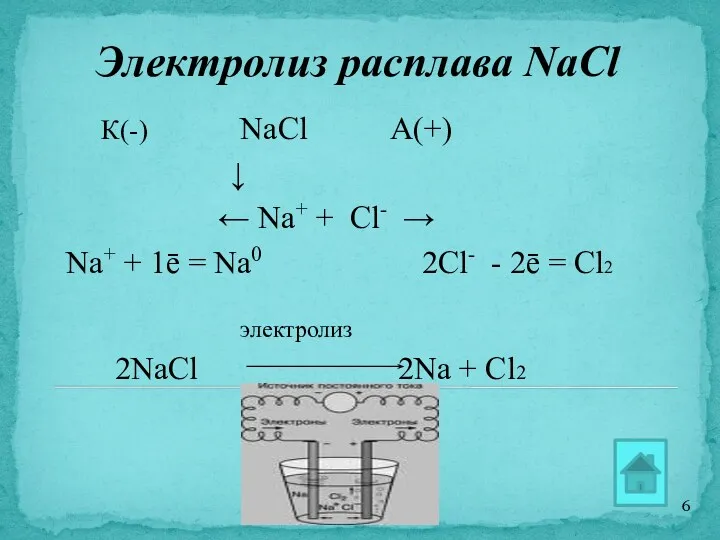
- 6. Электролиз расплава NaCl К(-) NaCl А(+) ↓ ← Na+ + Cl- → Na+ + 1ē =
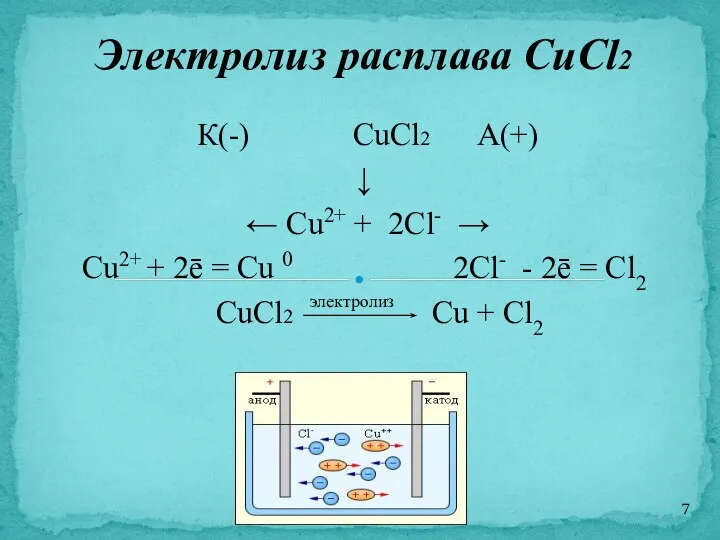
- 7. К(-) CuCl2 А(+) ↓ ← Cu2+ + 2Cl- → Cu2+ + 2ē = Cu 0 2Cl-
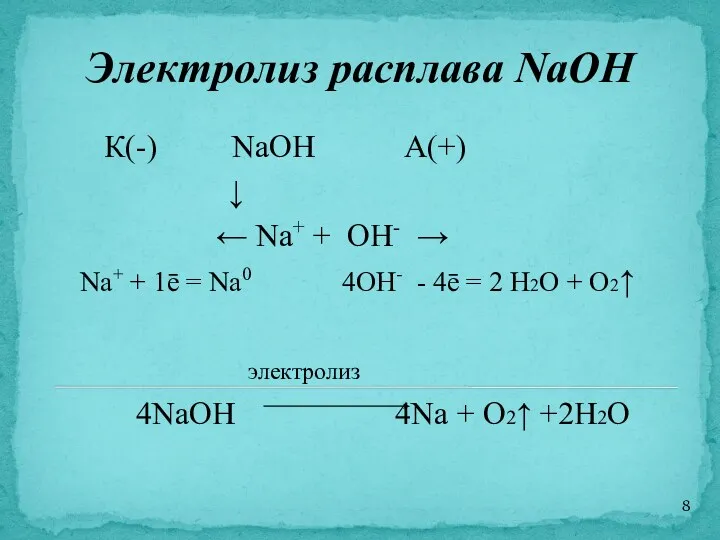
- 8. Электролиз расплава NaOH К(-) NaOH А(+) ↓ ← Na+ + OH- → Na+ + 1ē =
- 9. Электролиз в растворах (процесс на катоде) В растворах процесс на катоде не зависит от материала катода,
- 10. Электролиз в растворах (процесс на катоде) б) Если металл расположен в ряду напряжений между Al и
- 11. Процесс на аноде В растворах процесс на аноде зависит от материала анода и от природы аниона.
- 12. Процесс на аноде б) Если анод инертный, то в случае бескислородных анионов (кроме фторидов) идет окисление
- 13. Электролиз раствора NaCl на инертном аноде К(-) NaCl А(+) ↓ ← Na+ + Cl- → 2Н2О
- 14. Электролиз раствора CuSO4 на инертном аноде К(-) CuSO4 А(+) ↓ ← Cu2+ + SO42- → Cu2+
- 15. Электролиз раствора NaCl на растворимом аноде К(-) NaCl А(+) ↓ (Cu) ← Na+ + Cl- →
- 16. Применение электролиза: получение чистых металлов (Алюминий, магний, натрий, кадмий получают только электролизом)
- 17. очистка металлов
- 18. получение щелочей, хлора, водорода
- 19. защита металлов от коррозии (При этом на поверхности металлических изделий электрохимическим методом наносят тонкий слой другого
- 20. копирование рельефных изделий из металлов и других материалов. Гальванопластика позволяет создавать документально точные копии барельефов, монет,
- 21. применение электролиза в косметологии для электроэпиляции (при удалении волос этим методом используются очень тонкие иголочки, которыми
- 22. Тест по теме "Электролиз" 1. При электролизе раствора сульфата цинка с инертными электродами на аноде выделяется:
- 23. 3. При электролизе расплава гидроксида натрия на аноде выделяется: а) натрий; б) водород; в) кислород; г)
- 24. 5. Процесс на катоде при электролизе растворов солей зависит от: а) природы катода; б) активности металла;
- 25. 7. При электролизе 240 г 15%-го раствора гидроксида натрия на аноде выделилось 89,6 л (н.у.) кислорода.
- 26. А теперь проверим ваши ответы! 1-б 2-б 3-в, г 4-а, г 5-б 6- в 7- в
- 27. Домашнее задание: Учебник О.С.Габриеляна Химия 11 класс § 18 (стр.217 - 222), упр. 22,23,25.
- 28. Список использованной литературы: 1. О.С.Габриелян Учебник химии для 11 класса, М., Дрофа, 2004г. Интернет – ресурсы:
- 30. Скачать презентацию























 Диены (диолефины, алкадиены)
Диены (диолефины, алкадиены) Застосування неметалів
Застосування неметалів Строение вещества. Химические элементы
Строение вещества. Химические элементы Простые вещества. Сложные вещества
Простые вещества. Сложные вещества Степень окисления элементов
Степень окисления элементов Химические основы жизни
Химические основы жизни Химическая связь и ее типы. Кристаллические решётки
Химическая связь и ее типы. Кристаллические решётки Периодический закон Менделеева
Периодический закон Менделеева Железо, его характеристики, свойства и соединения
Железо, его характеристики, свойства и соединения Строение атома. Периодическая таблица Менделеева. Химическая связь
Строение атома. Периодическая таблица Менделеева. Химическая связь Химический состав водоотталкивающих средств
Химический состав водоотталкивающих средств Нефть - природный источник углеводородов
Нефть - природный источник углеводородов Фазовые диаграммы бинарных систем с полиморфными превращениями на примере фазовой диаграммы системы железо-цементит Fe Fe3C
Фазовые диаграммы бинарных систем с полиморфными превращениями на примере фазовой диаграммы системы железо-цементит Fe Fe3C Фазовое равновесие
Фазовое равновесие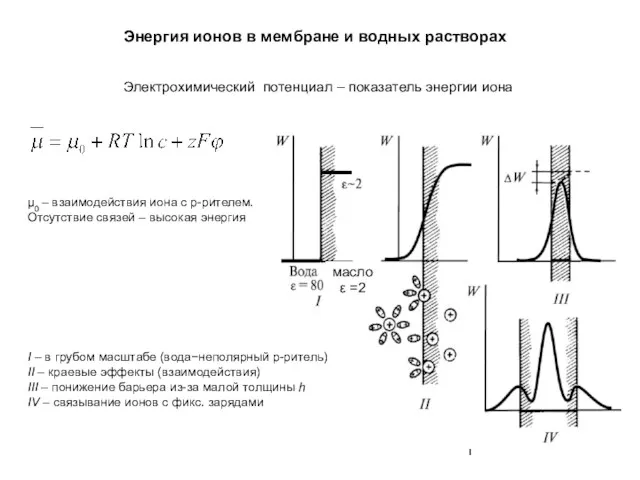 Энергия ионов в мембране и водных растворах
Энергия ионов в мембране и водных растворах Обмен сложных липидов
Обмен сложных липидов Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы
Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы Этиловый спирт в жизни человека
Этиловый спирт в жизни человека Основні класи неорганічних сполук
Основні класи неорганічних сполук Органические соединения серы
Органические соединения серы Галогены. Строение атомов фтора и хлора
Галогены. Строение атомов фтора и хлора Главная подгруппа IV группы. Общая характеристика элементов
Главная подгруппа IV группы. Общая характеристика элементов Естествознание для всех. Викторина
Естествознание для всех. Викторина Дисперсные системы
Дисперсные системы Галогены. Получение и применение галогенов
Галогены. Получение и применение галогенов Автомобильные пластичные смазки
Автомобильные пластичные смазки Нітроген
Нітроген Химическая технология. Введение
Химическая технология. Введение