Содержание
- 2. Что такое спирты? СПИРТЫ (алкоголи) – класс органических соединений, содержащих одну или несколько группировок С–ОН, при
- 3. Классификация спиртов Классификация спиртов разнообразна и зависит от того, какой признак строения взят за основу. 1.
- 4. 2)По типу атома углерода, с которым связана группа ОН, спирты делят на: а) первичные, у которых
- 5. в) третичные, у которых ОН-группа связана с третичным атомом углерода. Третичный углеродный атом (выделен зеленым цветом)
- 6. В соответствии с типом углеродного атома присоединенную к нему спиртовую группу также называют первичной, вторичной или
- 7. Номенклатура спиртов. Для распространенных спиртов, имеющих простое строение, используют упрощенную номенклатуру: название органической группы преобразуют в
- 8. В том случае, когда строение органической группы более сложное, используют общие для всей органической химии правила.
- 9. Систематические названия простейших спиртов составляют по тем же правилам: метанол, этанол, бутанол. Для некоторых спиртов сохранились
- 10. Физические свойства спиртов. Спирты растворимы в большинстве органических растворителей, первые три простейших представителя – метанол, этанол
- 11. Химические свойства спиртов. Спирты отличаются разнообразными превращениями. Реакции спиртов имеют некоторые общие закономерности: реакционная способность первичных
- 12. Реакции, протекающие по связи О–Н. При взаимодействии с активными металлами (Na, K, Mg, Al) спирты проявляют
- 14. При действии окислителей (К2Cr2O7, KMnO4) первичные спирты образуют альдегиды, а вторичные – кетоны (рис.7) Рис. 7.
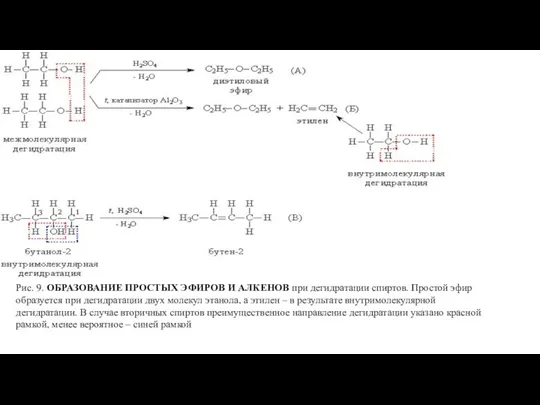
- 15. Реакции, протекающие по связи С–О. В присутствии катализаторов или сильных минеральных кислот происходит дегидратация спиртов (отщепление
- 16. Рис. 9. ОБРАЗОВАНИЕ ПРОСТЫХ ЭФИРОВ И АЛКЕНОВ при дегидратации спиртов. Простой эфир образуется при дегидратации двух
- 17. Разрыв связи С–О в спиртах происходит также при замещении ОН-группы галогеном, или аминогруппой (рис. 10). Рис.
- 18. Получение спиртов Некоторые из показанных выше реакций (рис. 6,9,10) обратимы и при изменении условий могут протекать
- 19. Этанол образуется и при так называемом спиртовом брожении сахаров, например, глюкозы С6Н12О6. Процесс протекает в присутствии
- 20. Применение спиртов Способность спиртов участвовать в разнообразных химических реакциях позволяет их использовать для получения всевозможных органических
- 22. Скачать презентацию


















 Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Соединения щелочных металлов
Соединения щелочных металлов Об изучении окислительно-восстановительных реакций в школьном курсе химии. Степени окисления атомов и формулы веществ
Об изучении окислительно-восстановительных реакций в школьном курсе химии. Степени окисления атомов и формулы веществ Відносна молекулярна маса речовини, її обчислення за хімічною формулою
Відносна молекулярна маса речовини, її обчислення за хімічною формулою Алканы
Алканы Химические свойства основных классов неорганических веществ
Химические свойства основных классов неорганических веществ Дистиляттағы цианидтер, алифаттық қатардағы галоген туындылары, хлороформ, хлоралгидрат, төртхлорлы көміртек
Дистиляттағы цианидтер, алифаттық қатардағы галоген туындылары, хлороформ, хлоралгидрат, төртхлорлы көміртек Углеводородное сырье: способы переработки
Углеводородное сырье: способы переработки Предельные углеводороды
Предельные углеводороды Комплесные соединения
Комплесные соединения Мұнай. Мұнайдың шығу тарихы
Мұнай. Мұнайдың шығу тарихы Лекция 1. Периодический закон и периодическая система химических элементов. Индустрия красоты
Лекция 1. Периодический закон и периодическая система химических элементов. Индустрия красоты Салыстырмалы тығыздығы мен элементтердің массалық үлестері бойынша газ күйіндегі заттардың молекулалық формулаларын табу
Салыстырмалы тығыздығы мен элементтердің массалық үлестері бойынша газ күйіндегі заттардың молекулалық формулаларын табу Алкалоидтар түсінігі. Никотин, кофеин,морфин, хинин туралы түсініктер
Алкалоидтар түсінігі. Никотин, кофеин,морфин, хинин туралы түсініктер Неметаллические материалы, используемые в машино- и приборостроении
Неметаллические материалы, используемые в машино- и приборостроении Спирти. 3агальна характеристика спиртів
Спирти. 3агальна характеристика спиртів Алюминий и его соединения
Алюминий и его соединения Метаболизм нуклеиновых кислот
Метаболизм нуклеиновых кислот Азотистые гетероциклические соединения
Азотистые гетероциклические соединения Формы минералов и их агрегатов
Формы минералов и их агрегатов Химические свойства металлов
Химические свойства металлов Що ховається за цифрами? Харчові домішки
Що ховається за цифрами? Харчові домішки Адсорбция-фазалар бөлу беттерінде жүретін бір компоненттің екінші компонентке сіңуі
Адсорбция-фазалар бөлу беттерінде жүретін бір компоненттің екінші компонентке сіңуі Угарный газ
Угарный газ Контрольная работа по дисциплине Физическая химия. Раздел: Электрохимия
Контрольная работа по дисциплине Физическая химия. Раздел: Электрохимия Адсорбция. Разделение однородных и неоднородных смесей
Адсорбция. Разделение однородных и неоднородных смесей Ферум та його сполуки
Ферум та його сполуки Аминокислоты. Белки
Аминокислоты. Белки