Содержание
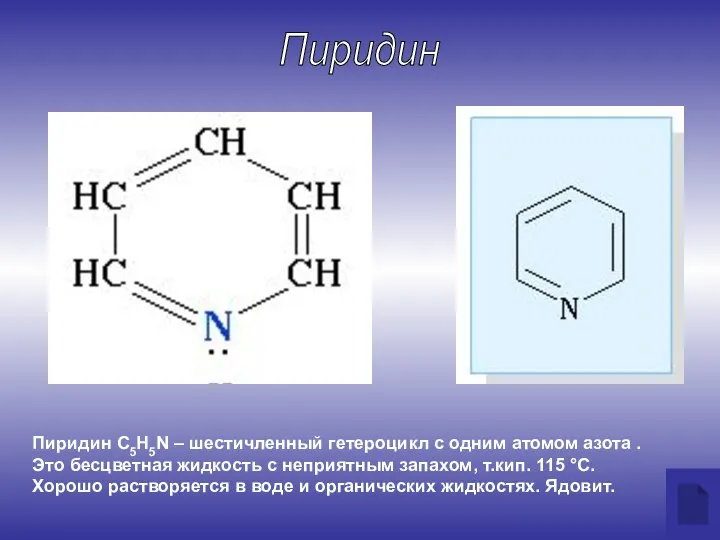
- 2. Пиридин С5H5N – шестичленный гетероцикл с одним атомом азота . Это бесцветная жидкость с неприятным запахом,
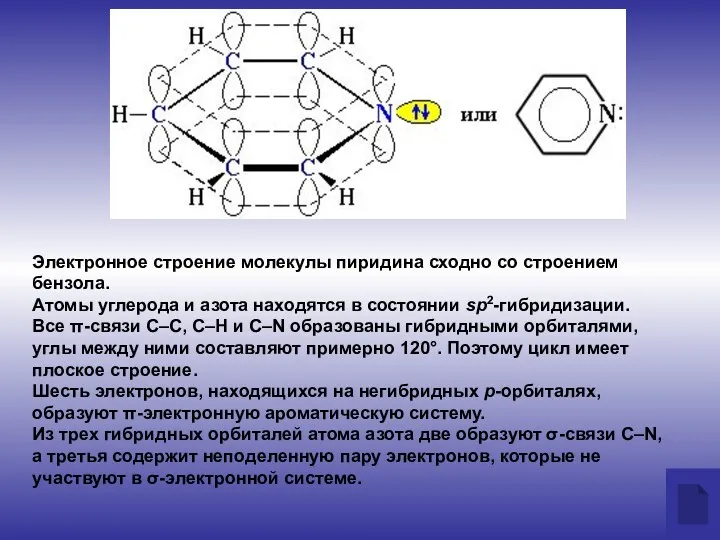
- 3. Электронное строение молекулы пиридина сходно со строением бензола. Атомы углерода и азота находятся в состоянии sp2-гибридизации.
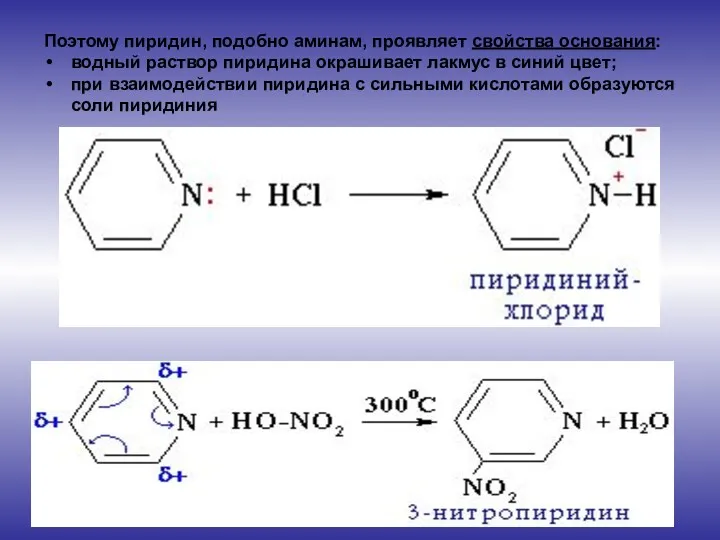
- 4. Поэтому пиридин, подобно аминам, проявляет свойства основания: водный раствор пиридина окрашивает лакмус в синий цвет; при
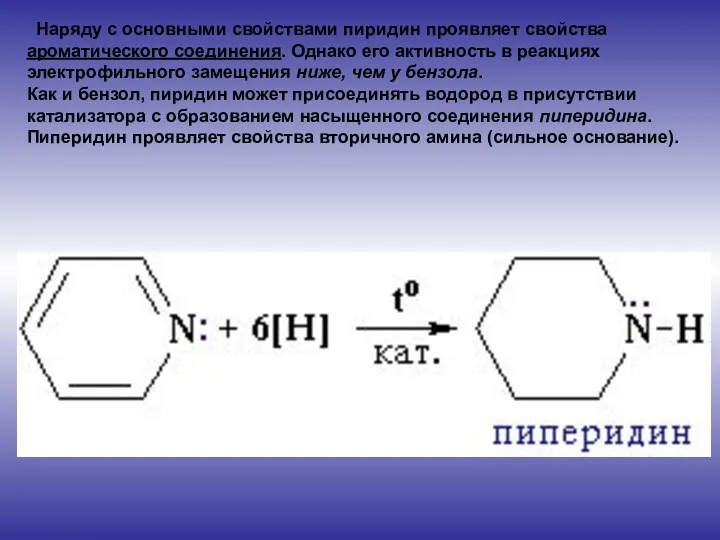
- 5. Наряду с основными свойствами пиридин проявляет свойства ароматического соединения. Однако его активность в реакциях электрофильного замещения
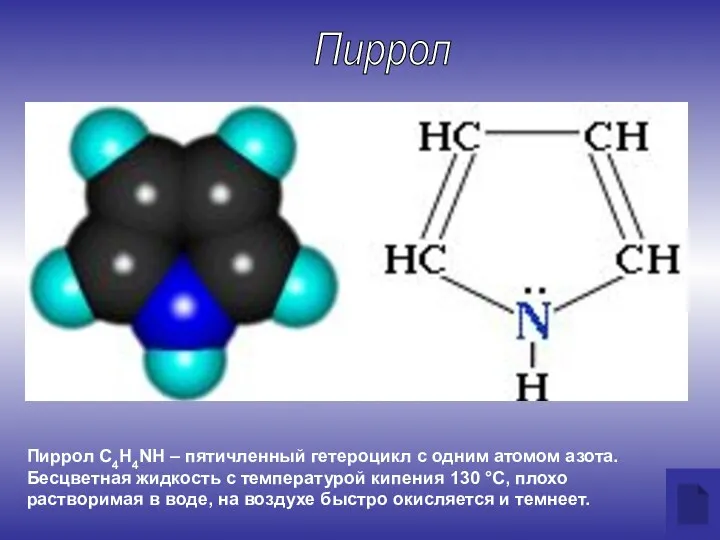
- 6. Пиррол С4H4NН – пятичленный гетероцикл с одним атомом азота. Бесцветная жидкость с температурой кипения 130 °С,
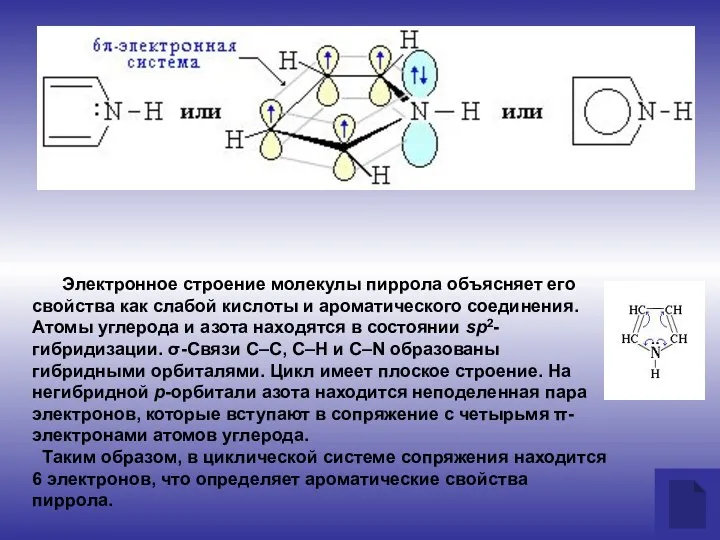
- 7. Электронное строение молекулы пиррола объясняет его свойства как слабой кислоты и ароматического соединения. Атомы углерода и
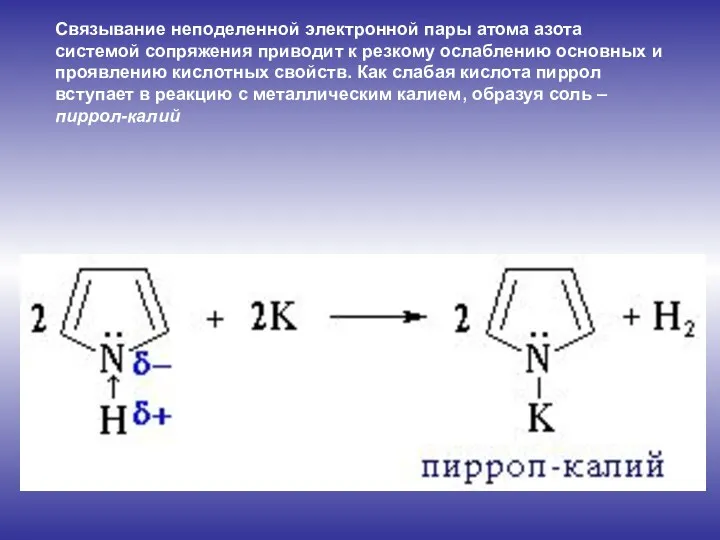
- 8. Связывание неподеленной электронной пары атома азота системой сопряжения приводит к резкому ослаблению основных и проявлению кислотных
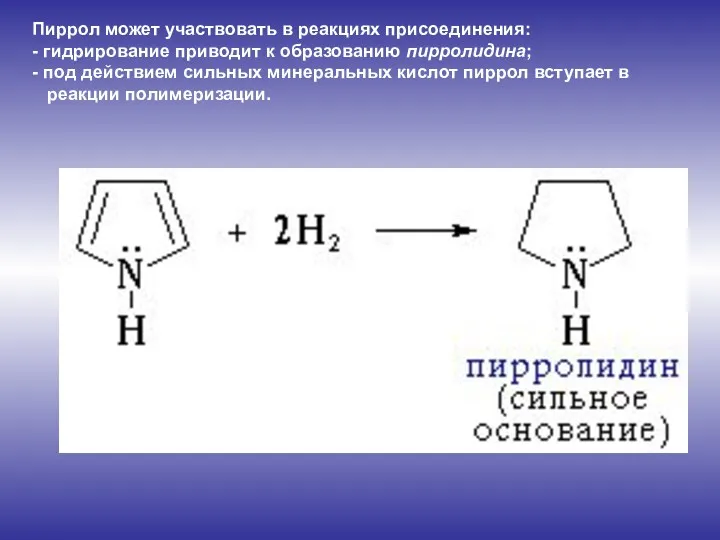
- 9. Пиррол может участвовать в реакциях присоединения: - гидрирование приводит к образованию пирролидина; - под действием сильных
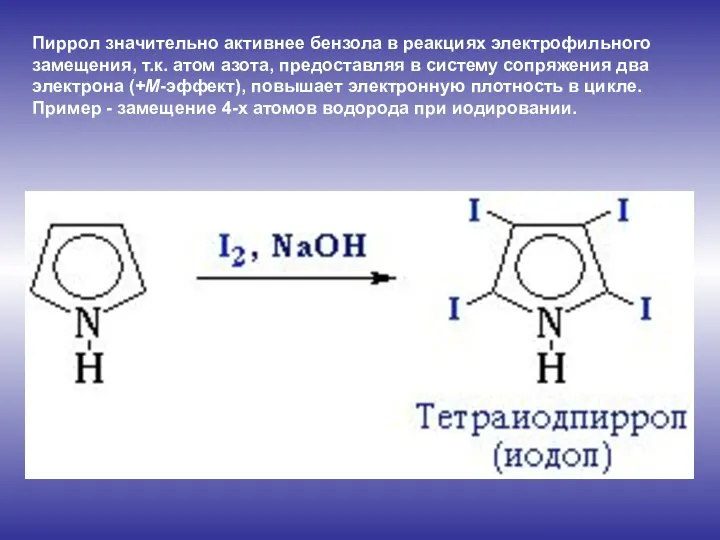
- 10. Пиррол значительно активнее бензола в реакциях электрофильного замещения, т.к. атом азота, предоставляя в систему сопряжения два
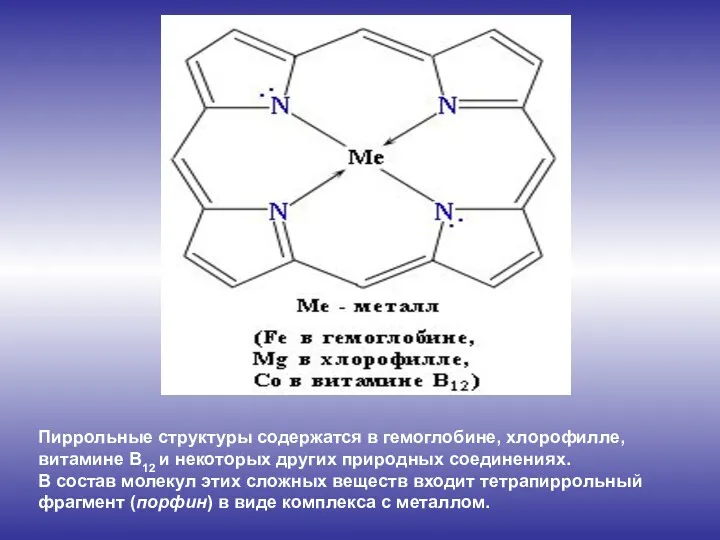
- 11. Пиррольные структуры содержатся в гемоглобине, хлорофилле, витамине В12 и некоторых других природных соединениях. В состав молекул
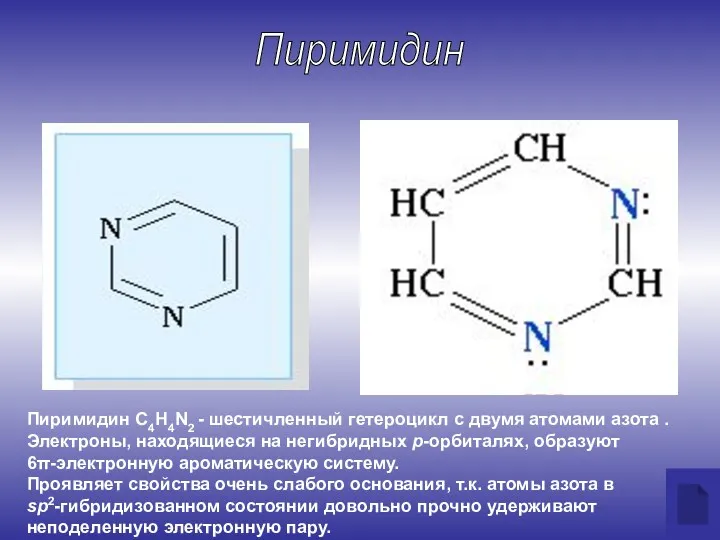
- 12. Пиримидин С4Н4N2 - шестичленный гетероцикл с двумя атомами азота . Электроны, находящиеся на негибридных р-орбиталях, образуют
- 13. Пурин С5H4N4 – соединение, в молекуле которого сочетаются структуры шести- и пятичленного гетероциклов, содержащих по два
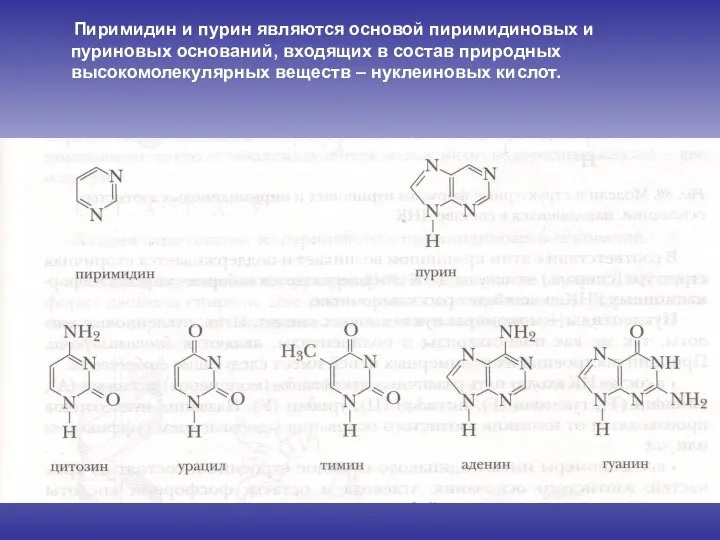
- 14. Пиримидин и пурин являются основой пиримидиновых и пуриновых оснований, входящих в состав природных высокомолекулярных веществ –
- 15. Пуриновые основания − производные пурина, входящие в состав нуклеиновых кислот: аденин и гуанин . Для гуанина
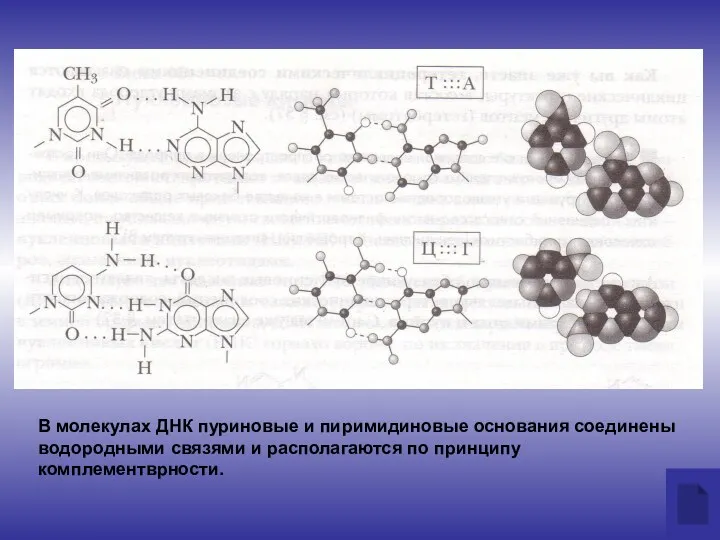
- 16. В молекулах ДНК пуриновые и пиримидиновые основания соединены водородными связями и располагаются по принципу комплементврности.
- 18. Скачать презентацию


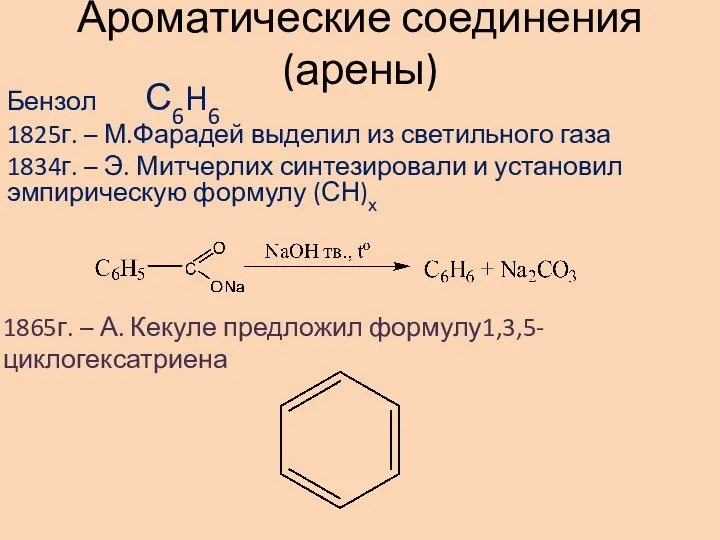 Ароматические соединения (арены)
Ароматические соединения (арены) Лихеоиндикация. Экологические аспекты переработки полимеров
Лихеоиндикация. Экологические аспекты переработки полимеров Аминокислоты. Изомерия. Белки
Аминокислоты. Изомерия. Белки Effect of anodizing parameters on growth of selfordering TiO2
Effect of anodizing parameters on growth of selfordering TiO2 Сполуки основних класів у будівництві і побуті
Сполуки основних класів у будівництві і побуті Химия в строительстве
Химия в строительстве Характеристика s,p,d,f - элементов
Характеристика s,p,d,f - элементов Crystal defects
Crystal defects Геохимия магматического процесса
Геохимия магматического процесса Вода - основа жизни
Вода - основа жизни Карбоновые кислоты. Тест
Карбоновые кислоты. Тест Радиоактивные элементы
Радиоактивные элементы Методика проверки и оценивания заданий с развернутым ответом линии 30 и 31
Методика проверки и оценивания заданий с развернутым ответом линии 30 и 31 Кислород. Оксиды. Валентность
Кислород. Оксиды. Валентность Физические свойства металлов
Физические свойства металлов Water
Water Каменный уголь. Физические и химические свойства
Каменный уголь. Физические и химические свойства Методы окислительно-восстановительного и комплексонометри-ческого титрования
Методы окислительно-восстановительного и комплексонометри-ческого титрования Твердые вещества
Твердые вещества Кремний. Основные минералы кремния
Кремний. Основные минералы кремния Кaрбоновые кислоты
Кaрбоновые кислоты Твёрдое агрегатное состояние. Кристалические решетки. Урок 4
Твёрдое агрегатное состояние. Кристалические решетки. Урок 4 Детонаційна стійкість бензину
Детонаційна стійкість бензину Сущность процесса электролитической диссоциации
Сущность процесса электролитической диссоциации Основные понятия и законы химии. 10 класс
Основные понятия и законы химии. 10 класс Mechanistic insights into the aminolysis of 3,4-epoxysulfolane
Mechanistic insights into the aminolysis of 3,4-epoxysulfolane Азотная кислота и её свойства
Азотная кислота и её свойства Биомакромолекулы. Нуклеиновые кислоты
Биомакромолекулы. Нуклеиновые кислоты