2. Специфические свойства азотной кислоты
А) Разлагается на свету:
4HNO3 = 4NO2 +
2H2O +O2 (на свету) обратимая реакция
4NO2 + 2H2O + O2 = 4 HNO3
Хранить азотную кислоту необходимо в прохладном темном месте.
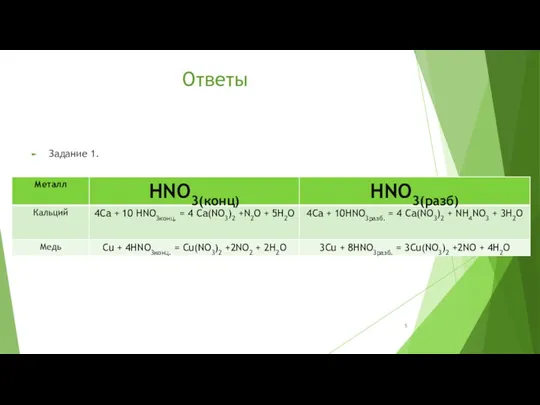
Б) Взаимодействие с металлами (кроме Au, Pt) = соль + H2O + …
HNO3
Концентрированная
Разбавленная
Без нагревания не взаимодействует с Al, Cr, Fe
C активными металлами (до Al) получатся N2O
C малоактивными металлами получатся NO2
Cо щелочными и щелочноземельными металлами
получатся NH4NO3
С Mg - Zn
Получатся N2
с очень разбавленной NH4NO3
После Zn
Получается NO












 Галогены
Галогены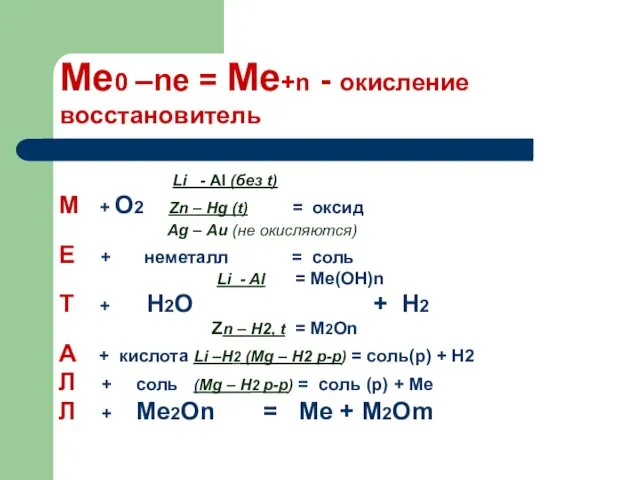 Коррозия металлов
Коррозия металлов Заключительный урок в 8 классе Тест по химии.
Заключительный урок в 8 классе Тест по химии. Технология производства сложных полиэфиров
Технология производства сложных полиэфиров Вред Coca-Cola на организм человека
Вред Coca-Cola на организм человека Оксиды и гидроксиды металлов. 11 класс
Оксиды и гидроксиды металлов. 11 класс Непредельные углеводороды
Непредельные углеводороды Аммиак
Аммиак Мыло
Мыло Олово и свинец
Олово и свинец Судың диссоциациялануы. Сутектік көрсеткіш. Тұздар гидролизі
Судың диссоциациялануы. Сутектік көрсеткіш. Тұздар гидролизі Химия в сельском хозяйстве. Химизация сельского хозяйства и ее направления
Химия в сельском хозяйстве. Химизация сельского хозяйства и ее направления Ультраосновные породы (гипербазиты)
Ультраосновные породы (гипербазиты) Коррозия металлов
Коррозия металлов Строение атома. Периодический закон и периодическая система элементов
Строение атома. Периодический закон и периодическая система элементов Кислородные соединения азота
Кислородные соединения азота Карбоновые кислоты
Карбоновые кислоты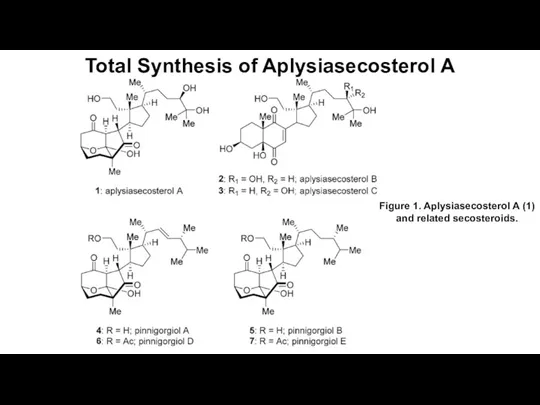 Total Synthesis of Aplysiasecosterol A
Total Synthesis of Aplysiasecosterol A Кислоты и основания. (Лекция 16)
Кислоты и основания. (Лекция 16) Stirring in liquid media
Stirring in liquid media Химия в быту
Химия в быту Ископаемые углеводороды
Ископаемые углеводороды NaHSO4. Гидросульфат натрия
NaHSO4. Гидросульфат натрия Современные тенденции развития химии
Современные тенденции развития химии Иондық байланыс
Иондық байланыс Вклад ученых-химиков в победу в Великой Отечественной войне
Вклад ученых-химиков в победу в Великой Отечественной войне ЕГЭ по химии. Анализ результатов решения (часть 2)
ЕГЭ по химии. Анализ результатов решения (часть 2) Органические и неорганические кислоты
Органические и неорганические кислоты